-
下列属于碱性氧化物的是( )
A. CO2 B. NaCl C. Na2O D. Mg(OH)2
难度: 简单查看答案及解析
-
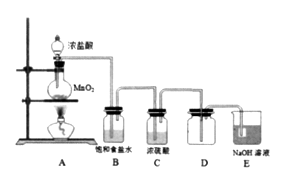
仪器名称为“冷凝管”的是( )
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
下列物质的水溶液能导电,但属于非电解质的是( )
A. CO2 B. CH3COOH C. KCl D. Fe
难度: 中等查看答案及解析
-
下列属于氧化还原反应的是( )
A. CO2+2NaOH =Na2CO3+H2O B. HCl+ NaOH = NaCl + H2O
C. Cl2+2NaOH = NaCl+NaClO+H2O D. NH4Cl + NaOH = NH3·H2O + NaCl
难度: 简单查看答案及解析
-
下列分散系能用半透膜分离出分散质的是( )
A. CuSO4溶液 B. 盐酸 C. 生理盐水 D. 淀粉溶液
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A. 氯碱工业的反应原理是电解熔融氯化钠
B. 纯碱在造纸工业中有着重要的应用
C. 水玻璃可用于建筑黏合剂
D. 铁的化合物在人体内发生氧化还原反位起传递电子作用
难度: 中等查看答案及解析
-
下列表示正确的是( )
A. HClO的结构式 H-Cl-O B. CC14的电子式
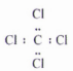
C. Na+离子的结构示意图
 D. 乙醇的球棍模型
D. 乙醇的球棍模型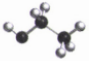
难度: 简单查看答案及解析
-
下列能使湿润的淀粉碘化钾试纸变蓝的气体是( )
A. CO2 B. Cl2 C. NH3 D. HCl
难度: 中等查看答案及解析
-
2017年3月28 日,中国成功开采可燃冰,主要成分为甲烷,属于一次能源。下列不属于 一次能源的是( )
A. 石油 B. 风能 C. 太阳能 D. 氢能
难度: 简单查看答案及解析
-
下列说法正确的是
A. 硫酸铜粉末是常见的干燥剂,具有较强的吸水能力 B. 漂白粉的主要成分是Ca(ClO)2
C. 保存氯化亚铁溶液时,需加入少量铁粉 D. 氨气能使湿润的蓝色石蕊试纸变红
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. C2H4和C3H6互为同系物 B. 168O表示质子数为8、中子数为8的核素
C.
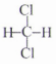 和
和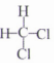 互为同分异构体 D.
互为同分异构体 D.  的名称是2-乙基丁烷
的名称是2-乙基丁烷难度: 中等查看答案及解析
-
在一定条件下,可逆反应2X(g)+Y(s)
2Z(g)△H=-akJ·mol-1,下列说法一定正确的是( )
A. 当反应消耗1molY时,反应放出akJ的热量
B. 当反应达到平衡时,X、Y、Z 三者的物质量之比为2∶1∶2
C. 当反应达到平衡时,压缩体积,X的正、逆反应速率都增大,平衡向正反应方向移动
D. 恒温恒容,反应达到平衡后,加入1molY平衡向正反应方向移动
难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A. 食醋除去水垢中的碳酸钙:CaCO3+2H+=Ca2++CO2↑+H2O
B. 小苏打治疗胃酸过多的反应:CO32-+2H+=CO2↑+ H2O
C. 氢氧化钡溶液与硫酸溶液反应:Ba2++2OH-+2H++SO42- =BaSO4↓+2H2O
D. 碳酸氢铵溶液与过量氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O
难度: 中等查看答案及解析
-
M、W、X、Y、Z五种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( )
W
Z
X
Y
M
A. M、W、Z的原子半径依次减小
B. Y元素与氢元素可形成YH4、Y2H4、Y3H8等多种化合物
C. M、W、Y的最高价氧化物对应水化物的酸性依次降低
D. 工业上常用W与YZ2反应制备Y,同时生成WZ2
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 可以利用溴水区分裂化汽油和直馏汽油
B. 煤的气化是指高温下煤与水蒸汽反应生成CO、CH4、H2、焦炉气的过程
C. 乙烯、苯均能与H2发生加成反应,说明二者均含碳碳双键
D. 相同质量的乙炔、苯分别在足量的氧气中燃烧,苯比乙炔消耗的氧气质量多
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 油脂是热值最高的营养物质,也可制造油漆
B. 氨基酸可通过脱水缩合直接形成蛋白质
C. 检验淀粉在稀硫酸条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热,观察是否有砖红色沉淀
D. 鸡蛋清溶液中加入饱和硫酸铵溶液、饱和硫酸铜溶液均会发生盐析而凝聚
难度: 中等查看答案及解析
-
铁电池是一种新兴的化学电源,总反应方程式:3Zn+2FeO42-+8H2O= 3Zn(OH)2↓+ 2Fe(OH)3↓+4OH-,其工作示意图如下。
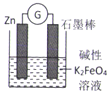
下列说法不正确的是( )
A. Zn极上发生氧化反应
B. 电解质溶液中电子由左侧向右侧转移
C. 正极的电极反应式:FeO42-+3e-+4H2O=Fe(OH)3+5OH-
D. 反应一段时间后,Zn极质量减少6.5g,假设反应前后溶液体积不变仍为100 mL,则OH-浓度约增大了 1.33 mol·L-1
难度: 中等查看答案及解析
-
室温下,不能说明HCO3-为弱电解质的是( )
A. 0.01mol·L-1 HCO3-溶液pH大于2 B. NaHCO3溶液显碱性
C. 向紫色石蕊试液中呼气,溶液变红色 D. 向Na2CO3溶液滴加醋酸,有气泡产生
难度: 中等查看答案及解析
-
已知断开lmolO2(g)中的共价键,需要吸收dkJ的能量,根据下表键能(键能是指拆开1 mol气态物质中某种共价键需要吸收的能量)数据,下列热化学方程式正确的是( )
共价键
键能/kJ·mol-1
H—C
a
H—O
c
C=O
b
A. CH4(g)+2O2(g) = CO2(g)+2H2O(g) △H= ( 2b+2c -4a-2d ) kJ·mol-1
B. CH4(g)+2O2(g) = CO2(g)+2H2O(l) △H= ( 4a+2d-2b-2c ) kJ·mol-1
C. CH4(g)+2O2(g) = CO2(g)+2H2O(1) △H=( 4a+2d-2b-4c ) kJ·mol-1
D. CH4(g)+2O2(g) = CO2(g)+2H2O(g) △H= (4a+2d-2b-4c ) kJ·mol-1
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. CCl4、C2H4、SiO2都存在共价键,它们都是共价化合物
B. SO2溶于水时,需克服共价键和分子间作用力
C. 某物质在熔融状态能导电,则该物质中一定含有离子键
D. CO2和N2中,每个原子的最外层都具有8电子稳定结构
难度: 中等查看答案及解析
-
对H2O2的分解速率影响因素进行研究。在相同温度下,实验测得不同条件下出O2浓度随时间变化如图所示。下列说法不正确的是( )

A. 图甲表明,可通过适当增大H2O2浓度,加快H2O2分解速率
B. 图乙表明,可通过调节溶液的酸碱性,控制H2O2分解速率快慢
C. 图丙表明,Mn2+少量存在时,碱性太强,不利于H2O2分解
D. 图乙、图丙和图丁表明,Mn2+是H2O2分解的催化剂,提高Mn2+的浓度就能增大H2O2 分解速率
难度: 困难查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 12g金刚石含有的C-C键数为2 NA,6.0g二氧化硅含有的Si-O键数为0.4NA
B. lmol硫在空气中完全燃烧生成SO3消耗的氧气分子数为3NA
C. 常温常压下,2.24LCO2和N2O混合物中所含有的原子数为0.3NA
D. 4.6g金属钠与500mL0.2mol·L-1的盐酸充分反应,转移电子数为0.1NA
难度: 困难查看答案及解析
-
在25℃时,向l0mL0.01mol·L-1NaA溶液中逐滴加入0.01mol·L-1的盐酸,滴定曲线如下图所示,下列说法正确的是( )
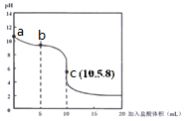
A. a点到c点的过程中,c(HA)+c(A-)=0.01mol·L-1等式始终成立
B. b点时,溶液中微粒浓度大小的关系:c(A-)>c(Cl-)>c(HA)>c(OH-)>c(H+)
C. c点溶液存在的关系:c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-)
D. 由图可知,等浓度的HA、NaA混合溶液中,HA的电离程度大于A-的水解程度
难度: 困难查看答案及解析
-
聚合硫酸铁(PFS)是水处理中重要的絮凝剂,以废铁屑为原料制备PFS的具体工艺流程如下:
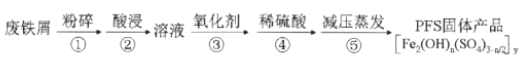
下列说法不正确的是( )
A. 步骤①,粉碎的目的是增大反应物接触面积,提高“酸浸”反应速率
B. 步骤③,可选用H2O2、Cl2、KMnO4等氧化剂将Fe2+转化为Fe3+
C. 步骤④,加稀硫酸调节pH在一定范围内,若pH偏小则Fe3+水解程度太弱,若pH偏大时则形成Fe(OH)3沉淀
D. 步骤⑤,减压蒸发,有利于降低蒸发温度防止产物分解
难度: 中等查看答案及解析
-
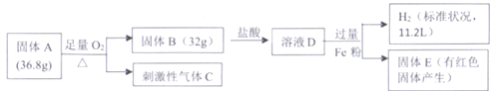
已知:AgOH很不稳定,易分解生成Ag2O(黑色)。溶液X中可能含有下列离子:Ag+,NH4+、Fe3+、SO42-、SO32-、Cl-中的几种离子。为了确定其组成,某同学进行了如下实验:
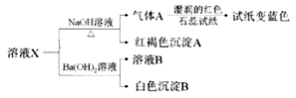
下列说法不正确的是( )
A. 溶液X与NaOH反应生成红褐色沉淀A,可推测该溶液中不存在SO32-
B. 溶液X中一定不含Ag+
C. 溶液X中一定存在NH4+、Fe3+、SO42-
D. 取少量溶液B,加入AgNO3溶液,若有沉淀产生,则有Cl-
难度: 困难查看答案及解析

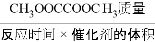
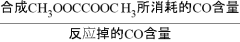 ×100%
×100%