-
下列材料中,属于有机合成材料的是
A.蚕丝. B.羊毛 C.涤纶 D.棉花
难度: 简单查看答案及解析
-
下列说法不符合科学道理的是( )
A. 人体如缺钙可能患佝偻病 B. 胃酸过多可喝烧碱液中和
C. 燃烧鉴别羊毛和化纤织品 D. 天然气泄漏不能点火检查
难度: 简单查看答案及解析
-
下列肥料属于复合肥料的是
A.NH4NO3 B.KNO3 C.KCl D.Ca(H2PO4)2
难度: 简单查看答案及解析
-
化学与日常生活、工农业生产密切相关。下列说法中不正确的是
A. 用含有碳酸氢钠的发酵粉焙制糕点
B. 工业上用熟石灰处理硫酸厂的污水
C. 医疗上用纯酒精作消毒剂
D. 生活中用含有NaOH的清洁剂去油污
难度: 简单查看答案及解析
-
下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减小的是()
A、.烧碱 B、石灰水 C、浓盐酸 D、氯化钠
难度: 中等查看答案及解析
-
一般情况下,两种活泼性不同的金属在潮湿的环境中接触时,活泼性强的金属首先被腐蚀。为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌的金属是( )
A. 锌板 B. 银板 C. 铜板 D. 锡板
难度: 简单查看答案及解析
-
下列化肥属于复合肥料的是( )
A. 硝酸钾 B. 氯化钾 C. 碳酸氢钠 D. 氨水(NH3•H2O)
难度: 中等查看答案及解析
-
实验室配制50g质量分数为6%的氯化钠溶液,整个配制过程如图所示,其正确的操作顺序是
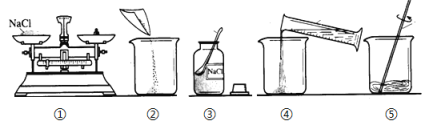
A.③①②④⑤ B.①③④②⑤ C.③①④②⑤ D.①④③②⑤
难度: 中等查看答案及解析
-
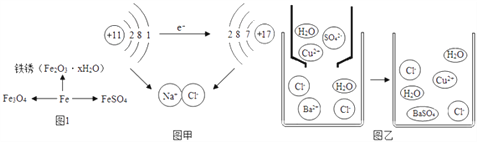
可园学校化学兴趣小组的同学在实验室发现有一瓶无色溶液,由于保管不当,标签残缺不全.下列分析与判断不正确的是( )
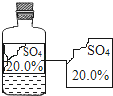
A. 这瓶溶液的pH值一定为7
B. 这瓶溶液不可能是硫酸铜溶液
C. 这瓶液体不可能是碱
D. 这瓶溶液中不一定含有金属元素
难度: 困难查看答案及解析
-
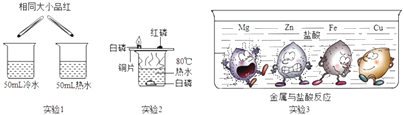
如图是初中化学中几个重要实验,有关该几个实验的说法错误的是( )
A.

实验中热水的作用是隔绝氧气和提供热量
B.
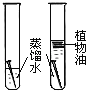
实验中左边试管中铁钉生锈而右边试管中铁钉不生锈,可证明铁生锈的条件之一是与氧气接触
C.

实验可证明分子是不断运动的
D.

实验中下层蜡烛先熄灭,上层蜡烛后熄灭,能证明二氧化碳的密度比空气大且不能燃烧,也不能支持燃烧
难度: 中等查看答案及解析
-
有关实验现象的叙述正确的是( )
A. 白磷在空气中燃烧产生白色烟雾
B. 铵盐与熟石灰混合研磨都会生成无色无味的气体
C. 鉴别稀食盐水和醋酸,取样分别滴加紫色石蕊溶液,溶液变红的是醋酸
D. 将锌粒、镁带分别放入等浓度的稀盐酸中,锌粒反应更剧烈
难度: 中等查看答案及解析
-
我市有些滩涂地区的土壤被称为"盐碱地",当地农民常用引进内河淡水浸泡再排水的方法改良土壤。若以土壤pH为纵坐标,浸泡水次数(m)为横坐标,下列能正确表示土壤pH变化的图像的是
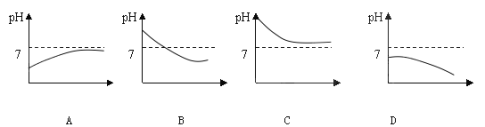
难度: 简单查看答案及解析
-
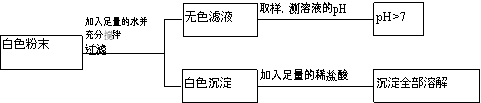
一包由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液X。在滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体。下列判断错误的是
A. 原白色粉末的组成有3组可能
B. 原白色粉末中一定含有CaCO3
C. 原白色粉末中一定不含有CuSO4
D. 若向无色滤液X中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl2、NaOH
难度: 中等查看答案及解析
-
除去下列物质中混有的少量杂质(括号内为杂质),所用方法错误的是
A.CO(CO2):通过氢氧化钠溶液、干燥
B.N2(O2):通过灼热的铜网
C.Cu粉(Fe):加稀硫酸
D.CaO(CaCO3):溶解、过滤、蒸发
难度: 简单查看答案及解析
-
某学生要配制质量分数为10%的食盐溶液,他读量筒中水的体积刻度时,视线仰视.而调节天平平衡时,指针偏左,称量食盐时天平平衡,则他配制的食盐溶液的质量分数( )
A.等于10% B.小于10% C.大于10% D.无法确定
难度: 中等查看答案及解析
-
推理和归纳是化学学习和研究中常用的思维方法。下列推理正确的是( )
A. 稀有气体可做保护气,可做保护气的一定是稀有气体
B. 单质是由一种元素组成的物质,由一种元素组成的物质一定是单质
C. 性质活泼的金属在空气中容易被腐蚀,铝在空气中不易被腐蚀是因为其性质不活泼
D. 可燃物在有限空间燃烧能发生爆炸,面粉粉尘在仓库内遇明火也可能爆炸
难度: 困难查看答案及解析
-
业制镁的方法为:将含碳酸钙的贝壳制成石灰乳;在海水(含氯化镁)中加入石灰乳,过滤;在氢氧化镁中加入盐酸,结晶;电解熔融氯化镁得到镁。该方法中涉及的化学反应不包括
A. 分解反应 B. 化合反应 C. 置换反应 D. 复分解反应
难度: 中等查看答案及解析
-
下列生活中的有关问题,处理正确的是
A.我们可以用甲醛的稀溶液对水产品进行处理,延长保鲜时间
B.生活中,可以把稀盐酸倒入铝制水壶中充分的浸泡,便于除去水壶中的水垢
C.液化气泄漏着火时,应立刻关闭阀门,并开窗通风
D.钢铁在潮湿的环境中比在干燥环境中容易生锈
难度: 简单查看答案及解析