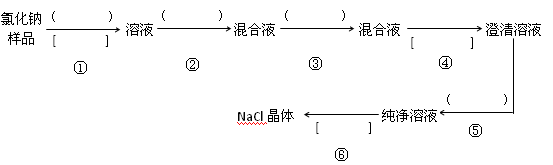
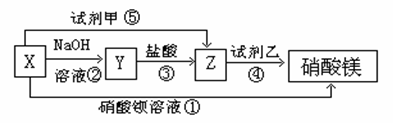
-
下列叙述正确的是 ( )
A.1 mol H2O的质量为18g/mol B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g D.标准状况下,1 mol任何物质体积均为22.4L
难度: 简单查看答案及解析
-
下列离子反应方程式,书写正确的是.( )
A. 向碳酸钠溶液中加盐酸 CO32- + 2H+ = H2O +CO2 ↑
B.向稀硫酸溶液中投入铁粉 2Fe +6H+ = 2Fe3+ +3H2 ↑
C. 向盐酸中投入碳酸钙 CO32- + 2H+ = H2O +CO2 ↑
D. 氢氧化钡溶液中加入硫酸 H+ + OH- =H2O
难度: 简单查看答案及解析
-
配制一定体积、一定物质的量浓度的溶液时,下列会使配得的溶液浓度偏小的是( )
A. 容量瓶中原有少量蒸馏水
B. 溶液从烧杯转移到容量瓶中后洗涤了烧杯
C.定容时观察液面俯视
D.定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线
难度: 简单查看答案及解析
-
下列关于分散系的说法,正确是………………………………………………( )
A.稀硫酸不是分散系
B.一种分散系里只有分散质和分散剂两种物质
C.分散剂一定是液体
D.按分散质和分散剂的状态(气、液、固态),有9种组合方式
难度: 简单查看答案及解析
-
氢化钙中的氢元素为-1价,它可用做生氢剂,反应的化学方程式是:
CaH2+2H2O==Ca(OH)2+2H2↑。该反应中,水的作用是. ( )
A.溶剂 B.还原剂 C.氧化剂 D.既是还原剂又是氧化剂
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述不正确的是. .( )
A.标准状况下,22.4LH2含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+数为0.02 NA
C.标准状况下,1 NA CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol /L的MgCl2溶液中,含有Cl- 个数为1 NA
难度: 简单查看答案及解析
-
下列变化中,必须加入氧化剂才能发生的是( )
A. SO2→S B. SO32—→SO2 C. I- →I2 D. HCO3—→CO32—
难度: 简单查看答案及解析
-
下列电离方程式,书写正确的是…………… ………… ( )
A. Al2(SO4)3 =2Al3+ + 3SO42- B.AlCl3 = Al3+ +Cl3-
D. Mg(NO3)2 = Mg+2 +2NO3- D.KMnO4 =K+ +Mn7+ +4O2-
难度: 简单查看答案及解析
-
下列说法正确的是……………………… …… ( )
A.易溶于水的物质一定是电解质 B.液态氯化氢能导电
C.液态氯化钠能导电 D.熔融的液态钠是电解质
难度: 简单查看答案及解析
-
下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是 ( )
A.蒸发 B.蒸馏 C. 升华 D.萃取
难度: 简单查看答案及解析
-
下列反应中,铁元素被氧化的是…………………………………………….( )
A.FeS +2HCl = FeCl2 + H2S↑ B. Fe +H2SO4 = FeSO4 +H2↑
C. FeO + 2HCl =FeCl2 +H2O D. Fe2O3 +3CO = 2Fe +3CO2
难度: 简单查看答案及解析
-
下列各组,可用交叉分类法进行分类的是…………………………………..( )
A.Na2CO3 、Na2SO4、K2CO3、K2SO4 B.石灰石、氯化钙、纯碱、氯化钠
C.干冰、一氧化碳、石墨、金刚石 D.氢气、盐酸、苛性碱、小苏打
难度: 简单查看答案及解析
-
下列实验操作中错误的是 ..( )
A.蒸发时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取时,溶剂要互不相溶,溶质在两种溶剂中的溶解度相差很大
难度: 简单查看答案及解析
-
在水溶液中能大量共存,且加入过量稀硫酸溶液时,有气体生成的是………( )
A. Na+ 、 Ag+ 、CO32- 、Cl- B. K+ 、 Ba2+ 、 SO42- 、 Cl-
C. Na+ 、 K+ 、CO32- 、Cl- D. Na+ 、K+ 、 Cl- 、 SO42—
难度: 简单查看答案及解析
-
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是………………………..( )
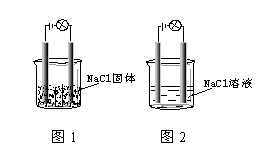
A. NaCl是非电解质
B. NaCl溶液是电解质。
C. NaCl在水溶液中电离出了可以
自由移动的离子。
D. NaCl溶液中水电离出大量的离子
难度: 简单查看答案及解析
-
下列各组微粒中,在酸性条件下均可以做氧化剂的是………………………( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
以水为分散剂的分散系,按稳定性由强到弱的顺序排列的是… ( )
A. 溶液、胶体、浊液 B. 浊液、胶体、溶液
C. 胶体、浊液、溶液 D. 浊液、溶液、胶体
难度: 简单查看答案及解析
-
正确书写离子方程式时,应使等号两边……………………… ( )
A.离子的物质的量相等 B.微粒的总的数量应相等
C.正电荷和负电荷总数应相等 D.电荷量和各元素原子的物质的量应相等
难度: 简单查看答案及解析
-
某元素在化学反应中由化合态变为游离态,则该元素…………… ( )
A.一定被氧化了 B.一定被还原了
C.既可能被氧化也可能被还原 D.既不可能被氧化,也不可能被还原
难度: 简单查看答案及解析
-
欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是.. ( )
① 将14.2 g Na2SO4 溶于100ml水中
② 将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③ 将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A.①② B.②③ C.①③ D.①②③
难度: 简单查看答案及解析