-
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是( )
A.1molO2参加反应,一定得4×6.02×1023个电子
B.7.5g SiO2晶体中含有硅氧键数为0.5×6.02×1023
C.2.24L CH4中含有的原子数为0.5×6.02×1023
D.250mL 2mol/L的氨水中含有NH3•H2O的分子数为0.5×6.02×1023难度: 中等查看答案及解析
-
表示下列各反应的离子方程式,不正确的是( )
A.铁溶于足量的稀硝酸:Fe+4H++NO3-═Fe3++NO↑+2H2O
B.碳酸氢镁溶液中加入足量的澄清石灰水:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O
C.足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32-+H2O═2NaHCO3↓
D.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-难度: 中等查看答案及解析
-
下列关于元素的叙述正确的是( )
A.非金属元素间不可能形成离子化合物
B.只有在原子中,质子数才与核外电子数相等
C.目前使用的元素周期表中,最长的周期含有32种元素
D.目前使用的元素周期表中,包含元素种类最多的族为ⅥA难度: 中等查看答案及解析
-
在AlCl3和FeCl3的混合液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得到的沉淀物是( )
A.Fe2S3、I2
B.Al(OH)3、I2
C.Fe(OH)3、Al(OH)3
D.FeS、S、Al(OH)3难度: 中等查看答案及解析
-
有一种锂电池,用金属锂和石墨做电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(
)中而形成的,电池总反应方程式为:8Li+3SOCl2═6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1难度: 中等查看答案及解析
-
在一密闭容器中通入A、C、D各为2mol和xmolB,按下式发生反应:A(g)+4B(g)
2C(g)+D(g);△H>0达到平衡,下列说法错误的是( )
A.若容器容积可变,且保持温度和压强不变,A、B、C、D的物质的量均加倍或减半,平衡不移动
B.若容器的容积可变,且保持温度和压强不变,A、B、C、D的物质的量均增加1mol,平衡一定右移
C.若容器的容积可变,且保持压强不变,降低温度时,容器的容积可能变大
D.若容器的容积固定,且通过调节温度使反应达到平衡时保持容器中气体总物质的量为10mol,当起始反应正方向进行时,x的取值范围是4<x<8难度: 中等查看答案及解析
-
已知0.1mol•L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)难度: 中等查看答案及解析
-
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)与对应选项不正确的是( )
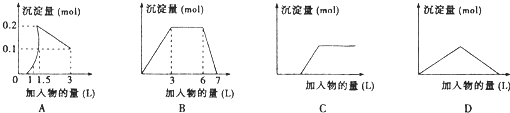
A.向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合液中加入0.1 mol/L稀H2SO4溶液
B.向含有0.1 mol/L AlCl3和0.3mol/L NH4Cl的1L混合液中加入0.1mol/L NaOH溶液
C.向烧碱溶液中滴加明矾溶液
D.向Ca(OH)2溶液中逐渐通入二氧化碳难度: 中等查看答案及解析