-
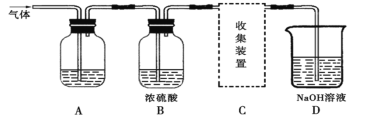
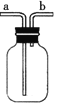
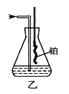
汽车在剧烈碰撞后,安全气囊会弹出并充满一种保护气体。该气体在空气中含量最高,其分子式为
A. O2 B. CO C. N2 D. CO2
难度: 中等查看答案及解析
-
下列做法不能体现低碳生活的是
A. 减少食物加工过程 B. 注意节约用电
C. 尽量购买本地的、当季的食物 D. 大量使用薪柴为燃料
难度: 中等查看答案及解析
-
下列“化学与生活”的说法错误的是
A. 硫酸钡可用作白色颜料 B. 石膏可用来调节水泥的凝固时间
C. 胆矾可用于检验酒精中是否有水 D. 硫酸可用来制药
难度: 简单查看答案及解析
-
下列过程属于大气固氮的是
A. 分离液态空气制氮气 B. 合成氨
C. 闪电时N2转化为NO D. 豆科作物根瘤菌将N2转化为NH3
难度: 简单查看答案及解析
-
下列化合物可由两种单质直接化合得到的是
A. SO3 B. NO2 C. CuS D. FeS
难度: 简单查看答案及解析
-
可用碱石灰干燥的气体是
A. H2S B. Cl2 C. NH3 D. SO2
难度: 简单查看答案及解析
-
不能用启普发生器制取的气体是
A. H2S B. SO2 C. CO2 D. H2
难度: 中等查看答案及解析
-
科学家发现微量硫化氢可以调节心血管功能。有关硫化氢的叙述正确的是
A. 硫化氢不稳定,受热易分解
B. 硫化氢是无色无味并且有毒的气体
C. 硫化氢分子中所有原子的最外电子层都达到8电子稳定结构
D. 硫化氢能溶于水形成一种弱酸,其电离方程式是H2S
2H+ + S2-
难度: 简单查看答案及解析
-
对下列事实的解释错误的是
A. 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B. 胆矾受热后变色,说明胆矾受热不稳定
C. 常温下,浓硫酸可以用铝槽贮存,说明铝与浓硫酸不反应
D. 反应FeS +H2SO4==FeSO4+H2S↑能进行,说明硫化氢难溶于硫酸溶液,是弱酸
难度: 中等查看答案及解析
-
常温下,将铁片投入浓H2SO4中,下列说法正确的是
A. 不发生反应 B. 铁被钝化 C. 产生大量SO2 D. 产生大量H2
难度: 简单查看答案及解析
-
二氧化硫能使浸过溴水的滤纸褪色,这说明了
A. 二氧化硫的漂白性 B. 溴的挥发性 C. 溴的氧化性 D. 二氧化硫的氧化性
难度: 中等查看答案及解析
-
常温下,测得某稀盐酸的pH = 2。下列讨论错误的是
A. 该溶液中c(H+)=1×10-2 mol/L B. 该溶液中c(H+)>c((OH—)
C. 该溶液中c(OH- ) =1×10-7 mol/L D. Kw = c(H+)·c(OH- ) = 1×10-14
难度: 简单查看答案及解析
-
能表示人喝水时的胃液的pH变化的图像是
A.
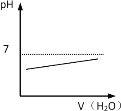
B.
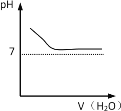
C.
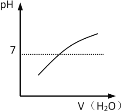
D.
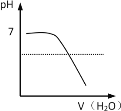
难度: 简单查看答案及解析
-
将SO2气体逐渐通入某溶液,溶液pH随通入SO2气体体积变化如图所示,该溶液是
A. 氨水 B. 氢氧化钠 C. 氢硫酸 D. 氯水
难度: 中等查看答案及解析
-
下列反应中,调节反应物的用量或浓度,不会改变反应产物的是
A. 铁在硫蒸气中燃烧 B. 硫化氢在氧气中燃烧
C. 硫酸中加入锌粉 D. 二氧化碳通入澄清石灰水
难度: 简单查看答案及解析
-
在检验SO42-的过程中,下列操作中正确的是
A. 先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-
B. 先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-
C. 先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-
D. 先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-
难度: 中等查看答案及解析
-
根据下列实验内容得出的结论正确的是
选项
实验内容
结论
A
某气体的水溶液能使红色石蕊试纸变蓝
该气体一定是NH3
B
某气体能使酸性高锰酸钾溶液褪成无色
该气体一定是SO2
C
某物质的水溶液中加入盐酸产生能使澄清石灰水变浑浊的无色气体
该溶液一定含有CO32-
D
某气体完全燃烧,火焰呈淡蓝色
该气体一定是H2S
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
选用一种试剂能把浓度各均为1mol/L的Na2SO4、Na2CO3、Na2S、BaCl2溶液加以区别开,这种试剂是
A. CaCl2 B. H2SO4 C. 盐酸 D. AgNO3
难度: 中等查看答案及解析
-
下列气体溶解于水,发生氧化还原反应的是
A. SO2溶于水 B. NO2溶于水 C. CO2溶于水 D. NH3溶于水
难度: 简单查看答案及解析
-
下图喷泉实验的现象与下列性质无关的是( )
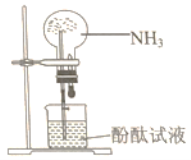
A. 氨易溶于水 B. 氨能与水反应
C. 氨水显碱性 D. 氨易液化
难度: 简单查看答案及解析
-
实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )
A.
 氨气发生装置 B.
氨气发生装置 B. 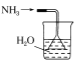 是氨气吸收装置
是氨气吸收装置C.
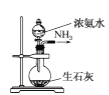 是氨气发生装置 D.
是氨气发生装置 D. 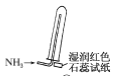 是氨气收集、检验装置
是氨气收集、检验装置难度: 中等查看答案及解析
-
检验铵根离子的实验所依据的是:①氨气极易溶于水;②铵根离子与OH- 间发生反应产生氨气;③NH3·H2O电离出NH4+和OH -;④石蕊在碱性条件下变为蓝色。
A. ②④ B. ①②③④ C. ①②③ D. ②③④
难度: 简单查看答案及解析
-
同时对农作物施用多种化肥,不宜与硫酸铵同时施用的是
A. (NH2)2CO B. KCl C. NH4Cl D. K2CO3
难度: 简单查看答案及解析
-
下列关于催化剂的说法中,正确的是
A. 催化剂在反应过程中始终未参与反应
B. 使用催化剂时,一般要将原料净化,防止催化剂中毒
C. 使用催化剂的同时,若给反应体系进行高温加热,可以加快反应速率
D. 在实验室制氧气、制二氧化碳的实验中都用了二氧化锰作催化剂
难度: 简单查看答案及解析
-
若在已达到平衡的2SO2 + O2
2SO3反应体系中,充入少量的18O2,一段时间后,18O这种原子存在于
A. O2 B. SO2 C. SO3 D. O2、SO2、SO3
难度: 简单查看答案及解析
-
对反应A + 3B
2C + D 来说,下列反应速率中,最大的是
A. v(A)=0.3mol/(L·min) B. v(B)=0.6mol/(L·min)
C. v(C)=0.5mol/(L·min) D. v(D)=0.4mol/(L·min)
难度: 简单查看答案及解析
-
能够充分说明在恒温下的密闭容器中,反应H2(g)+I2(g)
2HI(g)已达到平衡状态的标志是
A. 容器中H2、I2、HI的物质的量之比为1:1:2
B. H2、I2、HI在密闭容器中共存
C. 单位时间内生成2molHI 时,即消耗1molH2
D. 2 v正(H2)=v逆(HI)
难度: 简单查看答案及解析
-
常温下,将甲针筒内20mLH2S推入含有10 mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
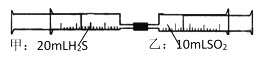
A. 有淡黄色固体生成
B. 有无色液体生成
C. 气体体积缩小
D. 最终约余15mL气体
难度: 简单查看答案及解析
-
已知黑火药爆炸的反应是:S + 2 KNO3 + 3 C== K2S + 3 CO2↑ + N2↑ 。下列关于此反应的讨论正确的是
A. 若12克碳参加反应电子共转移12 mol B. 该反应中还原剂只有碳
C. 该反应中氧化剂只有硝酸钾 D. 反应产物中有两种共价化合物
难度: 中等查看答案及解析