-
氮是与人类生活密切相关的一种重要元素。根据要求回答:
(1)写出N2的电子式_________;将空气中的氮气转化为含氮化合物的过程称为固氮,当今大规模人工固氮的主要方法是(用化学方程式表示)______________________________。
(2)某无色混合气体中可能含有NH3、O2、H2、NO、HCl等气体,将它通过浓H2SO4 后发现气体体积减少,将剩余气体与空气接触后呈红棕色,此混合气中一定不含有_________。
(3)实验室有多种制取氨气的方法,其中加热消石灰与氯化铵的混合固体就是方法之一。
①写出此反应的化学方程式:_____________________________________________。
②氨气可使湿润的红色石蕊试纸变蓝的原因(用相应的方程式说明)_______________。
③用乙装置(见图)吸收一段时间氨气后,再通入空气,同时将加热的铂丝插入乙装置的锥形瓶内,锥形瓶中不可能生成的物质是___(选填序号)。
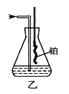
a H2 b NO2 c HNO3 d NH4NO3
写出乙装置中氨催化氧化的化学方程式:__________________________。
(4)已知3Cl2+2NH3==N2 + 6HCl,若NH3过量则还有反应:NH3+ HCl== NH4Cl 。常温常压下,若在一密闭容器中将15mLCl2和40mL NH3充分混合反应后,剩余气体的体积为____mL。
-
化学与人类生活密切相关。请按要求,回答下列问题:
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:______________。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:________。
(3)工业上制漂白粉的化学方程式为____________,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是_________。
(4)KAl(SO4)2·12H2O因其溶于水生成_____(化学式)可以吸附杂质,从而达到净水作用。
-
化学物质及其变化与人类生产、生活密切相关,请填写下列空格:
(1)现有水、氮气、氧气、铁四中物质,其中:(填写化学式)
①可供给人类呼吸的是______.
②可作溶剂,对生命活动具有重要作用的是______.
③可用于食品防腐的是______.④应用最广泛的金属是______.
(2)用化学方程式表示:
①水在通电作用下的反应:_______②细铁丝在氧气中燃烧的反应:______.
③实验室制取二氧化碳的反应:______.
-
化学与人类生活密切相关。请按要求,回答下列问题:
(1)宇航员常用过氧化钠作供氧剂,写出对应反应的化学方程__、__。
(2)新制氯水在阳光照射下容易分解产生无色气体,该反应的化学方程式是__。
工业上将氯气通入冷的消石灰制成漂白粉,写出该反应的化学方程式并用双线桥法表示电子转移的方向和数目的__。
(3)KAl(SO4)2·12H2O因其溶于水生成__(化学式)胶体可以吸附杂质,从而达到净水的目的。
(4)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是__,当反应中有1molK2FeO4生成时,消耗的Cl2在标准状况下的体积为__L,转移电子的数目为__。
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是__,当反应中有1molK2FeO4生成时,消耗的Cl2在标准状况下的体积为__L,转移电子的数目为__。
-
化学与人类生活密切相关。请按要求,回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH  2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____,当反应中有1mol K2FeO4生成时,消耗Cl2在标况下的体积为_________ L,转移电子的数目为_____。
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____,当反应中有1mol K2FeO4生成时,消耗Cl2在标况下的体积为_________ L,转移电子的数目为_____。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:_____________________________________________。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:___________。
(4)工业上制漂白粉的化学方程式为_______________________________,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是______。
(5)KA1(SO4)2•12H2O因其溶于水生成_____(化学式)可以吸附杂质,从而达到净水作用。
(6)硅钢具有很高的_____,主要用作变压器的铁芯;硅酸钠水溶液的俗名为______,可作为木材________________的原料。
(7)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:________________________________。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
-
化学与人类生活密切相关。请按要求,回答下列问题:
(1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式____,将54.8g Na2CO3和NaHCO3 的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L,另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=____,气体V=____。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为____,若有2mol氯气参与该反应,则此时转移的电子数为____NA。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为____。
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为____。
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为____g(请保留两位小数)。
| 9 | 白球比 | 1.6 | |
| 10 | 乳酸脱氢酶 | 161 | U/L |
| 11 | 磷酸肌酸激酶 | 56 | U/L |
| 12 | 甘油三酯 | 0.52 | mmol/L |
| 13 | 总胆固醇 | 4.27 | mmol/L |
| 14 | 高密度脂蛋白胆固醇 | 1.57 | mmol/L |
| 15 | 低密度脂蛋白胆固醇 | 1.40 | mmol/L |
| 16 | 葡萄糖 | 4.94 | mmol/L |
-
化学与人类生活密切相关。请按要求,回答下列问题:
(1) 春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式__________,将54.8g Na2CO3和NaHCO3的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L,另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=__,气体V=___。
(2)“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______,若有2mol氯气参与该反应,则此时转移的电子数为___NA。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为______。
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为_______。
-
化学与人类生活密切相关。请按要求,回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 + 3Cl2 +10KOH 2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是____________,当反应中有1mol K2FeO4生成时,消耗的Cl2在标况下的体积为____________L,转移电子的数目为____________。
2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是____________,当反应中有1mol K2FeO4生成时,消耗的Cl2在标况下的体积为____________L,转移电子的数目为____________。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:_____________________________________________。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_____。
(4)工业上制漂白粉的化学方程式为________________________________,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是_________________________。
(5)KAl(SO4)2·12H2O因其溶于水生成_____(化学式)可以吸附杂质,从而达到净水作用。
(6)硅酸钠水溶液的俗名为__________,可作为木材_______________的原料。
-
化学与人类生活密切相关。请按要求回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 +3Cl2 +10KOH 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____,当反应中有0.5mol K2FeO4生成时,消耗Cl2在标况下的体积为_________,转移电子的数目为_____。
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____,当反应中有0.5mol K2FeO4生成时,消耗Cl2在标况下的体积为_________,转移电子的数目为_____。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式__________。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:___________。
(4)工业上制漂白粉的化学方程式为_______________________________,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是______。
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_____________________。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
-
化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活。
【I】日常生活中使用的各种电池就是利用化学反应将化学能转化为电能,各种各样的电池的发展是化学对人类的一项重大贡献。请回答下列有关化学电源的问题:
(1)下列有关电池的叙述中正确的是___________。
A.锌锰干电池工作一段时间后碳棒变细 B.氢氧燃料电池可将热能直接转变为电能
C.甲烷燃料电池工作时甲烷在负极被氧化 D.太阳能电池的主要材料是高纯度的二氧化硅
(2)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述正确的是
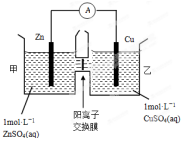
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.甲池中的阳离子向乙池移动,保持溶液中电荷平衡
(3)航天技术上使用的氢一氧燃料电池具有高能、轻便和不污染环境等优点。氢一氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都可表示为2H2+O2=2H2O。酸式氢一氧燃料电池的电解质是酸,放电时其正极的电极反应可表示为__________________,放电一段时间后电解质溶液的pH将_____(填“变大”、“变小”、“不变”)。
【II】自来水厂生产自来水时,需要用到净水剂,对水进行消毒杀菌处理。
(4)漂白粉是常用的一种消毒剂,保存不当容易变质,有关化学方程式为____________。漂白粉不能与家庭中常用的洁厕剂(一种酸性液体,主要含HCl)混合使用,否则容易造成人体中毒,其原因是(用有关的离子方程式表示)____________________。
(5)高铁酸钾(K2FeO4)足一种新型多功能水处理剂。工业上有多种方法制备高铁酸钾,其中一种方法是在氢氧化钾溶液中用次氯酸钠氧化氢氧化铁。该反应的可用离子方程式表示为___________。
(6)用高铁酸钾和锌制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,己知该电池的总反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,则负极的电极反应是______________。

