-
不同温度(T1和T2)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸收热量。下列说法正确的是( )
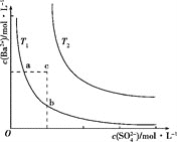
A. T1>T2
B. 加入BaCl2固体,可使a点变成c点
C. c点时,在T1、T2两个温度下均有固体析出
D. a点和b点的Ksp相等
难度: 困难查看答案及解析
-
用CuSO4·5H2O配制0.1 mol/L CuSO4水溶液,下面所列的方法正确的是( )
A. 取25 g CuSO4·5H2O溶于1 L水中
B. 将CuSO4·5H2O干燥去掉结晶水,取16 g溶于水制成1 L溶液
C. 将25 g CuSO4·5H2O溶于水制成1 L溶液
D. 取12.5 g CuSO4·5H2O溶于500 mL水中
难度: 简单查看答案及解析
-
下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项
离子组
加入试剂
加入试剂后发生反应的离子方程式
A
Na+、H+、Cl-、NO3-
铜
3Cu+2NO3-+8H+=3 Cu2++2NO↑+4H2O
B
Fe3+、ClO-、I-
氢氧化钠溶液
Fe3++3OH-= Fe(OH)3↓
C
Ba2+、HCO32-、Cl-
氢氧化钠溶液
HCO32-+ OH-=CO32-+H2O
D
Al3+、Cl-、SO42-
过量氢氧化钠
Al3++3OH-= Al(OH)3↓
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 蔗糖、淀粉、油脂及其水解产物均为非电解质
B. 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
C. 用新制Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖
D. 分子
所有碳原子一定不能共平面
难度: 简单查看答案及解析
-
下图是合成香料香豆素过程的中间产物,关于该物质的说法不正确的是( )
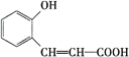
A. 分子式为C9H8O3
B. 有两种含氧官能团
C. 1 mol该物质最多能与5 mol H2发生加成反应
D. 该物质在一定条件下可发生酯化反应
难度: 中等查看答案及解析
-
下列叙述中正确的有( )
①NH4I的电子式:
 ②8个中子的碳原子的核素符号:146C③碘酒、淀粉、水雾、纳米材料均为胶体④烧碱、冰醋酸、氯仿、胆矾均为电解质 ⑤用托盘天平称取8.75g食盐⑥用酸式滴定管量取23.22mL高锰酸钾溶液 ⑦C60、C70、金刚石、石墨均为碳的同素异形体⑧X射线、质谱、核磁共振属于现代化学对物质结构进行研究的手段
②8个中子的碳原子的核素符号:146C③碘酒、淀粉、水雾、纳米材料均为胶体④烧碱、冰醋酸、氯仿、胆矾均为电解质 ⑤用托盘天平称取8.75g食盐⑥用酸式滴定管量取23.22mL高锰酸钾溶液 ⑦C60、C70、金刚石、石墨均为碳的同素异形体⑧X射线、质谱、核磁共振属于现代化学对物质结构进行研究的手段A. ②③④⑥⑦⑧ B. ①③④⑥⑦ C. ②⑥⑦⑧ D. ②⑦⑧
难度: 中等查看答案及解析
-
下列说法错误的是( )
A. 如果某化合物只含共价键,则其一定是共价化合物
B. 焓变小于0而熵变大于0的反应肯定是自发反应
C. 对于给定条件下反应物之间同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比率
D. 绿色化学的核心是利用化学原理对产生的环境污染进行治理
难度: 简单查看答案及解析


 )
)