-
除质量分数以外,人们有时也用体积分数来表示溶液的浓度.例如,52%的饮用白酒就是指每100体积的饮用白酒中含有52体积的乙醇.下列溶液的浓度属于用体积分数来表示的是( )
A.0.9%的生理盐水 B.5%的葡萄糖注射液
C.10%的氢氧化钠溶液 D.75%的医用酒精
难度: 中等查看答案及解析
-
甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
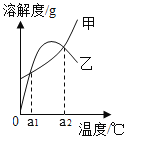
A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液
B.乙的溶解度随温度的升高而增大
C.相同温度时,甲的溶解度一定大于乙的溶解度
D.分别将甲、乙的饱和溶液从a2℃将至a1℃时,所得溶液中溶质的质量分数相等
难度: 中等查看答案及解析
-
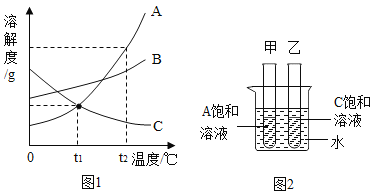
硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是
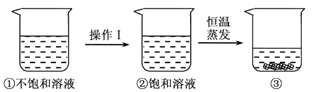
A. 操作I一定是降温 B. 操作I一定是加溶质
C. ①与③的溶质质量一定相等 D. ②与③的溶质质量分数一定相等
难度: 简单查看答案及解析
-
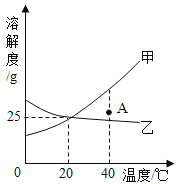
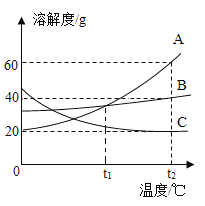
下图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
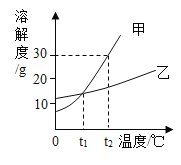
A.甲的溶解度受温度的影响比乙小
B.t1 ℃时,甲、乙溶解度相等
C.t2 ℃时,甲的饱和溶液的溶质质量分数等于30%
D.可采用降低温度的方法使乙的饱和溶液变为不饱和溶液
难度: 中等查看答案及解析
-
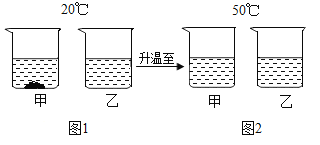
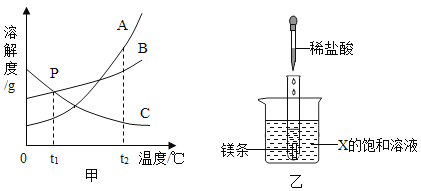
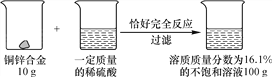
两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图所示,结合图二判断下列说法正确的是
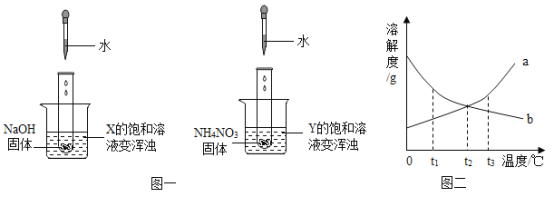
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2 ℃降温到t1 ℃,溶质的质量分数变大
D.t3 ℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
难度: 困难查看答案及解析
-
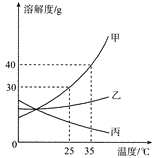
如图是甲、乙、两三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是
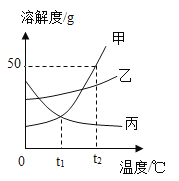
A.甲和丙的溶解度相等
B.在t2℃时,将28g甲物质加入到50g水中,充分溶解后所得溶液的质 量为78g
C.将t2℃时,甲的饱和溶液降温到t1℃,有晶体析出
D.将t1℃时,甲、乙、丙三种物质的饱和溶液升温至t2℃(不考虑水的蒸发),所得溶液中溶质的质量分数由大到小的顺序是甲> Z>丙
难度: 中等查看答案及解析
-
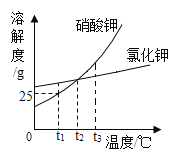
如图是KNO3和NaCl在水中的溶解度曲线,下列说法正确的是( )
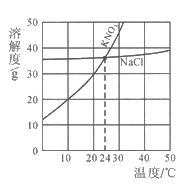
A.20℃时,KNO3的溶解度是30 B.KNO3的溶解度大于NaCl的溶解度
C.当KNO3中含有少量NaCl时,可以通过冷却热饱和溶液的方法提纯KNO3 D.将30℃时KNO3的饱和溶液和NaCl的饱和溶液同时降温至24℃,此时所得溶液中NaCl的质量分数大于KNO3的质量分数
难度: 困难查看答案及解析
-
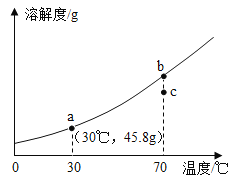
溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示,下列说法不正确的是( )
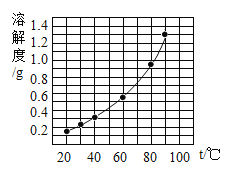
A.升高温度溴酸银的溶解度增大
B.40 ℃时溴酸银易溶于水
C.90 ℃时溴酸银溶液的溶质质量分数一定小于1.3%
D.溴酸银可用降温结晶的方法从溶液中析出
难度: 中等查看答案及解析
-
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是
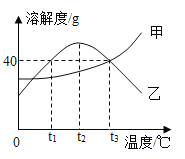
A. t1 ℃时,甲的溶解度大于乙的溶解度
B. t2 ℃时,乙的饱和溶液升温或降温均会析出晶体
C. 乙溶液从t3 ℃降温到t1 ℃,乙溶液中的溶质质量分数会发生改变
D. t3 ℃时,50 g水中加入40 g的甲物质充分溶解可得到90 g甲的饱和溶液
难度: 中等查看答案及解析
-
A、B两种物质的溶解度曲线如右图所示,下列说法错误的是
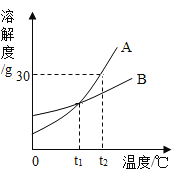
A.在t2℃时A的溶解度大于B的溶解度
B.A、B两种物质的溶解度都随温度升高而增大
C.t1℃时,A、B两种物质的饱和溶液中,溶质质量分数相等
D.t2℃时,A的饱和溶液中溶质质量分数为30%
难度: 中等查看答案及解析
-
甲、乙两种固体物质的溶解度曲线如下图所示,下列说法正确的是( )
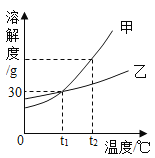
A.甲物质的溶解度大于乙物质的溶解度
B.两种物质的溶解度都随着温度的升高而增大
C.t1 ℃时,60 g甲加入100 g水中,充分溶解,得到160 g溶液
D.甲、乙的饱和溶液从t2 ℃降温到t1 ℃,析出晶体的质量:甲一定大于乙
难度: 中等查看答案及解析