-
准确量取25.00 mL酸性高锰酸钾溶液,可选用的仪器是( )
A.500 mL量筒 B.10 mL量筒
C.50 mL酸式滴定管 D.50 mL碱式滴定管
难度: 简单查看答案及解析
-
25 ℃时,在0.01 mol·L-1的硫酸溶液中,水电离出的H+浓度是 ( )
A.5×10-13 mol·L-1 B.0.02 mol·L-1
C.1×10-7 mol·L-1 D.1×10-12 mol·L-1
难度: 中等查看答案及解析
-
某反应:A
B + C 在室温下不能自发进行,在高温下能自发进行,对该反应过程△H、△S的判断正确的是( )
A.△H<0、△S<0 B.△H>0、△S<0
C.△H<0、△S>0 D.△H>0、△S>0
难度: 中等查看答案及解析
-
下列有关滴定操作的顺序正确的是( )
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液
③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④ B.③⑤①②④ C.③①⑤②④ D.⑤①③②④
难度: 中等查看答案及解析
-
重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有1个电子 B.1H与D互称同位素
C.H2O与D2O互称同素异形体 D.1H218O与D216O的相对分子质量相同
难度: 中等查看答案及解析
-
把0.05molNaOH固体分别加入到下列100ml液体中,溶液的导电性基本不变,该液体是( )
A.自来水 B.0.5mol·盐酸 C.0.5mol·醋酸 D.0.5mol·氯水
难度: 中等查看答案及解析
-
已知0.1 mol•L-1的醋酸溶液中存在电离平衡:CH3COOH
CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
A. 加少量烧碱溶液 B. 加醋酸钠 C. 加少量冰醋酸 D. 加水
难度: 中等查看答案及解析
-
在密闭容器中进行反应X2(g)+Y2(g)
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A.Z为0.2 mol·L-1 B.Y2为0.35 mol·L-1
C.X2为0.3 mol·L-1 D.Z为0.4 mol·L-1
难度: 中等查看答案及解析
-
在25℃的条件下,将体积都为10 mL,pH都等于3的醋酸和盐酸,加水稀释到a mL和b mL,测得稀释后溶液的pH均为5,则稀释时加入水的体积
A.a=b=10 mL B.a=b>10 mL
C.a<b D.a>b
难度: 中等查看答案及解析
-
下列各组物质中化学键的类型相同的是( )
A.HCl MgCl2 NH4Cl B.H2O Na2O CO2
C.CaCl2 NaOH H2S D. NH3 H2O CO2
难度: 简单查看答案及解析
-
下图是元素周期表的一部分,下列说法正确的是( )
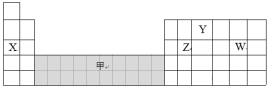
A.可在灰色区域“甲”中寻找催化剂 B.离子半径:W-﹥X+﹥Y3-
C.气态氢化物的稳定性:Z﹥W D.工业上电解X和W化合物的水溶液制备X
难度: 中等查看答案及解析
-
可逆反应:2NO2
2NO+O2 在密闭容器中反应,达到平衡状态的标志是:( )
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2 的同时,生成2n mol NO
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
A. ①④⑥ B.②③⑤ C.①③④ D. ①②③④⑤⑥
难度: 中等查看答案及解析
-
下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强 ④Cl2能与H2S反应生成S ⑤Cl原子最外层有7个电子,S原子最外层有6个电子 ⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS。
A.②⑤ B.①② C.①②④ D.①③⑤
难度: 中等查看答案及解析
-
已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO4•5H2O(s) === CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol1则Q1、Q2的关系为 ( )
A.Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
难度: 中等查看答案及解析
-
已知
(1)H2O(g) == H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g) == CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) == 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1
(Q1、Q2、Q3均大于0)若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ) ( )
A.Q1+Q2+Q3 B. 0.5 Q3-Q2+2Q1 C. 0.5 Q3+ Q2-2Q1 D. 0.5(Q1+Q2+Q3)
难度: 中等查看答案及解析
-
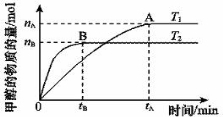
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下图转化关系。下列有关物质的推断正确的是( )
A.若甲为焦炭,则丁可能是O2 B.若甲为Fe,则丁可能是Cl2
C.若甲为AlCl3,则丁可能是NH3 D.若甲为NaHCO3,则丁可能是HCl
难度: 中等查看答案及解析
-
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
A.Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同
B.SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强
C.H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO
D.根据常温下铜与浓硝酸可以制取NO2,推出常温下铁与浓硝酸也可以制取NO2
难度: 中等查看答案及解析
-
下列热化学方程式正确的是 ( )
A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)
2NH3(g) ΔH=-38.6 kJ·mol-1
C.已知在101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为
H2(g)+
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
D.25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为
H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
难度: 中等查看答案及解析
-
下列叙述及解释正确的是 ( )
A.2NO2(g)(红棕色)
N2O4(g)(无色) ΔH<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅
B.对于N2(g)+3H2(g)
2NH3(g),平衡后,保持压强不变,充入Ar,平衡左移
C.FeCl3+3KSCN
Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl固体,因为平衡向逆反应方向移动,故体系颜色变浅
D.H2(g)+I2(g)
2HI(g) ΔH<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变
难度: 中等查看答案及解析
-
右图表示温度、压强对达平衡的可逆反应:2L(g)
2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
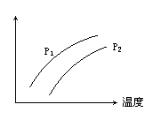
A.混合物中L的百分含量 B.混合气体的密度
C.L的转化率 D.混合气体的平均分子量
难度: 中等查看答案及解析
-
在t℃下,某反应达到平衡,平衡常数K=
。恒容时,温度升高,NO浓度减小。下列说法正确的是 ( )
A.该反应的焓变为正值
B.K表达式中,C(SO3)指反应在该条件下达到化学平衡时SO3的物质的量浓度
C.升高温度,逆反应速率减小
D.该反应化学方程式为:NO+SO3
NO2+SO2
难度: 中等查看答案及解析
-
常温下,将0.1 mol·L-1盐酸溶液与0.06 mol·L-1氢氧化钡溶液等体积混合,该混合溶液的pH等于( )
A.1.7 B.2.0 C.12.0 D.12.4
难度: 中等查看答案及解析
-
下列各组离子在溶液中一定能大量共存的是( )
A.pH=0的溶液中:ClO-、Cu2+、SO
、K+
B.使pH试纸变红色的溶液中:Fe2+、I-、NO3-、Cl-
C.能够和金属镁反应放出气体的溶液中:Na+、H+、SO
、Cl-
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HS-、Ca2+
难度: 困难查看答案及解析
-
常温下,下列各组比值为1∶2的是( )
A.0.1 mol/L与0.2 mol/L醋酸溶液,c(H+)之比
B.0.1 mol/L H2S溶液,c(S2-)与c(H+)之比
C.pH=10的Ba(OH)2溶液与pH=10的氨水,溶质的物质的量浓度之比
D.pH=3的硫酸与pH=3的醋酸溶液,c(SO42-)与c(CH3COO-)之比
难度: 中等查看答案及解析
-
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是( )
A.R的原子半径比Z的大
B.R的氢化物的热稳定性比W的强
C.X与Y形成的化合物只有一种
D.Y的最高价氧化物的水化物的酸性比W的强
难度: 中等查看答案及解析