-
分子数相等的 O2和 O3具有相同的( )
A. 质量 B. 物质的量 C. 摩尔质量 D. 原子总数
难度: 简单查看答案及解析
-
酸和碱的组成中都一定含有的元素是
A.金属元素 B.氧元素 C.氮元素 D.氢元素
难度: 简单查看答案及解析
-
下列变化或操作一定发生化学变化的是( )
A.粗盐提纯 B.酸溶液或碱溶液使指示剂变色 C.敞口放置浓盐酸 D.配制生理盐水
难度: 简单查看答案及解析
-
下列物质中与硝酸钾、硫酸铜可归为同一类别的是( )
A.生石灰 B.食盐 C.冰水 D.烧碱
难度: 简单查看答案及解析
-
能鉴别氢氧化钠和氢氧化钙溶液的试剂是( )
A.盐酸 B.氯化铁溶液 C.二氧化碳 D.酚酞试液
难度: 简单查看答案及解析
-
物质名称与化学式相符合的是( )
A.熟石灰:CaO B.胆矾:CuSO4•5H2O C.石灰石:Ca(OH)2 D.干冰:H2O
难度: 简单查看答案及解析
-
下列物质中属于纯净物的是( )
A.稀硫酸 B.消毒酒精 C.双氧水 D.矿泉水
难度: 简单查看答案及解析
-
工业酒精中含有甲醇,甲醇的化学式为 CH3OH,那么甲醇的摩尔质量为( )
A.32 B.32g C.32g/mol D.32mol
难度: 简单查看答案及解析
-
医生给病人输液时常用葡萄糖注射液。有关葡萄糖(C6H12O6)的正确说法是( )
A.葡萄糖是氧化物 B.葡萄糖由碳、氢、氧三种元素组成
C.葡萄糖各元素的质量比为 1:2:1 D.1mol 葡萄糖分子里含有 12 个氢原子
难度: 简单查看答案及解析
-
下列做法科学的是( )
A.用氢氧化钙改良酸性土壤 B.用石灰水证明鸡蛋壳的主要成分有碳酸盐
C.服用氢氧化钠治胃病 D.用食盐除去水垢
难度: 中等查看答案及解析
-
除去二氧化碳中的水蒸气,可选用的干燥剂是( )
A.氢氧化钠固体 B.生石灰 C.浓硫酸 D.氧化钠
难度: 简单查看答案及解析
-
试管内有难溶性碱,可用下列哪种物质洗去( )
A.HCl B.NaCl C.H2O D.Cu(OH)2
难度: 简单查看答案及解析
-
下列物质,属于有机酸的是( )
A.胃液中的盐酸 B.汽水中的碳酸 C.蓄电池中的硫酸 D.番茄汁中的乙酸
难度: 简单查看答案及解析
-
不适宜用溶解、过滤方法分离的一组物质是( )
A.碳酸钾、碳酸钙 B.氯化钡、氯化银
C.氢氧化钡、硫酸钡 D.硝酸银、硝酸钡
难度: 简单查看答案及解析
-
下列反应属于中和反应的是( )
A.MgCl2 +2NaOH =2NaCl +Mg(OH) 2↓ B.NaOH + HCl =NaCl + H2O
C.CuO + H2SO4 =CuSO4 +H2O D.CaO+H2O = Ca(OH)2
难度: 简单查看答案及解析
-
如图为某反应的微观示意图,其中不同的球代表不同元素的原子。下列说法正确的是( )
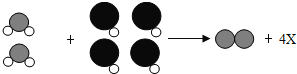
A.该反应属于置换反应 B.各元素化合价在反应前后都未改变
C.反应物分子的个数比为1:1 D.1个X分子中有3个原子
难度: 中等查看答案及解析
-
类推是学习中常用的思维方法,现有以下类推结果,其中错误的是
①碱的水溶液通常呈碱性,所以碱性溶液一定是碱的溶液
②氧化物都含有氧元素,所以含氧元素的化合物一定是氧化物
③酸碱发生中和反应生成盐和水,所以生成水的反应一定是中和反应
A.只有① B.①② C.①③ D.①②③
难度: 中等查看答案及解析
-
实验现象描述正确的是( )
A.红磷燃烧时发出耀眼的白光,产生大量白雾
B.硫酸铜溶液和氢氧化钠溶液混合后会产生蓝色沉淀
C.铁丝在空气中剧烈燃烧、火星四射,放热,生成黑色固体
D.打开盛有浓盐酸的试剂瓶,在瓶口处会看到大量白烟
难度: 简单查看答案及解析
-
将 20℃硝酸钾饱和溶液变为不饱和溶液,可行的方法是
A.降温后过滤,溶液恢复到 20℃ B.蒸发溶剂,过滤,恢复到 20℃
C.溶液中投入少量氯化钠固体 D.倒出一小部分溶液
难度: 中等查看答案及解析
-
某无色混合气体可能由 CH4、H2、CO、CO2 和 H2O 中的某几种气体组成,为确定其成分依次进行了如下实验(假设每一步反应均完全)。①通过澄清石灰水,溶液变浑浊;②通过氢氧化钠固体,质量增加;③在 O2 中点燃,燃烧产物能使白色 CuSO4 粉末变为蓝色。则原混合气体的成份不可能是
A.CO2、H2O、CO B.CO2、H2O、H2
C.CO2、H2O、CH4 D.CO2、CO、CH4
难度: 中等查看答案及解析