-
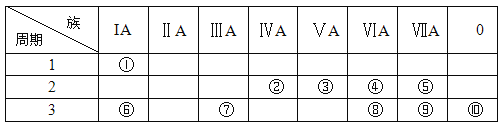
下列关于元素周期表的叙述正确的是( )
A. 有七个主族和八个副族 B. 只有六个周期
C. 零族位于元素周期表第18纵列 D. 第ⅢA族位于元素周期表第3纵列
难度: 简单查看答案及解析
-
下列方法中不能用于实验室制取氨气的是( )
A. 在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
B. 将烧瓶中的浓氨水加热
C. 加热试管中的氯化铵固体
D. 将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
难度: 中等查看答案及解析
-
下列叙述能证明金属A的金属性比金属B强的是( )
A. A原子的最外层电子数比B原子的最外层电子数少
B. A原子的电子层数比B原子的电子层数多
C. 1molA从稀硫酸中置换的氢气比1molB置换的氢气多
D. 常温下,A能从冷水中置换出氢气,而B不能
难度: 中等查看答案及解析
-
下列有关硫酸与硝酸的叙述正确的是( )
A. 浓硫酸具有吸水性,因而能使蔗糖炭化
B. 稀硝酸与活泼金属反应主要放出氢气
C. 可以用铁罐贮运冷的浓硫酸和浓硝酸
D. 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A. 含共价键的化合物一定是共价化合物
B. 含离子键的化合物一定是离子化合物
C. 离子化合物不可能都由非金属元素组成
D. 单质分子中一定含有共价键
难度: 困难查看答案及解析
-
X元素最高氧化物对应的水化物为H2XO4,则它对应的气态氢化物为( )
A. HX B. H2X C. XH4 D. XH3
难度: 中等查看答案及解析
-
下列有关碱金属、卤素结构和性质描述正确的是( )
①随着核电荷数的增加,卤素单质的熔沸点依次升高,密度依次增大
②随着核电荷数的增加,碱金属单质熔沸点依次降低,密度依次减小
③F、Cl、Br、I的最外层电子数都是7,Li、Na、K、Rb最外层电子都是1。
④碱金属单质的金属性很强,均易与氧气发生反应,加热时生成氧化物R2O
⑤根据同族元素性质的递变规律推测At 与H2化合较难,砹化银也难溶于水且具有感光性。
⑥根据F、Cl、Br、I的非金属性递减,可推出HF、HCl、HBr、HI的氧化性及稳定性依次减弱。
⑦卤素按F、Cl、Br、I的顺序其非金属性逐渐减弱的原因是随着核电荷数增加,电子层数增多,原子半径增大起主要作用
A. ①②③⑤ B. ①③④⑦ C. ①③⑤⑦ D. ②④⑤⑦
难度: 中等查看答案及解析
-
下列气体中,不会造成空气污染的是( )
A. N2 B. NO C. NO2 D. SO2
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A. 液氨常用于制冷剂 B. “84”消毒液的主要成分是NaClO
C. Na2O2可用于潜水艇中的供氧剂 D. 常温下,浓硫酸能与Fe剧烈反应放出SO2
难度: 简单查看答案及解析
-
下列物质见光会分解的是( )
A. H2SO4 B. NaCl C. SO2 D. HClO
难度: 简单查看答案及解析
-
氯水中存在多种分子和离子,它们在不同的反应中表现出不同的性质。下列结论正确的是( )
A. 加入有色布条,片刻后有色布条褪色,说明有Cl2存在
B. 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2存在
C. 先加入盐酸酸化,再加入AgNO3溶液,生成白色沉淀,说明有Cl-存在
D. 加入NaOH溶液,氯水的浅黄绿色消失,说明有HClO存在
难度: 中等查看答案及解析
-
某原子的质量数为293,核电荷数为118,其核内中子数和核外电子数分别为( )
A. 118 175 B. 118 118 C. 193 118 D. 175 118
难度: 简单查看答案及解析
-
元素周期表是学习化学的重要工具。如图是元素周期表中的一格,从中获取的信息不正确的是( )
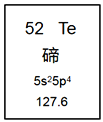
A. 该元素的元素符号为Te
B. 该元素属于金属元素
C. 该元素的原子核外有52个电子
D. 该元素的相对原子质量为127.6
难度: 简单查看答案及解析
-
已知元素的原子序数,可以推断元素原子的( )
①质子数 ②核电荷数 ③核外电子数 ④原子半径
A. ①③ B. ②③ C. ①②③ D. ②③④
难度: 简单查看答案及解析
-
下列各组物质中,化学键类型都相同的是( )
A. HCl与NaOH B. H2S与MgS C. H2O和CO2 D. H2SO4和NaNO3
难度: 中等查看答案及解析
-
下列五种有色溶液与SO2作用均能褪色,其实质相同的是( )
①品红溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液;⑤含I2的淀粉溶液
A. ①④ B. ①②③ C. ②③⑤ D. ③④
难度: 困难查看答案及解析
-
五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误的是( )
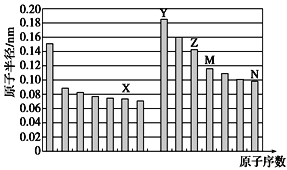
A. 非金属性:X>Z
B. 气态氢化物的稳定性:M<N
C. X和Y形成的化合物只可能含离子键
D. M最高价氧化物对应的水化物是一种弱酸
难度: 困难查看答案及解析
-
如图所示为元素周期表的一部分,下列有关短周期元素X、Y、Z、W的说法中,正确的是( )
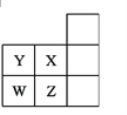
A. 元素X的最低化合价的绝对值与其最高化合价之和为8
B. 最高价氧化物对应的水化物的酸性:H2WO4>HZO4
C. 气态氢化物的稳定性:H2Y>H2W
D. 原子半径:Z>W>Y>X
难度: 中等查看答案及解析
-
下列化学用语或模型图正确的是( )
A. 氨气的结构式:
B. 用电子式表示氯化氢的形成过程为:

C. H2O的比例模型:
D. 14C的原子结构示意图
难度: 中等查看答案及解析
-
将足量的SO2通入BaCl2溶液中,无明显现象,当加入(或通入)某试剂(或气体)X后有沉淀生成.此试剂(或气体)X可能是( )
①NaOH溶液 ②NaCl溶液 ③氨水溶液 ④新制氯水 ⑤H2S ⑥CO2
A. ①②④ B. ①③④⑤ C. ②③⑤⑥ D. ④⑤⑥
难度: 困难查看答案及解析
-
如图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )
A. C元素是非金属性最强的元素
B. A元素最高价氧化物对应的水化物具有强氧化性
C. B元素的氧化物、氢化物的水溶液都呈酸性
D. 三种元素的原子半径的大小顺序是:B>C>A
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是( )
A. 原子半径:W>Z>Y>X
B. X的氢化物于水形成的溶液呈碱性
C. 最简单气态氢化物的热稳定性:Z>W
D. Y元素的最高价氧化物的水化物不与强碱反应
难度: 中等查看答案及解析
-
根据下列实验操作和现象所得出的结论错误的是( )
选项
操作
现象
结论
A
向蔗糖中加入浓硫酸
蔗糖变成疏松多孔的海绵状碳
浓硫酸具有脱水性和强氧化性
B
向盛Na2SiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去
2min后,试管里出现凝胶
非金属性:Cl>Si
C
向盛有铜片的容器中加入浓硝酸
产生大量红棕色气体,溶液变为蓝绿色
浓硝酸具有强氧化性和酸性
D
向澄清石灰水溶液中通入适量气体Y
出现白色沉淀
Y可能是CO2气体
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A. 氯气溶于水:Cl2+H2O═H++Cl- + ClO-
B. Fe溶于足量稀HNO3:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
C. NO2溶于水的反应:3NO2+H2O═2H+ +2NO3- +NO
D. AlCl3溶液中滴入过量稀氨水:Al3++4NH3·H2O = AlO2-+4NH4++2H2O
难度: 中等查看答案及解析
-
现有某稀硫酸和稀硝酸的混合溶液200 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。下列分析或结果正确的是
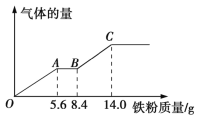
A. 原混合溶液中NO3-的物质的量为0.2 mol
B. OA段产生的是氢气
C. BC段产生NO
D. 原混合溶液中H2SO4的浓度为1.25mol/L
难度: 困难查看答案及解析