-
X、Y、Z、M、N代表五种金属。有以下化学反应:
①水溶液中:X+Y2+=X2++Y
②Z+2H2O(冷)=Z(OH)2+H2↑
③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M-2e-=M2+
④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
A.M<N<Y<X<Z B.N<M<X<Y<Z C.N<M<Y<X<Z D.X<Z<N<M<Y
难度: 简单查看答案及解析
-
下列说法正确的是
A. 任何化学反应不一定都有反应热
B. 使用催化剂可以改变反应的平衡常数
C. 升高温度使反应加快,是因为降低了反应的活化能
D. 对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同
难度: 中等查看答案及解析
-
一定温度下,满足下列条件的溶液一定呈碱性的是( )
A.c(H+)<c(OH-) B.pH=7.2
C.能与金属Al反应放出H2 D.能使广泛pH试纸呈红色
难度: 简单查看答案及解析
-
下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中
 减小
减小B.将CH3COONa溶液从20℃升温至30℃,溶液中
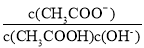 增大
增大C.向盐酸中加入氨水至中性,溶液中
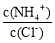 >1
>1D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中
 不变
不变难度: 中等查看答案及解析
-
下列各项实验基本操作中,正确的是
A.在做中和滴定实验时用蒸馏水清洗锥形瓶后,直接开始滴定实验
B.为了加快锌和硫酸反应的速率,可将稀硫酸改为浓硫酸
C.为了加快过滤速度,用玻璃棒搅拌漏斗中的液体
D.蒸干AlCl3溶液制无水AlCl3固体
难度: 中等查看答案及解析
-
下列实验现象或结果不能证明一元酸HR为弱酸的是()
A.室温时,NaR溶液的pH大于7
B.向HR溶液中滴加紫色石蕊试液,溶液变红色
C.向HR溶液中加入少量NaR固体,溶解后溶液的pH变大
D.室温时,0.01mol/L的HR溶液的pH=4
难度: 简单查看答案及解析
-
在容积不变的密闭容器中存在如下反应:2A(g)+B(g)
 3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
A.图I表示增加反应物浓度对该平衡的影响
B.图II表示减小压强对该平衡的影响
C.图Ⅲ表示温度对该平衡的影响,温度:乙>甲
D.图IV表示催化剂对该平衡的影响,催化效率:甲>乙
难度: 简单查看答案及解析
-
下列装置或实验操作正确的是
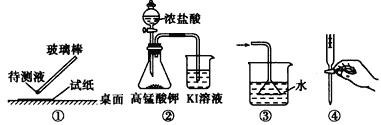
A. ①用pH试纸测某溶液的酸碱性 B. ②探究氧化性:KMnO4>Cl2>I2
C. ③吸收氨气制氨水 D. ④中和滴定实验
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:Fe3+、Ba2+、NO
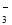 、Cl-
、Cl-B.使酚酞变红色的溶液中:Na+、NH
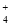 、C1-、SO
、C1-、SO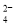
C.c(Al3+)=0.1mol/L的溶液中:K+、Mg2+、SO
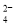 、AlO
、AlO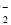
D.由水电离产生的c(H+)=10-13mol/L的溶液中:K+、Na+、CH3COO-、NO
难度: 简单查看答案及解析
-
在恒温恒容的密闭容器中,发生反应X(g)+2Y(g)
 3Z(g) ΔH=-a kJ·molˉ1 (a>0),下列说法正确的是 ( )
3Z(g) ΔH=-a kJ·molˉ1 (a>0),下列说法正确的是 ( )A.容器内气体的压强不再发生变化,说明反应达到平衡状态
B.达到化学平衡状态时,反应放出的总热量可能为 a kJ
C.当反应进行了2min时X的浓度减少了0.1mol/L ,则Z的反应速率为0.15mol·L-1·s-1
D.降低反应温度,正反应速率增大,逆反应速率减小
难度: 中等查看答案及解析
-
对于0.1mol∙L-1Na2SO3溶液,下列表述正确的是
A.升高温度,溶液的pH降低
B.加入少量NaOH固体,c(SO
 )与c(Na+)均增大
)与c(Na+)均增大C.c(Na+)+c(H+)=2c(SO
 )+2c(HSO
)+2c(HSO )+c(OH-)
)+c(OH-)D.c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)难度: 中等查看答案及解析
-
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量2g NaOH
C.用广范pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
难度: 简单查看答案及解析
-
在一定体积的密闭容器中,进行如下化学反应:2X(g)+Y(s)
 Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表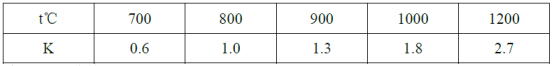
下列叙述不正确的是( )
A.上述反应的正反应是吸热反应
B.该反应的化学平衡常数表达式为K=
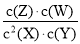
C.若在1L的密闭容器中通入X和Y各1mol,5min后温度升高到800℃,此时测得X为0.33mol,该反应达到平衡状态
D.混合气体的密度保持不变可作为该反应达到平衡的标志之一
难度: 困难查看答案及解析
-
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,工业设备如图所示,下列说法正确的是 ( )
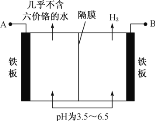
A. A接电源负极
B. 阳极区溶液中发生的氧化还原反应:Cr2O72-+6Fe2++14H+
 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2OC. 阴极区附近溶液pH减小
D. 若不考虑气体的溶解,当收集到H2 13.44 L时(标准状况下),有0.2 mol Cr2O72-被还原
难度: 简单查看答案及解析
-
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn+2MnO2+2H2O==Zn(OH)2+2MnO(OH),下列说法不正确的是
A.电池工作时,锌为负极 B.电池工作时,电解液中的OH- 移向负极
C.电池正极发生还原反应 D.锌的质量减少6.5g时,溶液中通过0.2mol电子
难度: 简单查看答案及解析
-
对下列实验现象或操作解释错误的是
现象或操作
解释
A
KI 淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去
SO2具有还原性
B
配制FeCl2溶液时,先将FeCl2溶于适量稀盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉
抑制Fe2+ 水解, 并防止Fe2+被氧化为Fe3+
C
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成
不能说明该溶液中一定含有SO
D
向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液,生成黑色沉淀
Ksp(CuS) < Ksp(ZnS)
A.A B.B C.C D.D
难度: 简单查看答案及解析

 CO2(g)+H2(g) ΔH=Q kJ·mol―1。已知该反应的平衡常数K与温度t的关系如图所示。若在一固定的密闭容器中,850 ℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
CO2(g)+H2(g) ΔH=Q kJ·mol―1。已知该反应的平衡常数K与温度t的关系如图所示。若在一固定的密闭容器中,850 ℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表: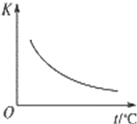
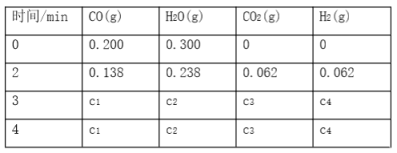
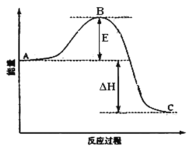
 2ClNO(g)。
2ClNO(g)。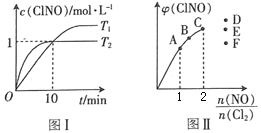
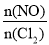 的变化如图II,则A、B、C三个状态中,NO的转化率最小的是____点,当
的变化如图II,则A、B、C三个状态中,NO的转化率最小的是____点,当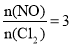 时,达到平衡状态时ClNO的体积分数φ可能是D、E、F三点中的_____点。
时,达到平衡状态时ClNO的体积分数φ可能是D、E、F三点中的_____点。