-
关于物质燃烧的现象描述错误的是
A. 磷在空气中燃烧,反应剧烈,产生大量白雾
B. 铁丝在氧气中燃烧,火星四射,生成黑色固体
C. 镁带在空气中燃烧,发出耀眼的白光,生成白色固体
D. 硫在氧气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体
难度: 中等查看答案及解析
-
空气是人类的宝贵资源,下列有关空气的说法错误的是( )
A. 空气的成分按体积计算,含量最多的气体是氮气 B. 空气是混合物
C. 氧气具有可燃性 D. 稀有气体的化学性质不活泼
难度: 简单查看答案及解析
-
对于下列几种化学符号,有关说法正确的是
①H ②Fe2+③Cu ④P2O5⑤Fe3+⑥NaCl
A.能表示一个分子的是①④⑥
B.表示物质组成的化学式是③④⑥
C.②⑤的质子数相同,化学性质也相同
D.④中的数字“5”表示五氧化二磷中有5个氧原子
难度: 中等查看答案及解析
-
一定条件下,一个密闭容器内发生反应,测得反应前后各物质的质量如下表所示.下列有关说法不正确的是( )
物质
A
B
C
D
反应前的质量(g)
15
15
25
20
反应后的质量(g)
0
10
x
y
A.x的取值范围是:0≤X≤45 B.参加反应的A和B的质量之比为3:1
C.当y≤20时,该反应为化合反应 D.x+y=65
难度: 困难查看答案及解析
-
下列说法涉及到化学变化的是
A. 酒香不怕巷子深 B. 野火烧不尽,春风吹又生
C. 泥菩萨过河,自身难保 D. 只要功夫深,铁杵磨成针
难度: 简单查看答案及解析
-
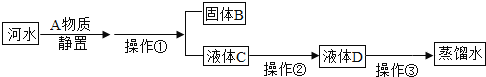
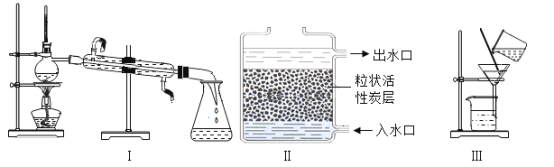
水是生命之源,下列关于水的说法正确的是( )
A.工业废水需要处理达标后才能排放
B.明矾可以使硬水转化为软水
C.蒸馏海水和电解水的过程中水发生的都是物理变化
D.蒸馏水、自来水都是纯净物
难度: 中等查看答案及解析
-
下列实验操作错误的是
A.
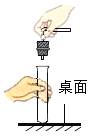 B.
B.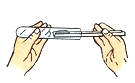 C.
C.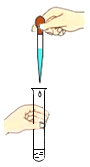 D.
D.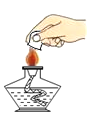
难度: 简单查看答案及解析
-
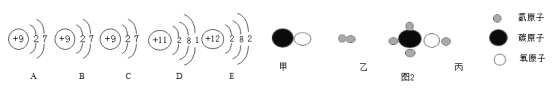
下图为元素周期表的一部分(X元素信息不全)。下列说法正确的是
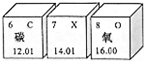
A.碳的化学性质活泼
B.X表示N2
C.氧原子的质子数是8
D.三种元素原子的核外电子数相同
难度: 中等查看答案及解析
-
碳可以与浓硫酸在加热的条件下发生如下反应:
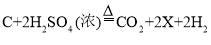 其中X的化学式为( )
其中X的化学式为( )A.O2 B.SO2 C.SO2 D.H2S
难度: 中等查看答案及解析
-
硝酸铵(NH4NO3)是常用的一种氮肥,NH4NO3中含有NO3-,则NO3-中氮元素的化合价为( )
A.+2 B.+3 C.+4 D.+5
难度: 简单查看答案及解析
-
核电荷数多于核外电子数的粒子一定是( )
A.分子 B.原子 C.阴离子 D.阳离子
难度: 简单查看答案及解析
-
下列对分子、原子、离子的认识,不正确的是( )
A.分子、原子、离子都能构成物质
B.气体压缩为液体,分子体积变小
C.温度越高,分子运动越快
D.钠原子和钠离子的化学性质不同
难度: 简单查看答案及解析
-
水在实验中起着重要的作用,下列实验中,水用来隔绝空气的是( )
A.
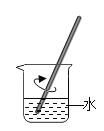 溶解物质 B.
溶解物质 B.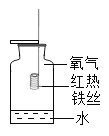 铁丝燃烧
铁丝燃烧C.
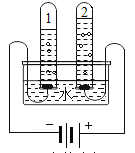 水的电解 D.
水的电解 D.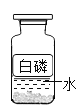 保存白磷
保存白磷难度: 中等查看答案及解析
-
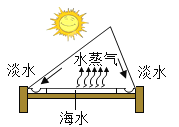
如图所示:甲瓶中盛放的是浓H2SO4,乙瓶中放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花不变色;若关闭阀门Ⅱ,打开阀门Ⅰ,紫色小花()
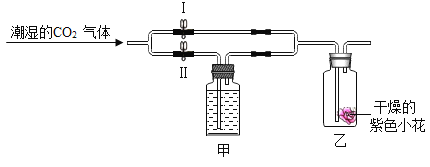
A.变红色 B.变蓝色 C.变白色 D.不变色
难度: 简单查看答案及解析
-
用CO2和NH3合成尿素[CO(NH2)2]是固定和利用CO2的成功范例,其反应的化学方程式为:CO2+2NH3═CO(NH2)2+H2O。下列说法正确的是( )
A.尿素中有2个氮原子
B.尿素的相对分子质量是60g
C.参加反应的CO2与NH3的质量比是44:17
D.该反应是充分利用CO2的一种有效途径
难度: 中等查看答案及解析
-
微粒是构成化学物质的基础,下列对微粒的描述正确的是( )
A.仅有碳原子构成的物质属于纯净物
B.原子中一定含有质子、中子、电子
C.NaCl是由离子构成的,所以HCl也是有离子构成的
D.Cl-的离子结构示意图为
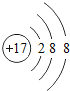
难度: 中等查看答案及解析
-
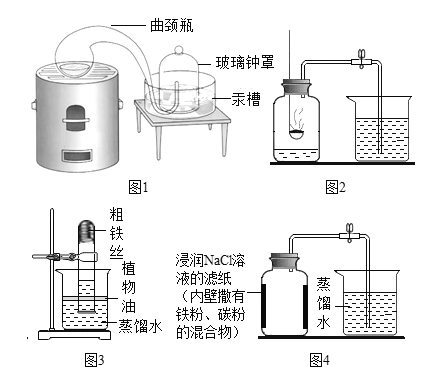
某化学兴趣小组的同学在老师的指导下,正确完成如下图所示两个实验。已知所用实验装置气密性良好。
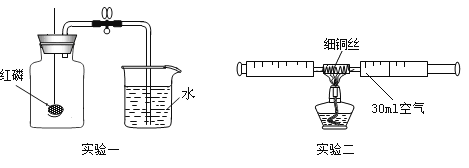
关于该实验,有如下说法:①红磷熄灭并冷却后才能打开弹簧夹;②点燃酒精灯加入铜丝,可观察到铜丝有红色变成黑色;③停止加热后即可读出注射器内气体的体积约为24mL;④实验取用铜丝质量的多少不会影响实验结果;⑤两个实验均能证明空气是混合物;⑥两个实验均能证明空气中约含1/5体积的氧气。其中正确说法的个数有( )
A. 2个 B. 3个 C. 4个 D. 5个
难度: 中等查看答案及解析
-
豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2),关于亮氨酸的说法正确的是( )
A. 亮氨酸是氧化物
B. 亮氨酸中碳元素的质量分数为27.3%
C. 一个亮氨酸分子由22个原子构成
D. 亮氨酸中碳、氢、氮、氧四种元素的质量比为6:13:1:2
难度: 中等查看答案及解析
-
已知:
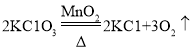 ,如图表示一定质量的
,如图表示一定质量的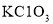 和
和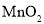 固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )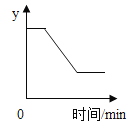
A.固体中氧元素的质量 B.生成O2的质量
C.固体中
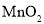 的质量 D.固体中钾元素的质量
的质量 D.固体中钾元素的质量难度: 中等查看答案及解析
-
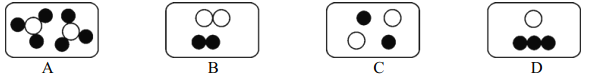
某化学反应的微观示意图如下图所示,(不同小球代表不同的原子),下列说法中不正确的是
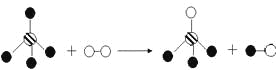
A. 在此图示变化中共有四种物质
B. 该图示变化中的分子没有变化
C. 原子是化学反应中的最小粒子
D. 反应前后物质的质量总和不变
难度: 中等查看答案及解析
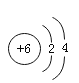 和
和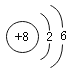 两种原子中相等的是_____(填序号)。
两种原子中相等的是_____(填序号)。