-
下列化学用语正确的是( )
A.
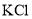 的电子式:
的电子式: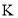
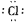 B.
B.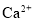 的结构示意图:
的结构示意图: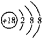
C.纯碱的化学式:
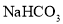 D.
D.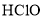 的结构式:
的结构式:
难度: 简单查看答案及解析
-
能量通常包括热能、电能、光能、机械能、化学能等,下列有关能量转化关系的判断错误的是( )
A.甲烷燃烧:化学能转化为热能和光能
B.植物进行光合作用:太阳能转化为化学能
C.二次电池放电:电能转化为化学能
D.风力发电:风能转化为机械能,机械能转化为电能
难度: 中等查看答案及解析
-
1940年科学家用a粒子轰击
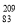 Bi发现了元素At,其反应为
Bi发现了元素At,其反应为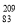 Bi +
Bi +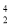 He→
He→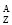 At+2
At+2 n,则At的中子数为( )
n,则At的中子数为( )A.85 B.126 C.127 D.211
难度: 简单查看答案及解析
-
下列反应中符合图中所示能量转化关系的是( )
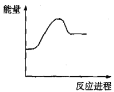
A.
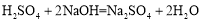
B.
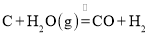
C.
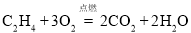
D.
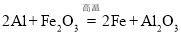
难度: 中等查看答案及解析
-
下列说法错误的是( )
A.石油裂解气能使酸性高锰酸钾溶液褪色 B.石油的分馏、催化裂化都是化学变化
C.裂化汽油不能用来萃取溴水中的溴 D.煤油馏分的沸点范围低于重油馏分的沸点范围
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.第Ⅰ
 族和Ⅶ
族和Ⅶ 族元素形成的化合物均含离子键
族元素形成的化合物均含离子键B.在反应
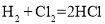 中,断裂
中,断裂 —
— 、
、 —
— 键吸收的能量大于形成
键吸收的能量大于形成 —
— 键释放的能量
键释放的能量C.乙烯、苯乙烯均能发生加聚反应,二者互为同系物
D.从海带中提取碘的过程中,可以利用
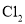 或
或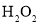 将
将 氧化成
氧化成
难度: 中等查看答案及解析
-
设
 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )A.标准状况下,
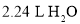 中所含共用电子对数为
中所含共用电子对数为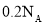
B.
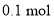 甲苯中含有的碳碳双键数为
甲苯中含有的碳碳双键数为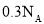
C.
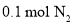 与
与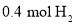 在一定条件下充分反应,生成
在一定条件下充分反应,生成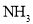 分子的数目为
分子的数目为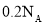
D.由
 、
、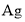 、足量
、足量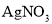 溶液形成的原电池中,当正极增重
溶液形成的原电池中,当正极增重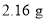 时,电路中通过的电子数为
时,电路中通过的电子数为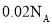
难度: 中等查看答案及解析
-
下列实验操作能达到相应实验目的的是( )
实验操作
实验目的
A
向少量溴的四氯化碳溶液中滴加植物油,振荡
检验植物油中含碳碳不饱和键
B
以镁、铝为电极,插入烧碱溶液中构成原电池
证明镁比铝活泼
C
向乙酸乙酯粗产品中加入
 溶液,分液
溶液,分液提纯乙酸乙酯
D
常温下,在浓硫酸、稀硫酸中分别加入铝片
探究浓度对反应速率的影响
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
唐代张九龄诗句“松叶堪为酒,春来酿几多”涉及淀粉、麦芽糖、葡萄糖、乙醇等化学物质,下列有关说法错误的是( )
A.淀粉、乙醇所含元素种类相同
B.蔗糖和麦芽糖、淀粉和纤维素都互为同分异构体
C.麦芽糖、葡萄糖都能被新制的氢氧化铜氧化
D.淀粉、麦芽糖都能发生水解反应,最终生成葡萄糖
难度: 中等查看答案及解析
-
图是五种短周期主族元素在周期表中的相对位置,其中E元素的原子半径在同周期中最小。下列说法正确的是( )
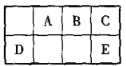
A.原子半径由大到小的顺序是D>A>B
B.由A、B、氢元素形成的化合物一定是共价化合物
C.最高价氧化物对应的水化物的酸性:C>E
D.D的氧化物是碱性氧化物
难度: 简单查看答案及解析
-
相同温度下,将下列四组试剂混合后生成氢气速率最大的是( )
A.
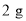 锌片、
锌片、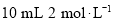 盐酸 B.
盐酸 B.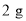 锌粉(另含
锌粉(另含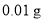 铜片)、
铜片)、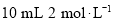 盐酸
盐酸C.
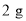 锌粉、
锌粉、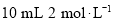 盐酸 D.
盐酸 D.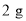 镁粉、
镁粉、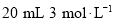 硝酸
硝酸难度: 简单查看答案及解析
-
有机物
 (
( )、
)、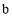 (
(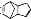 )、
)、 (
(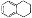 )的分子式均为C10H12,下列说法错误的是( )
)的分子式均为C10H12,下列说法错误的是( )A.b、c两种物质均不属于烷烃
B.b能使酸性高锰酸钾溶液褪色
C.1 mol b、c分别与足量H2发生加成反应时,都是最多消耗3 mol H2
D.a、b、c分子中所有原子不可能共平面
难度: 中等查看答案及解析
-
 、
、 、
、 、
、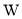 是原子序数依次增大的四种短周期主族元素,
是原子序数依次增大的四种短周期主族元素, 、
、 、
、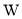 原子最外层电子数之和为20,
原子最外层电子数之和为20, 的单质与冷水反应缓慢,与沸水反应迅速。下列说法中错误的是( )
的单质与冷水反应缓慢,与沸水反应迅速。下列说法中错误的是( )A.简单氢化物稳定性:
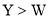 B.最高正价:
B.最高正价:
C.
 可分别与
可分别与 、
、 、
、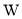 形成二元离子化合物 D.单质沸点:
形成二元离子化合物 D.单质沸点: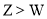
难度: 中等查看答案及解析
-
以石墨、镁为电极材料,以
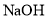 、
、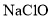 的混合溶液为电解质溶液,将化学反应
的混合溶液为电解质溶液,将化学反应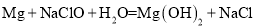 设计成原电池。下列说法错误的是( )
设计成原电池。下列说法错误的是( )A.石墨极上发生还原反应 B.
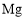 是负极
是负极C.正极反应式为
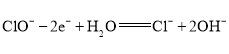 D.消耗
D.消耗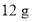 镁理论上有
镁理论上有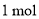 电子通过外电路
电子通过外电路难度: 中等查看答案及解析
-
用
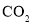 、
、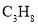 为原料可制备丙烯(
为原料可制备丙烯( ),反应为
),反应为 。一定温度下,向
。一定温度下,向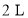 恒容密闭容器中通入
恒容密闭容器中通入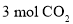 、
、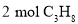 ,测得
,测得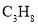 与
与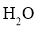 的物质的量随时间的变化关系如下表所示,下列说法错误的是( )
的物质的量随时间的变化关系如下表所示,下列说法错误的是( )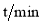
0
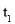
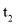

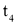
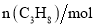
2
1.4
1
0.8
0.8
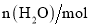
0
0.6
1
1.2
1.2
A.
 时,该反应达到平衡
时,该反应达到平衡B.
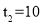 时,0~10
时,0~10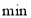 内用
内用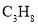 表示的平均反应速率为
表示的平均反应速率为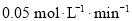
C.当混合气体的平均相对分子质量不变时,该反应达到平衡
D.平衡时与起始时气体的压强之比是

难度: 中等查看答案及解析
-
如图是某种烃的含氧衍生物
 的球棍模型示意图,下列说法正确的是( )
的球棍模型示意图,下列说法正确的是( )
A.
 与其在酸性条件下水解后所得的混合物可用分液的方法进行分离
与其在酸性条件下水解后所得的混合物可用分液的方法进行分离B.
 在碱性条件下水解的产物之一是一种常用的医用消毒剂,其纯净物消毒效果最佳
在碱性条件下水解的产物之一是一种常用的医用消毒剂,其纯净物消毒效果最佳C.
 充分燃烧,消耗
充分燃烧,消耗 氧气
氧气D.
 蒸气与乙烯组成的混合气体中,氧的质量分数为
蒸气与乙烯组成的混合气体中,氧的质量分数为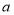 ,则氢的质量分数为
,则氢的质量分数为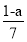
难度: 中等查看答案及解析
 、
、 、
、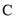 、
、 在周期表中的相对位置如图所示。回答下列问题:
在周期表中的相对位置如图所示。回答下列问题: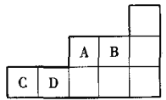
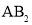 分子中每个原子最外层都达到8电子稳定结构,
分子中每个原子最外层都达到8电子稳定结构,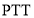 是一种高分子化合物,其一种合成路线如下:
是一种高分子化合物,其一种合成路线如下:
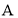 的产量可以用来衡量一个国家的石油化工发展水平,其结构简式为_____。
的产量可以用来衡量一个国家的石油化工发展水平,其结构简式为_____。 的化学名称是_____;
的化学名称是_____;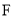 中官能团的名称是______。
中官能团的名称是______。 的反应类型是___;
的反应类型是___;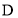 与有机物
与有机物 互为______(填“同系物”“同分异构体”“同位素”或“同素异形体”)。
互为______(填“同系物”“同分异构体”“同位素”或“同素异形体”)。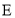 还可以由有机物
还可以由有机物 (
( )在一定条件下发生水解反应得到,写出与
)在一定条件下发生水解反应得到,写出与 的结构简式:___。在
的结构简式:___。在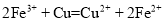 ,图1是根据该反应设计的原电池。甲烷、空气(或氧气)与
,图1是根据该反应设计的原电池。甲烷、空气(或氧气)与 溶液可构成燃料电池,如图2所示。回答下列问题:
溶液可构成燃料电池,如图2所示。回答下列问题: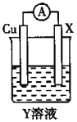

 的成分是_____(填化学式),该原电池始工作时移向正极的离子是______(填离子符号),负极的电极反应式为_________,
的成分是_____(填化学式),该原电池始工作时移向正极的离子是______(填离子符号),负极的电极反应式为_________,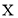 不可能是____(填字母)。
不可能是____(填字母)。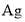 B.
B. C.石墨D.铂
C.石墨D.铂 2SO3(g),反应过程中的能量变化如图1所示,某反应物和生成物的浓度随时间的变化如图2所示。
2SO3(g),反应过程中的能量变化如图1所示,某反应物和生成物的浓度随时间的变化如图2所示。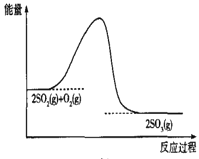
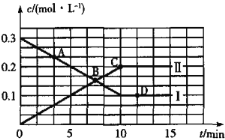
 表示的物质是______(填化学式),从反应开始至反应达到平衡,该物质的化学反应速率为______ mol/(L·min)。
表示的物质是______(填化学式),从反应开始至反应达到平衡,该物质的化学反应速率为______ mol/(L·min)。