-
有关钠的叙述正确的是( )
A. 2.3 g钠与97.7 g水反应后溶液中溶质的质量分数等于4%
B. 钠跟CuSO4溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出了金属铜
C. 将金属钠与水反应后的溶液中通入适量氯气后,溶液中含有两种溶质
D. 钠在空气中的缓慢氧化与其在空气中点燃的产物相同
难度: 中等查看答案及解析
-
将0.195g锌粉加入到20.0mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是
A.M B.M2+ C.M3+ D.MO2+
难度: 中等查看答案及解析
-
下列物质与其用途相符合的是( )
①Cl2-制消毒剂 ②AgBr-制胶卷,感光纸 ③AgI-人工降雨 ④碘-预防甲状腺肿大 ⑤淀粉-检验I2的存在 ⑥NaClO-漂白纺织物
A.②③④⑤⑥ B.①②③④⑤ C.②③④⑤ D.全部
难度: 简单查看答案及解析
-
下列实验方法或操作正确的是
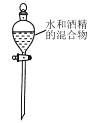
A.分离水和酒精
 B.蒸发NH4Cl溶液得到NH4Cl晶体
B.蒸发NH4Cl溶液得到NH4Cl晶体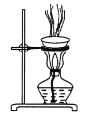
C.配制一定物质的量浓度溶液时转移溶液
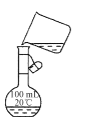 D.除去氯气中的氯化氢
D.除去氯气中的氯化氢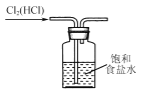
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.18O2与18O2互为同位素 B.18O与16O 是同一种核素
C.原子核都是由质子和中子构成的 D.Na2O2中阳离子和阴离子的个数比为2:1
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下22.4LHF中所含电子数为10NA
B.100mL12mol·L—1盐酸与足量MnO2共热,转移的电子数为0.6NA
C.1mol·L-1Na2CO3溶液中,CO32―的数目小于NA
D.1molCH5+中含有的电子数目为10NA
难度: 简单查看答案及解析
-
在标准状况下,将VL气体A(摩尔质量为Mg/mol),溶于0.1L水中,所得溶液密度为dg/cm3,则该溶液的物质的量浓度为
A.
mol/L B.
mol/L
C.
mol/L D.
mol/L
难度: 简单查看答案及解析
-
下列关于某些离子的检验说法正确的是
A.向某溶液中加稀盐酸,将产生的无色气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定有CO32-或HCO3-
B.向某溶液中加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有SO42-
C.向某溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则原溶液中存在NH4+
D.向某溶液中加入硝酸银溶液产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有Cl-
难度: 中等查看答案及解析
-
核内中子数为N的R2+,质量数为A,则ng它的氧化物(RO)中所含质子的物质的量是( )
A.
(A-N+8) mol B.
(A-N+10)mol
C.(A-N+2)mol D.
(A-N+6)mol
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.金属原子失电子越多,其还原性越强
B.制成0.5L1mol/L的Na2CO3溶液,需要Na2CO3·10H2O晶体质量为143g
C.相同条件下,相同物质的量的O2和N2的密度比等于7:8
D.SO2→SO32-,需要加入适当的氧化剂才能完成
难度: 中等查看答案及解析
-
为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1g 样品加热,其质量变为w2g ,则该样品的纯度(质量分数)是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
已知A是一种金属单质,B为淡黄色固体,其转化关系如图所示,则以下有关C的性质描述错误的是( )
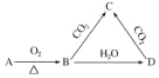
A.C与CO2能继续反应 B.澄清石灰水反应产生白色沉淀
C.与足量盐酸反应放出气体 D.受热易分解
难度: 中等查看答案及解析
-
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应的产物并不改变的是( )
A.Na和O2 B.NaOH和CO2
C.Na2O2和CO2 D.Na2CO3和盐酸
难度: 中等查看答案及解析
-
为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是( )
选项
被陶瓷的物质(杂质)
除杂试剂
分离方法
A
HCl(H2O)
碱石灰
洗气
B
KNO3溶液(KOH)
FeCl3溶液
过滤
C
KNO3固体(NaCl)
用H2O溶解
降温结晶
D
CO2(HCl)
NaOH溶液
洗气
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
以下是以空气、海水中的物质为原料制取纯碱的工业流程:
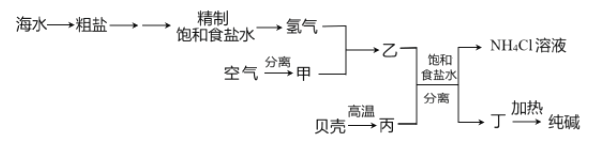
已知粗盐中含有Ca2+、Mg2+、SO42-等杂质离子。下列有关说法不正确的是
A. 除去粗盐中的杂质离子可依次加入NaOH 溶液、BaCl2 溶液、Na2CO3 溶液
B. 甲、丙分别为N2、CO2
C. 分离得到丁和NH4Cl 溶液的操作是过滤
D. 上述流程中物质转化有涉及置换反应
难度: 中等查看答案及解析
-
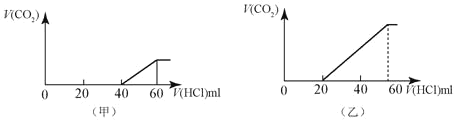
已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3+6HCl=3Cl2+KCl +3H2O,③2KBrO3+Cl2=Br2+ 2KClO3,
下列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KClO3>KBrO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为5∶1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
难度: 中等查看答案及解析
-
水热法制备Fe3O4纳米颗粒的反应为:3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,下列说法中,不正确的是( )
A.x=4
B.每生成1molFe3O4,反应转移的电子总数为3mol
C.1molFe2+被氧化时,被Fe2+还原的O的物质的量为0.25mol
D.可以通过丁达尔效应判断有无Fe3O4纳米颗粒生成
难度: 中等查看答案及解析
-
将定量的Na2CO3和NaHCO3的混合物加热到不再放出气体时,收集到CO2 a L,冷却后向残余物中加入足量盐酸又收集到CO2 2a L (体积均在标准状况下测定)。则混合物中Na2CO3和NaHCO3的物质的量之比为( )
A.1:1 B.1:2 C.1:3 D.1:4
难度: 简单查看答案及解析
-
已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl ②Q+H2O―→X+H2
③Y+NaOH―→G+Q+H2O ④Z+NaOH―→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是
A. G、Y、Q、Z、X B. X、Z、Q、G、Y
C. X、Z、Q、Y、G D. G、Q、Y、Z、X
难度: 中等查看答案及解析
-
已知Cu2O能与硝酸反应,方程式为:3Cu2O+14HNO3═6Cu(NO3)2+2NO↑+7H2O,若生成NO的体积为0.448L(标况下),那下列说法正确的是( )
A.被氧化的Cu2O为1.44g
B.做氧化剂的硝酸为0.14mol
C.至少需0.5moI/L硝酸140mL与Cu2O反应
D.转移的电子总数为0.06NA
难度: 中等查看答案及解析