-
某运动饮料含有下列成分,其中只含有共价键的是
A.C6H12O6 B.Na2CO3 C.MgSO4 D.NaCl
难度: 中等查看答案及解析
-
纳米金(79Au)粒子在遗传免疫等方面有重大的应用前景,下列说法错误的是
A.Au为第六周期元素 B.Au为黑色金属
C.Au的质子数为79 D.纳米金表面积大吸附能力强
难度: 中等查看答案及解析
-
下列化学用语表示错误的是
A.氨分子的电子式:
B.正丁烷的球棍模型:
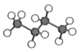
C.乙烯的结构简式:CH2=CH2
D.原子核内有8个中子的碳原子:
难度: 中等查看答案及解析
-
下列说法正确的是
A.18O2和16O2互为同素异形体 B.戊烷和丙烷互为同系物
C.C60和C70互为同位素 D.H2NCH2COOCH3和CH3CH2NO2互为同分异构体
难度: 中等查看答案及解析
-
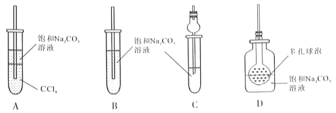
下列除杂方法选用错误的是
物质(括号内为杂质)
除杂方法
A
硝基苯(苯)
蒸馏
B
乙烯(SO2)
NaOH溶液,洗气
C
己烷(己烯)
溴水,分液
D
淀粉溶液(NaCl)
渗析
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
我国著名书画家赵估曾有诗句“用过天晴云破处,干峰碧波色来”描述汝窑青瓷之美。青色主要来自添加的玛瑙粉末.下列有关说法错误的是
A.青瓷的青色来自于玛瑙中的SiO2
B.陶瓷是传统的无机非金属材料
C.瓷器质量与原料矿物组成、升温速度、煅烧时间等因素有关
D.青瓷化学性质稳定,耐酸碱侵蚀
难度: 中等查看答案及解析
-
下列我国合成的材料中,主要成分由同周期两种元素组成的是
A.可实现高温超导的钙钛矿(CaTiO3)薄膜
B.制造大口径高精度非球面反射镜的碳化硅材料
C.大面积单品六方氮化硼半导体材料
D.可淡化海水的石墨烯纳米网
难度: 简单查看答案及解析
-
关于离子化合物NH5,下列说法正确的是
A.N为-5价 B.阳离子的电子数为11
C.阴离子为8电子稳定结构 D.阴阳离子个数比是1:1
难度: 中等查看答案及解析
-
2019年是门捷列夫元素周期表发表150周年.根据元素周期律和元素周期表,下列说错误的是
A.砹(85At)的单质在常温常压下是液体 B.位于第四周期VA族的元素为非金属元素
C.铷(37Rb)元素的最高化合价是+1 D.第七周期0族元素的原子序数为118
难度: 中等查看答案及解析
-
白藜芦醇具有抗衰老作用,其结构如图所示.下列有关说法错误的是
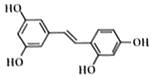
A.分子式为C14H12O4
B.含有羟基与碳碳双键
C.能发生加聚反应
D.一氯代物有4种
难度: 中等查看答案及解析
-
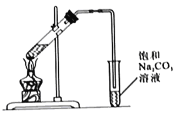
2019年6月17日,屠呦呦团队宜布青蒿素应用取得科研新进展.已知:青蒿素难溶于水、易溶于乙醚.实验室模拟从青蒿中提取青蒿素流程如下图,该提取过程不需要用到的仪器或装置是

A.
 B.
B. C.
C.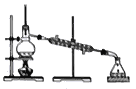 D.
D.
难度: 简单查看答案及解析
-
已知NA是阿伏加德罗常数的值,下列关于铜生锈反应2Cu+O2+H2O+CO2=Cu2(OH)2CO3的说法错误的是
A.消耗32gCu转移的电子数为NA B.1.8g H2O含有的质子数为NA
C.22g CO2的共用电子对数为NA D.标况下,11.2LO2和CO2混合气体中O原子数为NA
难度: 中等查看答案及解析
-
科学家合成一种新化合物:
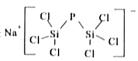 ,下列关于组成该化合物的四种元素的说法正确的是
,下列关于组成该化合物的四种元素的说法正确的是A.原子半径:Cl>P>Na B.含氧酸酸性:Cl>P>Si
C.气态氢化物的稳定性:Cl>Si>P D.单质熔点:Si>Na> Cl
难度: 中等查看答案及解析
-
我国科学家用三元催化剂Mo/P/WOx催化纤维素直接氢解制乙醇,其转化关系如图所示.下列说法错误的是
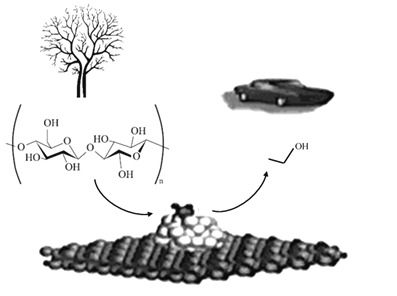
A.纤维素是天然高分子化合物
B.该法实现由纤维素廉价高效制备乙醇
C.一个纤维素分子含有6个羟基
D.纤维素直接氢解制乙醇过程中Mo/P/WOx有参与反应
难度: 中等查看答案及解析
-
主族元素M、X、Y、Z的原子序数依次增加,且均不大于20;M原子的最外层电子数与次外层电子数之和为8;Y、Z是处于不同周期的金属元素;X、Y、Z原子最外层电子数之和为11。下列说法正确的是
A.简单离子半径:Y<M<X
B.Z与M形成的化合物中可能含有共价键
C.X的最高价氧化物对应的水化物在其同族元素中酸性最强
D.常温下,Y和Z的单质均能与水剧烈反应
难度: 中等查看答案及解析
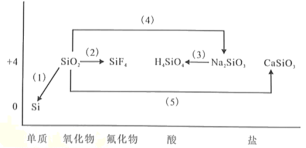
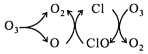
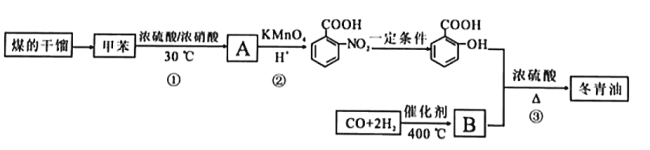
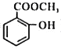 ),合成路线如下:
),合成路线如下: