-
若在宇宙飞船的太空实验室(失重条件下)进行以下实验,其中最难完成的是 ( )
A. 将金粉和铜粉混合 B. 将牛奶加入水中混合
C. 将氯化钠晶体溶于水中 D. 用漏斗、滤纸过滤除去水中的泥沙
难度: 简单查看答案及解析
-
据报道,塑料吸管及其他一次性塑料制品已经对西班牙海洋生态造成严重影响。40%至60%的海龟会吞食塑料废物、一些鸟类的塑料废物吞食率高达93%塑料制品之所以成为海洋生物的杀手,主要是因为 ( )
A.塑料制品中含有有毒物质
B.大部分塑料制品的降解需要几十甚至几百年
C.塑料制品会漂浮在海洋表面
D.海洋生物会误食塑料制品,且无法消化
难度: 简单查看答案及解析
-
下列关于“不一定”的说法中不正确的是 ( )
A.含氧化合物不一定是氧化物 B.由同种元素组成的纯净物不一定是单质
C.纯净物不一定由同种分子构成 D.能分解出氧气的化合物不一定是氧化物
难度: 简单查看答案及解析
-
把打磨过的镁条放入CuSO4溶液中,镁条表面覆盖了红色物质,一会儿又有大量气泡冒出。同学们对“放出气体”这一异常现象进行猜想、实验。其中没有价值的是
A.小宇推测气体是氢气并检验 B.小琪猜想CuSO4溶液呈酸性并测定
C.小寒认为气体是二氧化碳并检验 D.小梁认为试剂变质,更换后再做
难度: 困难查看答案及解析
-
为除去样品中杂质(括号中为杂质),选用的试剂及操作均正确的一组是 ( )
样品组成
选用的试剂
选用的操作
A
NaCl(Na2SO4)
Ba(NO3)2
过滤
B
MnO2(KCl)
H2O
过滤
C
K2CO3(KCl)
HCl
搅拌
D
CO2(CO)
O2
点燃
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
钠是一种银白色固体,放置在空气中会迅速与氧气反应生成氧化钠,把钠投入水中,与水剧烈反应,熔化成闪亮小球在水面上游动,生成了氢氧化钠和氢气。下列有关钠的叙述不正确的是
A.金属钠必须隔绝空气保存
B.钠与水反应放热,使钠熔化,钠是熔点最低的金属
C.钠和水反应的化学方程式为 2Na+2H2O=2NaOH+H2↑
D.把钠投入硫酸铜溶液中会产生无色无味的气体和蓝色沉淀
难度: 简单查看答案及解析
-
下列各组物质中,能相互反应且反应前后溶液总质量保持不变的是 ( )
A.氧化铁固体和盐酸 B.铝和硫酸铜溶液
C.硫酸和烧碱溶液 D.碳酸钾溶液和硝酸钠溶液
难度: 简单查看答案及解析
-
在锥形瓶甲中放入10g块状纯净的碳酸钙,在锥形瓶乙中放入10g粉末状纯净的碳酸钙,分别同时加入足量同浓度的稀盐酸与碳酸钙反应。下列图中对该实验产生气体的质量与反应时间的关系,描述合理的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
在一只盛有稀硫酸的烧杯中飘浮着一个木块,往烧杯中加入少量的某种物质后,木块浸没在水中的体积变大则加入固体物质可能是 ( )
A.Fe B.Cu C.Ba(OH)2 D.Mg(NO3)2
难度: 中等查看答案及解析
-
将25克甲物质跟5克乙物质发生反应,所得混合物中有10克甲、11克丙,还有另一种新物质丁。若甲、乙、丙、丁的相对分子质量分别为30、20、44、18,化学式分别为A、B、C、D。则下列化学方程式中正确的是( )
A.A+B=C+D B.A+2B=2C+D
C.2A+B=2C+D D.2A+B=C+2D
难度: 困难查看答案及解析
-
现有
和
组成的固体混合物共5
,向其中加入100
溶质质量分数为7.3%的稀盐酸,恰好完全反应,得到105
不饱和溶液。则原固体混合物中镁元素的质量为
A.1.2
B.12
C.2.4
D.4.8
难度: 中等查看答案及解析
-
甲、乙、丙、丁分别为1~18号元素中的一种,且核电荷数依次增大,甲的单质是一种最理想的燃料,乙原子的最外层电子数是电子层数的3倍,丙的离子带一个单位的正电荷,丁与乙的原子最外层电子数相同。下列有关说法错误的是
A. 甲和乙元素组成的物质分解能得到氧气
B. 丙和丁的原子在化学反应中都容易失去电子
C. 甲、乙、丙三种元素能组成一种碱
D. 丁的单质在乙的单质中燃烧,产生蓝紫色火焰
难度: 中等查看答案及解析
-
在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如下图所示。图中a、b、c、d分别表示相应物质的质量分数。下列数据正确的是
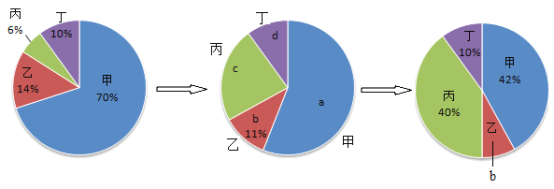
A.a=56% B.b=6% C.c=17% D.d=8%
难度: 中等查看答案及解析
-
如果按某种标准能将 Cu2O、Na2SO3、NO 划为同一类物质,则下列物质中能划分为此类 物质的是 ( )
A.K2SO4 B.K2MnO4 C.NaH2PO4 D.HNO3
难度: 困难查看答案及解析