-
适度饮水有益于健康,但过量饮水使体内电解质浓度过低,导致生理紊乱而引起“水中毒”,下列属于人体内常见电解质的是 ( )
A.CO2 B.NaCl C.BaSO4 D.葡萄糖
难度: 简单查看答案及解析
-
溶液、胶体和浊液这三种分散系的根本区别是
A. 是否是大量分子或离子的集合体 B. 是否能通过滤纸
C. 分散质粒子直径的大小 D. 是否均一、透明、稳定
难度: 简单查看答案及解析
-
我们生活在千变万化的物质世界里。下列变化中,没有发生氧化还原反应的是( )
A.爆竹爆炸

B.木炭燃烧

C.钢水浇铸
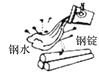
D.电解水
难度: 简单查看答案及解析
-
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性。磁流体的分散质粒子直径在5.5~36 nm之间。下列说法正确的是( )
A.所得的分散系属于悬浊液
B.该分散系能产生丁达尔效应
C.所得的分散系中水是分散质
D.将所得分散系过滤,在滤纸上能得到分散质
难度: 简单查看答案及解析
-
当光束通过下列物质时,不会出现丁达尔效应的是( )
①氢氧化铁胶体 ②水 ③有尘埃的空气 ④蔗糖溶液 ⑤硫酸铜溶液
A.①②④ B.①③⑤ C.①③④ D.②④⑤
难度: 简单查看答案及解析
-
下列叙述中,正确的是( )
A.KNO3固体不导电,所以KNO3不是电解质
B.铜丝、石墨均能导电,所以它们都是电解质
C.熔融的MgCl2能导电,所以MgCl2是电解质
D.NaCl溶于水,在通电条件下才能发生电离
难度: 简单查看答案及解析
-
下列离子方程式中,书写正确的是( )
A.将稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑
B.将氧化镁与稀盐酸混合:MgO+2H+=Mg2++H2O
C.将铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
D.将稀盐酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3
难度: 简单查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是( )。
A.H+、Cl-、Ca2+、
B.Na+、Mg2+、SO42-、OH-
C.K+、Na+、OH-、Cl-
D.Cu2+、Ba2+、Cl-、SO42-
难度: 简单查看答案及解析
-
下列化学反应中,不属于氧化还原反应的是 ( )
A. Mg+2HCl===MgCl2+H2↑
B. 2NO+O2===2NO2
C. CuO+H2
Cu+H2O
D. CaCl2+Na2CO3===CaCO3↓+2NaCl
难度: 简单查看答案及解析
-
下列转化,需要加入氧化剂才能实现的是( )
A.I2
I- B.Fe2+
Fe3+ C.HCO3-
CO2 D.MnO4-
Mn2+
难度: 简单查看答案及解析
-
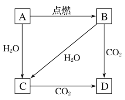
用流程图示的方法可以清楚反映物质之间的转化关系,如在常温下金属Na露置于空气中发生一系列变化:Na
乙
NaOH
Na2CO3·хH2O
Na2CO3。上述转化关系中的物质乙是( )
A.Na2O2 B.Na2O C.NaCl D.NaHCO3
难度: 简单查看答案及解析
-
保存钠的方法是( )
A.放在棕色瓶中 B.放在细沙中 C.放在水中 D.放在煤油中
难度: 简单查看答案及解析
-
NaHCO3和Na2CO3是常见的钠盐,下列对它们的俗名、分类和用途描述不正确的是( )
A.NaHCO3可做治疗胃酸过多的药剂 B.Na2CO3俗名纯碱,属于碱
C.Na2CO3可用于清洗餐具上的油污 D.NaHCO3可用于泡沫灭火器
难度: 简单查看答案及解析
-
下列对焰色反应实验操作注意事项的说明,正确的是( )
①钾的火焰颜色,要透过蓝色钴玻璃观察
②先把铂丝灼烧到与原来火焰颜色相同,再蘸取被检验的物质
③每次实验后,要用盐酸把铂丝洗净
④实验时最好选择本身颜色较微弱的火焰
⑤没有铂丝,也可用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确 C.仅有⑤不正确 D.全对
难度: 简单查看答案及解析
-
Cl2是一种重要的化工原料。下图是一些含氯产品。

①中钢瓶上应贴的标签为( )
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
难度: 简单查看答案及解析
-
下列说法中不正确的是( )
A.Cl2在与金属反应时表现强氧化性
B.任何物质的燃烧必须有O2参与
C.Cl2与H2O反应的离子方程式为Cl2+H2O=HClO+H++Cl-
D.漂白粉的有效成分是Ca(ClO)2
难度: 简单查看答案及解析
-
下列化合物中,不能通过单质间化合直接制取的是( )
A. FeCl2 B. CuCl2 C. HCl D. FeCl3
难度: 中等查看答案及解析
-
欲除去Cl2中的少量HCl气体,可选用
A.NaOH溶液 B.饱和食盐水 C.浓硫酸 D.石灰水
难度: 中等查看答案及解析
-
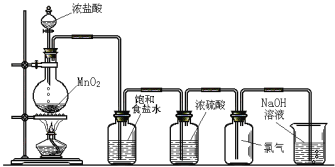
实验室制氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性;②缓缓加热;③在烧瓶中加入少量的MnO2,向分液漏斗中加入浓盐酸;④通过分液漏斗慢慢向烧瓶中注入浓盐酸;⑤将多余氯气用浓NaOH溶液吸收;⑥当有连续气泡出现时,开始用向上排空气法收集氯气。
A.①②③④⑤⑥ B.③④②①⑥⑤
C.①④③②⑥⑤ D.①③④②⑥⑤
难度: 简单查看答案及解析
-
下列实验现象的描述不正确的是( )
A.钠在空气中燃烧,发出黄色火焰,生成白色固体
B.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方形成白雾
C.过氧化钠固体与水反应放热,生成使带火星的木条复燃的气体
D.将干燥的有色布条放入盛有干燥氯气的集气瓶中,布条不褪色
难度: 简单查看答案及解析
-
下列物质中,既含有氯分子,又含有氯离子的是( )
A.氯化钠溶液 B.新制氯水
C.漂白粉 D.液氯
难度: 简单查看答案及解析
-
某同学在实验室中进行如下实验:
编号
Ⅰ
Ⅱ
Ⅲ
实验
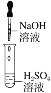
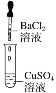

现象
没有明显变化,溶液仍为无色
有沉淀生成,溶液为蓝绿色
有无色气泡产生
以下结论不正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为BaSO4
C.Ⅲ中发生的反应是离子反应
D.Ⅲ中发生反应的离子方程式为2H++Zn=Zn2++H2↑
难度: 简单查看答案及解析