-
Cl2是一种重要的化工原料。
(1)在常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液。该反应的离子方程式为:_______________________。
(2) 工业上利用Cl2制盐酸,其化学方程式为_____________________________。
高一化学填空题简单题查看答案及解析
-
(12分)工业上将纯净干燥的氯气通入到0.5 mol·L-1NaOH溶液中得到漂白水。某同学想在实验室探究Cl2性质并模拟制备漂白水,下图是部分实验装置。已知KMnO4与浓盐酸反应可以制取Cl2。(装置D中纸条为红色)
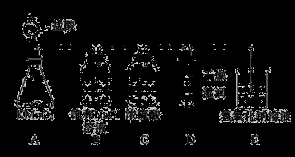
(1)配平KMnO4与盐酸反应的化学方程式:
KMnO4+ HCl(浓) = KCl + MnCl2+ Cl2↑+ H2O
(2)如果反应中转移0.5mol电子,则生成Cl2的物质的量为____________。
(3)浓硫酸的作用是 。
(4)实验时装置D中的现象是 。
(5)装置E中发生化学反应的离子方程式为 。
(6)配制480 mL物质的量浓度为0.5 mol·L-1NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ,需称量的NaOH的质量是 。
高一化学填空题中等难度题查看答案及解析
-
工业上将纯净干燥的氯气通入到0.5 mol·L-1 NaOH溶液中得到漂白水。某同学想在实验室探究Cl2性质并模拟制备漂白水,下图是部分实验装置。已知KMnO4与浓盐酸反应可以制取Cl2。(注:装置D中布条为红色)

(1)用装置A制备Cl2,该同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未顺利流下,你认为原因可能是:__________________。
(2)配平KMnO4与盐酸反应的化学方程式:
KMnO4+ HCl(浓) = KCl + MnCl2+ Cl2↑+ H2O ,该反应中氧化剂和还原剂的物质的量之比为________。
(3)饱和食盐水的作用是______________,浓硫酸的作用_____________,装置E的作用是_______________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_________________________。
(5)配制450 mL物质的量浓度为0.4 mol·L-1 NaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ,需用托盘天平称量NaOH的质量是 。
高一化学实验题困难题查看答案及解析
-
下列说法不正确的是
A.Cl2能使湿润的有色布条褪色,所以Cl2具有漂白性
B.红热的铁丝在Cl2中剧烈燃烧,反应生成FeCl3
C.利用溴单质的氧化性可以把碘离子转化为碘单质
D.实验室常用NaOH溶液吸收多余的Cl2以避免污染
高一化学选择题中等难度题查看答案及解析
-
下列关于工业生产的说法正确的是
A. 工业上以氯气和澄清石灰水为原料制造漂白粉
B. 工业上利用H2和Cl2的混合气体在光照下反应来制取盐酸
C. 工业上将氯气溶于NaOH溶液制备漂白粉
D. 漂白粉要干燥和密封保存
高一化学单选题简单题查看答案及解析
-
Cl2是一种重要的化工原料,结合氯气的相关知识解决下列问题。
(1)工业上将氯气通入消石灰中制取漂白粉,写出该反应的化学方程式__________。
(2)漂白粉的有效成分是(填化学式)_________。
(3)氯水与二氧化硫均具有漂白性,若将两者按适当比例混合则漂白性很差,用离子方程式表示其原因____。
(4)实验室可以用KMnO4与浓盐酸在常温下制备Cl2。高锰酸钾溶液常用于物质的定性检验与定量分析。某化学兴趣小组在实验室里用0.1mol/LKMnO4溶液与300ml0.2mol/L的KI溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的体积为________ml。(已知MnO4-在此条件下被还原为Mn2+)
高一化学填空题中等难度题查看答案及解析
-
(15分)工业上将纯净干燥的氯气通入到物质的量浓度为0.375 mol·L-1NaOH溶液中得到漂白水。某同学想在实验室探究Cl2性质并模拟制备漂白水,下图是部分实验装置。已知KMnO4与盐酸溶液反应可以制取Cl2。
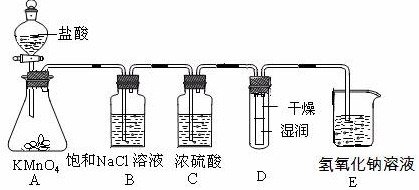
(1)配制物质的量浓度为0.375 mol·L-1NaOH溶液100mL时, 用托盘天平称取所需的NaOH质量为 。
(2)浓硫酸的作用是 。
(3)装置E中发生化学反应方程式为 。
(4)装置B中饱和NaCl溶液的作用是________。
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色。该同学认为Cl2的密度比空气大,可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的。请判断该解释是否合理,并分析产生上述实验现象的原因
________ ;如需改进,请简述设计方案 (若认为合理。则此问可不作答)。
(6)氯元素含量为10%的漂白水溶液355g,其中含NaClO的物质的量为 mol。
高一化学实验题简单题查看答案及解析
-
(1)实验室里可以用KMnO4与浓盐酸反应制取氯气,其反应的离子方程式为: ________
(2)某温度下,将Cl2通入NaOH 溶液中,反应得到含有C1O-与C1O3-物质的量之比为1: 1的混合液,
反应的化学方程式是________________________。
(3)“流感”成为2017 年冬季最可怕的流行病,历城二中要求每班每天必须用“84”消毒液进行消
毒,已知某品牌“84”消毒液的有效成分为NaClO,写出向该溶液中通入过量的CO2所发生的有关离子方程式________________________
(4)氰(CN) 2的化学性质和卤素(X2) 很相似,化学上称为拟卤素。试写出(CN)2与水反应的化学方程式: _______
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当
于多少克Cl2的氧化能力。NaClO2的有效氯含量为_________。(计算结果保留两位小数)
高一化学综合题中等难度题查看答案及解析
-
乙烯和丙烯是重要有机化工原料。
I.以乙烯为原料可以制备乙二醇和高分子化合物B。
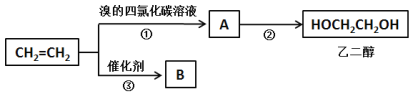
(1)①的化学方程式为______________。
(2)②为取代反应,通过A与NaOH溶液加热条件下完成转化。②的化学反应方程式为__________。
(3)③的反应类型为_______________,B的结构简式为________________。
II.丙烯酸乙酯天然存在于菠萝等水果中,是一种天然香料,也可以由乙烯和丙烯为原料合成。
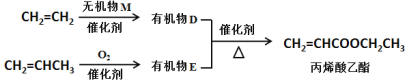
(4)有机物E中的官能团是_________________。
(5) D与E反应生成丙烯酸乙酯的化学反应方程式为__________________。
(6)下列说法正确的是______________。
a.乙烯、丙烯是石油裂解的产物 b.乙二醇易溶于水
c.E能使酸性高锰酸钾溶液褪色 d.D可以由葡萄糖分解得到
高一化学综合题简单题查看答案及解析
-
下列离子方程式书写正确的是( )
A.常温下氯气与NaOH溶液反应:Cl2+2OH -═Cl-+ClO-+H2O
B.FeCl3溶液中加入铜粉:Fe3++Cu═Fe2++Cu2+
C.铜与浓硫酸反应:Cu+4H++SO42-═Cu2++SO2↑+2 H2O
D.实验室用大理石跟稀盐酸制取二氧化碳:2H++CO32-═CO2↑+H2O高一化学选择题中等难度题查看答案及解析