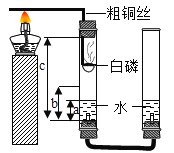
-
下列关于物质用途的描述中,不正确的是
A. 氧气用于气焊 B. 二氧化碳作燃料
C. 浓硫酸作干燥剂 D. 碳酸氢钠用于治疗胃酸过多
难度: 简单查看答案及解析
-
在空气的成分中,体积分数约占21%的是( )
A.氮气 B.二氧化碳 C.氧气 D.稀有气体
难度: 简单查看答案及解析
-
下列物质中,含有氧分子的是
A. O2 B. MnO2 C. CO2 D. H2O2
难度: 简单查看答案及解析
-
中华民族的发明创造为人类文明进步作出了巨大贡献。下列古代发明及应用中,不涉及化学变化的是
A.
 陶瓷烧制 B.
陶瓷烧制 B.  玉石雕印
玉石雕印C.
 粮食酿醋 D.
粮食酿醋 D.  火药爆炸
火药爆炸难度: 简单查看答案及解析
-
人体缺“铁”会引起( )
A.骨质疏松 B.佝偻病 C.食欲不振 D.贫血
难度: 简单查看答案及解析
-
下列食物中,富含蛋白质的是
A. 清蒸鱼 B. 小米粥 C. 白面馒头 D. 凉拌黄瓜
难度: 简单查看答案及解析
-
下列属于新能源的是
A.煤 B.氢能 C.石油 D.天然气
难度: 简单查看答案及解析
-
下列对于灭火原理的分析中,正确的是( )
A.砍掉大火蔓延路线前的树木——隔离可燃物
B.用锅盖盖灭油锅内的火——降低油温
C.用水扑灭燃着的木材——降低木材的着火点
D.用扇子扇灭烛火——隔绝空气
难度: 简单查看答案及解析
-
小刚测定了下列4种日用品的pH,其中呈酸性的是
日用品
A.洁厕灵
B.洗涤灵
C.洗发水
D.消毒液
pH
1
7
9
12
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列实验操作中,正确的是
A.倾倒液体
B.称量氢氧化钠
C.测定溶液的pH
D.稀释浓硫酸
难度: 简单查看答案及解析
-
如图为氢氧化钙的溶解度曲线,下列说法不正确的是( )
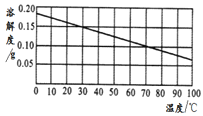
A.氢氧化钙的溶解度随温度的升高而减小
B.30℃时,100g水中最多溶解0.15g氢氧化钙
C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数变小
D.70℃时,饱和石灰水中溶质和溶液的质量比为0.1:100
难度: 中等查看答案及解析
-
A和B点燃条件下反应生成C和D。反应前后分子变化的微观示意图如下:
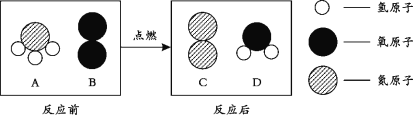
下列说法不正确的是( )
A.一个A分子中含有4个原子 B.D的化学式为H2O
C.生成物B和D的个数比为1:1 D.4种物质中,属于化合物的是A和D
难度: 中等查看答案及解析