-
某无土栽培所需的营养液成分是含有N、P、K、Ca等元素的无机盐,该配方适用于苦瓜、黄瓜、生菜的种植。可作营养液成分的是
A.P2O5 B.KOH C.NH4Cl D.CaCO3
难度: 中等查看答案及解析
-
逻辑推理是化学学习中常用的思维方法,下列推理正确的是
A.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B.化合物是由不同元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物
C.单质中只含有一种元素,所以只含有一种元素的物质一定是单质
D.活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
难度: 中等查看答案及解析
-
我国的成语、诗词和谚语中蕴含着科学道理。下列有关化学角度的认识中不正确的是( )
A.“蜡炬成灰泪始干”:说明蜡烛燃烧过程中既有化学变化,又有物理变化
B.“真金不怕火炼”:说明黄金的化学性质不活泼
C.“满架蔷薇一院香”:因为分子在不断运动
D.“百炼成钢”与“沙里淘金”:所蕴含的化学原理相同
难度: 简单查看答案及解析
-
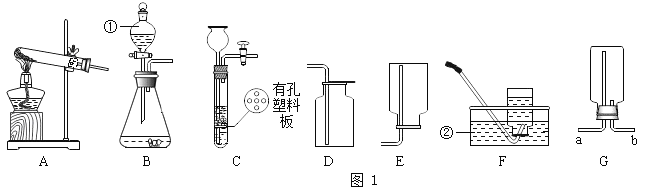
下列实验操作中,正确的是( )
A.
 点燃酒精灯 B.
点燃酒精灯 B. 过滤
过滤C.
 量取液体体积读数 D.
量取液体体积读数 D. 称量NaCl固体
称量NaCl固体难度: 简单查看答案及解析
-
垃圾分类是社会进步和生态文明的标志,是人人均可参与其中来保护环境和改善环境的方式。我们追求进步,崇尚文明,希望有碧水蓝天净土,共建美好家园。处置矿泉水瓶的正确方法是
A.扔进有害垃圾桶
B.扔进可回收垃圾桶
C.看到垃圾桶就扔进去
D.扔进其他垃圾桶
难度: 简单查看答案及解析
-
碳化硅硬度仅次于金刚石,具有较强的耐磨性能,是耐磨管道、叶轮、泵室、旋流器、矿斗内衬的理想材料,其耐磨性能是铸铁、橡胶使用寿命的5--20倍。也是航空飞行跑道的理想材料之一。已知碳化硅中碳元素显-4价,硅元素显+4价,则碳化硅的化学式为
A.SiC
B.Si2C3
C.Si3C2
D.SiC2
难度: 简单查看答案及解析
-
近期,英国《自然》杂志刊发了材料领域的最新研宄成果---一科学家找到了接近常温的超导材料“超氢化镧”。下列有关镧的说法错误的是( )
A. 镧是金属元素 B. 元素符号是La C. 中子数是57 D. 相对原子质量是138.9
难度: 简单查看答案及解析
-
用如图所示的密闭实验装置,能使液面a比液面b高的一组固体和液体可以是
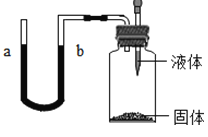
①食盐和水
②二氧化锰和过氧化氢溶液
③固体氢氧化钠和水
④石灰石和稀盐酸
⑤硝酸铵和水
⑥铁与稀硫酸
A.①②④ B.①②⑤⑥ C.①③④⑤ D.②③④⑥
难度: 中等查看答案及解析
-
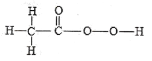
中国古代劳动人民很早就开始使用谷物酿酒了,酒的主要成分就是乙醇。汉代刘安在《淮南子》中提到“清盎之美,始于耒耜”。乙醇的分子结构模型如图所示,则下列叙述正确的是
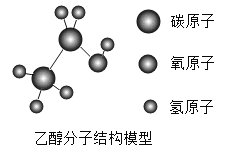
A.75%的酒精可用于消毒
B.一个乙醇分子中含有28个质子
C.乙醇是由碳原子、氢原子、氧原子构成的有机物
D.乙醇中氧元素的质量分数最大
难度: 简单查看答案及解析
-
分类是学习和研究化学物质的一种常用的科学方法,下列分类正确的是( )
A. 碘酸钾的化学式是KlO3,属于盐
B. 一氧化碳中含有碳元素,属于有机物
C. 臭氧中含有氧元素,属于氧化物
D. 碳酸氢钠能解离出H+,属于酸
难度: 中等查看答案及解析
-
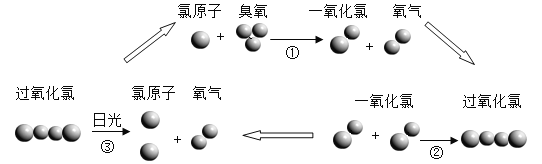
如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子.则该反应( )
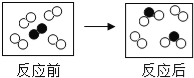
A.是化合反应 B.有单质生成
C.反应前后分子种类不变 D.参加反应的两种分子个数比为4:1
难度: 中等查看答案及解析
-
2019年诺贝尔化学奖颁给了美国德州大学奥斯汀分校约翰﹒古迪纳夫、美国纽约州立大学宾汉姆分校斯坦利﹒威廷汉和日本旭化成株式会社吉野彰三人,以表彰他们对锂离子电池研发的卓越贡献。那么,关于锂离子电池下列说法不正确的是
A.锂离子电池一般用石墨做电极是利用了石墨良好的导电性
B.锂在化学反应中容易失去一个电子形成锂离子,其符号为Li+
C.锂离子电池一般使用锂合金作为正极材料,锂合金是一种新型的锂金属单质
D.未来锂离子电池的广泛应用,体现了化学科学的发展能促进人类社会进步,提高人们的生活质量
难度: 简单查看答案及解析
-
甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是
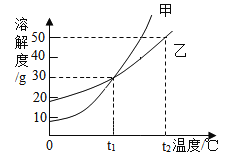
A.t1°C时,甲和乙的溶解度均为30
B.t2°C时, 甲和乙的饱和溶液中溶质的质量分数相等
C.t2°C时, 100g 水中放入60g乙,其溶质的质量分数为37.5%
D.t2°C时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
难度: 简单查看答案及解析
-
法匹拉韦(favipiravir)作为一种新型广谱抗RNA病毒药物,对新冠肺炎有一定疗效,化学式为C5H4FN3O2,下列关于法匹拉韦说法错误的是
A.法匹拉韦是由15个原子构成的
B.法匹拉韦相对分子质量是157
C.法匹拉韦是由碳、氢、氟、氮、氧五种元素组成的
D.法匹拉韦中含碳元素的质量分数最高
难度: 简单查看答案及解析
-
如图为一氧化碳还原氧化铁的“微型”实验装置,已知:
,下列说法错误的是
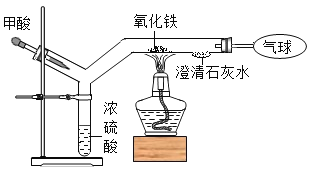
A.实验中所需CO可现制现用
B.此装置可节约用品,污染小
C.可以观察到固体由黑色变为红色
D.用气球收集尾气可减少一氧化碳对大气的污染
难度: 简单查看答案及解析
-
化学概念逻辑上存在如图所示关系,对下列概念间的关系说法正确的是( )

①纯净物与混合物属于包含关系 ②化合物与氧化物属于包含关系 ③单质与化合物属于交叉关系 ④金属元素与非金属元素属于并列关系 ⑤中和反应与复分解反应属于并列关系
A.①② B.③④ C.①⑤ D.②④
难度: 中等查看答案及解析
-
下列有关物质的检验、除杂、分离、区分所用的试剂或方法错误的是( )
选项
实验目的
所用试剂或方法
A
检验NH4NO3溶液和K2SO4溶液
NaOH溶液或Ba(NO3)2溶液
B
除去生石灰中含有杂质石灰石
水或稀盐酸
C
从H2O2溶液制氧气的残余物中分离出MnO2
过滤或蒸发
D
区分失去标签的浓硫酸和稀硫酸
水或小木条
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
根据实验操作所绘制的图象中,正确的是( )
A.
将铁粉加入到一定量的稀盐酸中,生成氢气的质量与加入铁粉的质量关系
B.
用一定量的一氧化碳和氧化铁反应,剩余固体质量与反应时间的关系
C.
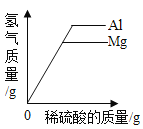 向等质量的金属镁和铝中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系
向等质量的金属镁和铝中加入足量且质量分数相等的稀硫酸,生成氢气的质量与加入稀硫酸质量的关系D.
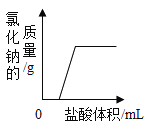 向久置空气中NaOH溶液中加入盐酸,生成氯化钠质量与加入盐酸的体积关系
向久置空气中NaOH溶液中加入盐酸,生成氯化钠质量与加入盐酸的体积关系难度: 困难查看答案及解析
-
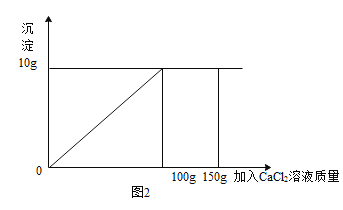
向下表中的甲物质中逐滴加入乙物质溶液至过量,反应生成气体或沉淀的质量与加入乙的质量关系符合如下曲线描述的是
选项
甲
乙
A.
铜、锌的混合物粉末
稀盐酸
B.
盐酸和稀硫酸的混合溶液
氯化钡溶液
C.
氯化钠和氯化钙的混合溶液
碳酸钠溶液
D.
盐酸和氯化铜的混合溶液
氢氧化钠溶液
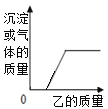
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
如表提供的四组物质符合图示,相连物质间在一定条件下可以发生反应的是()
甲
乙
丙
丁
A
CO
O2
H2SO4
CuO
B
Mg
HCl
CuSO4
NaOH
C
KOH
SO2
NaOH
CuSO4
D
Na2CO3
Ca(OH)2
HCl
CaCl2
A. 选项A B. 选项B C. 选项C D. 选项D
难度: 中等查看答案及解析