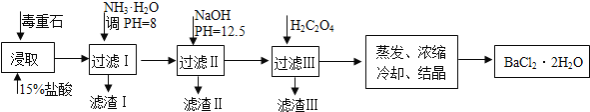
-
用CH4催化还原NOx可以消除氮氧化合物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ/mol
下列说法中错误的是( )
A. 等物质的量的CH4在反应①、②中转移电子数相同
B. 由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l);△H>-574kJ/mol
C. 4NO2(g)+2N2(g)=8NO(g);△H=+586kJ/mol
D. 若用标准状况下4.48L CH4把NO2还原为N2,整个过程中转移的电子总数为1.6NA
难度: 中等查看答案及解析
-
有一支50mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体全部放出,盛入量筒内,所得液体体积一定是( )
A. a mL B. (50―a)mL C. 大于(50―a)mL D. 大于amL
难度: 中等查看答案及解析
-
pH相同的氨水、NaOH和Ba(OH)2溶液,分别用蒸馏水稀释到原来的X、Y、Z倍,稀释后三种溶液的pH仍然相同,则X、 Y、Z的关系是( )
A.X=Y=Z B.X>Y=Z C.X<Y=Z D.X=Y<Z
难度: 简单查看答案及解析
-
下列说法错误的是
A.反应产物的总焓与反应物的总焓之差,称为反应焓变
B.反应产物的总焓小于反应物的总焓,该反应为吸热反应
C.同一反应在不同温度下进行,其焓变是不同的
D.已知2NO2(g)=N2O4(g) △H1,N2O4(g)=2NO2(g) △H2,则△H1=-△H2
难度: 中等查看答案及解析
-
某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用pH计测得某稀盐酸的pH为1.54
C.用广泛pH试纸测得某溶液的pH为2.3
D.配制100mL1mol/L的NaCl溶液用托盘天平称取5.85gNaCl固体
难度: 中等查看答案及解析
-
下列溶液一定呈中性的是( )
A.pH=7的溶液 B.酸与碱恰好完全反应生成正盐的溶液
C.使石蕊试液呈紫色的溶液 D.c(H+)=c(OH-)=10-6mol/L溶液
难度: 中等查看答案及解析
-
pH值相同的盐酸溶液与醋酸溶液分别和锌粒反应,若最后锌都已完全溶解,放出的气体一样多,下列说法正确的是( )
A.反应所需时间:醋酸>盐酸
B.整个反应阶段的平均反应速率:醋酸>盐酸
C.开始的反应速率:盐酸>醋酸
D.参加反应的锌的质量:盐酸<醋酸
难度: 中等查看答案及解析
-
下列有关滴定操作的顺序正确的是( )
①检查滴定管是否漏水;
②用标准溶液润洗盛装标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
③用蒸馏水洗涤玻璃仪器;
④装标准溶液和待测液并调整液面(记录初读数);
⑤取一定体积的待测液于锥形瓶中;
⑥进行滴定操作
A.①③②④⑤⑥ B.①②③④⑤⑥
C.②③①④⑤⑥ D.④⑤①②③⑥
难度: 简单查看答案及解析
-
25℃时,某溶液中由水电离出的c(OH-)=1×10-13mol/L,该溶液中一定不能大量共存的离子组是( )
A.NH
、Fe3+、SO
、Cl- B.CO
、PO
、K+、Na+
C.Na+、SO
、NO
、Cl- D.HPO
、Na+、HSO
、K+
难度: 中等查看答案及解析
-
已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
A.此酸的电离平衡常数约为1×10-7
B.升高温度,溶液的pH增大
C.该溶液的pH=4
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
难度: 中等查看答案及解析
-
实验测得常温下0.1mol/L某一元酸HA溶液的pH值大于1,0.1mol/L某一元碱BOH溶液里
=10-12。将此两种溶液等体积混合后,所得溶液的各离子的浓度由大到小排列的顺序( )
A.c(B+)>c(A-)>c(OH-)>c(H+) B.c(A-)>c(B+)>c(H+)>c(OH-)
C.c(B+)=c(A-)>c(H+)=c(OH-) D.c(B+)>c(A-)>c(H+)>c(OH-)
难度: 困难查看答案及解析
-
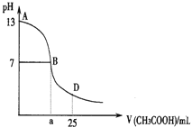
在100 mL某一元弱酸的溶液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。
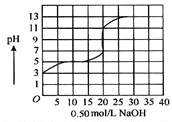
下列叙述正确的是( )
A.该弱酸在滴定前的浓度是0.15 mol/L
B.该弱酸稀释10倍后pH为4
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定过程为求滴定终点,最合适的指示剂是甲基橙
难度: 中等查看答案及解析
-
在一密闭容器中充入2molA和1molB发生反应:2A(g)+B(g)
xC(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol,B:0.3mol,C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%。则x的值为( )
A.只能为2 B.只能为3 C.只能为4 D.可能为2或3
难度: 困难查看答案及解析
-
如图是温度和压强对X+Y
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
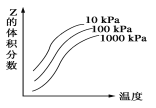
A.上述可逆反应的正反应为放热反应
B.X和Y中只有一种为气态,Z为气态
C.X、Y、Z均为气体
D.上述反应的逆反应ΔH>0
难度: 中等查看答案及解析
-
某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4 mol·L-1
难度: 困难查看答案及解析
-
反应N2O4(g)
2NO2(g) ΔH=57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
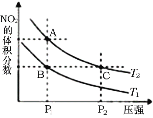
A.由状态B到状态A,可以用加热的方法
B.A、C两点气体的颜色:A深,C浅
C.A、C两点的反应速率:A>C
D.A、C两点气体的平均相对分子质量:A>C
难度: 中等查看答案及解析