-
“ 17世纪中国工艺百科全书” 《天工开物》为明代宋应星所著。下列说法错误的是
A.“ 凡铁分生熟,出炉未炒则生,既炒则熟” 中的“ 炒” 为氧化除碳过程
B.“ 凡铜出炉只有赤铜,以倭铅(锌的古称)参和,转色为黄铜” 中的“ 黄铜” 为锌铜金
C.“ 凡石灰经火焚,火力到后,烧酥石性,置于风中久自吹化成粉” 中的“ 粉” 为 CaO
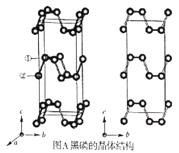
D.“ 凡松烟造墨,入水久浸,以浮沉分清悫” ,是指炭因颗粒大小及表面积的不同而浮沉
难度: 中等查看答案及解析
-
已知 NA是阿伏加德罗常数的值,下列说法正确的是
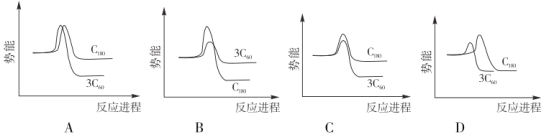
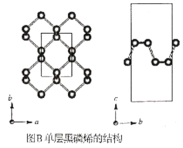
A.32gS8与 S6(
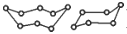 )的混合物中所含共价键数目为NA
)的混合物中所含共价键数目为NAB.1L0.1mol• L-1H2C2O4溶液中含 C2O42- 离子数为0.1NA
C.2molNO与 2molO2在密闭容器中充分反应,转移的电子数为 8NA
D.标准状况下 22.4L氯气与甲烷的混合气体,光照时充分反应生成 HCl分子数为NA
难度: 中等查看答案及解析
-
某学习小组用下列装置完成了探究浓硫酸和 SO2性质的实验(部分夹持装置已省略),下列“ 现象预测” 与“ 解释或结论” 均正确的是
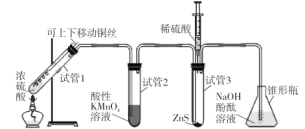
选项
仪器
现象预测
解释或结论
A
试管1
有气泡、酸雾,溶液中有白色固体出现
酸雾是SO2所形成,白色固体是硫酸铜晶体
B
试管2
紫红色溶液由深变浅,直至褪色
SO2具有还原性
C
试管3
注入稀硫酸后,没有现象
由于Ksp(ZnS)太小,SO2与ZnS在注入稀硫酸后仍不反应
D
锥形瓶
溶液红色变浅
NaOH溶液完全转化为NaHSO3溶液,NaHSO3溶液碱性小于NaOH
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
科学家发现了在细胞层面上对新型冠状病毒(2019-nCOV)有较好抑制作用的药物:雷米迪维或伦地西韦(RemdeSivir,GS-5734)、氯喹 (ChloroqquinE,Sigma-C6628)、利托那韦 (Ritonavir)。其中利托那韦(Ritonavir)的结构如下图,关于利托那韦说法正确的是
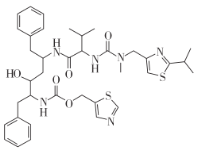
A.能与盐酸或 NaOH溶液反应
B.苯环上一氯取代物有 3种
C.结构中含有 4个甲基
D.1mol该结构可以与13molH2加成
难度: 中等查看答案及解析
-
最近我国科学家研制出一种高分子大规模储能二次电池,其示意图如下所示。这种电池具有寿命长、安全可靠等优点,下列说法错误的是
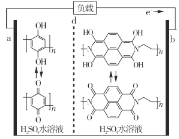
A.硫酸水溶液主要作用是增强导电性
B.充电时,电极b接正极
C.d膜是质子交换膜
D.充放电时,a极有
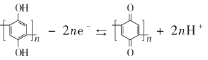
难度: 困难查看答案及解析
-
科学家合成出了一种用于分离镧系金属的化合物 A(如下图所示),短周期元素 X、Y、Z原子序数依次增大,其 中 Z位于第三周期。Z与 Y2可以形成分子 ZY6,该分子常用作高压电气设备的绝缘介质。下列关于 X、Y、Z的叙述,正确的是
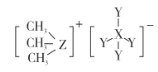
A.离子半径:Y >Z
B.氢化物的稳定性:X >Y
C.最高价氧化物对应水化物的酸性:X >Z
D.化合物 A中,X、Y、Z最外层都达到 8电子稳定结构
难度: 中等查看答案及解析
-
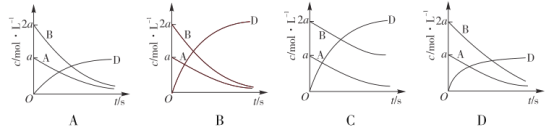
常温下,向20mL0.1mol• L-1HB溶液中逐滴滴入 0.1mol• L-1NaOH溶液,所得 PH变化曲线如图所示。下列说法错误的是
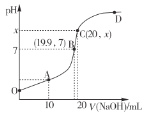
A.OA各点溶液均存在:c(B-) >c(Na+)
B.C至 D各点溶液导电能力依次增强
C.点 O时,pH>1
D.点 C时,X约为 10.4
难度: 困难查看答案及解析
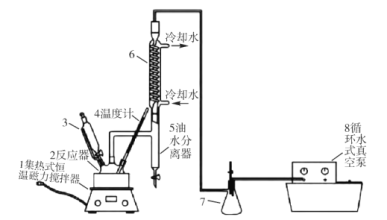
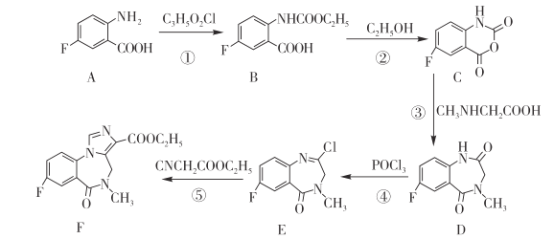
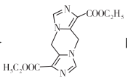 的合成路线________(无机试剂任选)。
的合成路线________(无机试剂任选)。