-
下列物质属于电解质的是
A.H2CO3 B.Cu C.盐酸 D.NH3
难度: 简单查看答案及解析
-
下列仪器及名称都正确的是
A.蒸馏烧瓶
B.冷凝管
C.长颈漏斗
D.容量瓶
难度: 简单查看答案及解析
-
下列物质的水溶液因水解呈酸性的是
A.NaOH B.NaHSO4 C.Fe(NO3)3 D.CaCl2
难度: 中等查看答案及解析
-
下列既属于置换反应又属于放热反应的是
A.HCl+KOH=KCl+H2O B.4Na+O2=2Na2O
C.C+H2O
CO+H2 D.2Mg+CO2
2MgO+C
难度: 简单查看答案及解析
-
下列物质的名称或俗称正确的是
A.BaCO3:重晶石 B.CH3OH:木醇
C.(NH4)2Fe(SO4)2:摩尔盐 D.
:2,3,3-三甲基丁烷
难度: 简单查看答案及解析
-
下列有关化学用语表示正确的是
A.中子数为10的氧原子:
B.HCl的电子式:
C.乙酸的键线式:
D.乙炔的比例模型:
难度: 简单查看答案及解析
-
下列说法不正确的是
A.乙醇、乙二醇互为同系物 B.H、D、T互为同位素
C.足球烯、纳米碳管互为同素异形体 D.正丁烷、异丁烷互为同分异构体
难度: 简单查看答案及解析
-
下列物质性质与用途具有对应关系的是
A.AgI见光易分解,可用于人工降雨
B.SiO2具有导电性,可用于制备光导纤维
C.CuSO4能杀死某些细菌,可作自来水的消毒剂
D.Na2CO3溶液呈碱性,可用于除去铁钉表面的油污
难度: 中等查看答案及解析
-
下列说法不正确的是
A.工业炼铁用焦炭在高温下直接还原铁矿石
B.紫外可见分光光度法可用来测定苯酚溶液中的苯酚含量
C.工业上乙苯、异丙苯通过苯与乙烯、丙烯反应获得
D.工业上以氯气和石灰乳为原料制造漂白粉
难度: 中等查看答案及解析
-
下列说法正确的是
A.利用蓝绿藻光解水是现阶段大量获取氢气的方法
B.煤的液化是物理变化,煤经液化可得到液态燃料油
C.石油的分馏产物中含有大量不饱和烃,可使酸性高锰酸钾溶液褪色
D.垃圾焚烧处理厂把生物质能转化为热能、电能,改善城市环境
难度: 中等查看答案及解析
-
下列实验操作或实验事故处理正确的是
A.实验室制硝基苯时,往浓硫酸中加入苯混合后再滴加硝酸
B.电器设备引起的火灾,可以用四氯化碳灭火器灭火
C.不慎将苯酚沾到皮肤上,应用65℃以上的热水冲洗
D.用减压过滤的方法除去溶液中混有的Fe(OH)3胶体
难度: 中等查看答案及解析
-
下列关于硫及其化合物说法正确的是
A.硫粉和铜粉共热时反应生成黑色的硫化铜
B.浓硫酸具有吸水性,可以干燥H2S、SO2等气体
C.FeSO4可用于生产防治缺铁性贫血的药剂
D.某溶液中加入盐酸酸化的BaCl2溶液,若有白色沉淀生成,则原溶液中含有
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A.NaHCO3的水解方程式:
+H2O
H3O++
B.Fe2O3与HI充分反应:Fe2O3+6H+=2Fe3++3H2O
C.铜插入稀硝酸中:Cu+4H++2
=Cu2++2NO↑+H2O
D.NaClO溶液中通入少量的CO2:ClO-+CO2+H2O=HClO+
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W原子序数依次增大,X是地壳中含量最多的元素,Y和Z的最外层电子数之和为10,部分元素在周期表中的结构如图。下列说法正确的是
X
Y
W
A.与Z同主族的元素都是金属元素
B.X与W能形成两种常见的化合物
C.Y的最高价氧化物对应的水化合物酸性最强
D.X的简单气态氢化物热稳定性比W强是由于氢键的影响
难度: 中等查看答案及解析
-
下列说法正确的是
A.人造奶油、大豆油、汽油的主要成分都是油脂
B.植物秸秆和土豆淀粉的水解产物在一定条件下可以发酵转化成酒精
C.蛋白质溶液中加入稀的(NH4)2SO4溶液,有固体析出,加水可重新溶解
D.生活中常见的合成橡胶、有机玻璃、酚醛树脂都是通过加聚反应制备的
难度: 中等查看答案及解析
-
化合物Y用于光学树脂的合成,可由X与2-甲基丙烯酰氯在一定条件下制得如下,有关化合物X、Y的说法正确的是
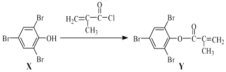
A.Y分子中最多有6个碳原子共面
B.X不能使溴水、酸性KMnO4溶液褪色
C.X、Y都能与NaOH溶液反应,1molX和Y均消耗4molNaOH
D.可用FeCl3溶液检验Y中是否混有X
难度: 中等查看答案及解析
-
常温下Ka(CH3COOH)=1.75×10−5,Kb(NH3·H2O)=1.75×10−5,下列说法正确的是
A.一定浓度的CH3COOH溶液加水稀释,所有的离子浓度都在减小
B.pH=4的CH3COOH和pH=10的NH3·H2O反应后pH=7
C.等浓度等体积的CH3COOH和NH3·H2O消耗NaHCO3的物质的量相同
D.等浓度的CH3COONa和NH4Cl溶液中阴离子浓度之和:前者小于后者
难度: 困难查看答案及解析
-
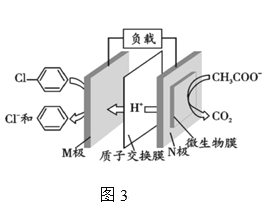
NO2、O2 和熔融 KNO3 可作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物 Y,Y 可循环使用。下列说法正确的是
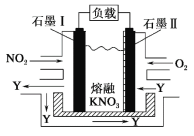
A.放电时,NO
向石墨Ⅱ电极迁移
B.电池总反应式为 4NO2+O2===2N2O5
C.石墨Ⅱ附近发生的反应为 NO+O2+e- ===NO
D.当外电路通过 4 mol e-,负极上共产生 2 mol N2O5
难度: 中等查看答案及解析
-
某反应由两步反应A
B
C构成,能量曲线如图所示,下列说法正确的是
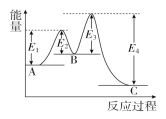
A.A、B、C三种物质中B最不稳定
B.两步反应均为放热反应
C.加入催化剂会改变两步反应的焓变
D.B
C的反应活化能是E4kJ/mol
难度: 中等查看答案及解析
-
NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下2.24LSO3溶于水生成0.1mol
B.6.4g由SO2和S2组成的混合物含有的原子数大于0.2NA
C.1mol锌和足量的浓H2SO4完全反应,转移的电子数小于2NA
D.12g金刚石(C)中含有的共价键数目为4NA
难度: 中等查看答案及解析
-
下列说法正确的是
A.SiO2硬度大与Si、O原子间的成键方式和排列方式有关
B.Al2O3熔点高,说明其中的共价键较难被削弱
C.NaOH晶体熔化时克服了离子键和共价键
D.H2O2受热易分解是因为分子间作用力弱
难度: 中等查看答案及解析
-
1L恒容密闭容器中充入2molNO和1molCl2反应:2NO(g)+Cl2(g)
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
t/min
温度/℃
0
5
8
13
T1
2
1.5
1.3
1.0
T2
2
1.15
1.0
1.0
A.T1>T2
B.T1时,反应前5min的平均速率为v(Cl2)=0.5mol·L-1·min-1
C.反应达平衡时,升高温度促进反应向正反应方向进行
D.T2时,向反应后的容器中充入2molNOCl(g),再次平衡时,c(NOCl)>2mol·L-1
难度: 困难查看答案及解析
-
常温下用0.1mol·L-1NaOH溶液滴定10.00mL二元弱酸H2A溶液,滴定曲线如图所示,d点恰好中和。假设混合时溶液体积变化忽略不计,下列说法不正确的是
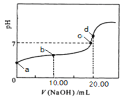
A.a点pH>1
B.c点时c(Na+)=c(H2A)+2c(A2-)+c(HA-)
C.b点时:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
D.滴定过程中c(Na+)+c(A2-)+c(HA-)+c(H2A)=0.1mol/L
难度: 中等查看答案及解析
-
已知BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓,下列说法正确的是
A.BeCl2溶液的pH<7,将其蒸干并灼烧后得到的残留物是BeCl2
B.Be(OH)2既能溶于盐酸,又能溶于NaOH溶液
C.BeCl2水溶液的导电性强,故BeCl2是离子化合物
D.工业上可以用电解熔融BeCl2的方法冶炼金属Be
难度: 困难查看答案及解析
-
某固体混合物可能由SiO2、Fe2O3、Fe、Na2SO3、Na2CO3、BaCl2中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
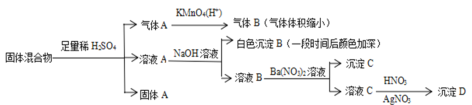
A.气体A是SO2和CO2的混合气体
B.固体A一定含有SiO2,可能含有BaSO4
C.该固体混合物中Fe2O3和Fe至少有其中一种
D.该固体混合物一定含有Na2CO3、Na2SO3、BaCl2
难度: 困难查看答案及解析
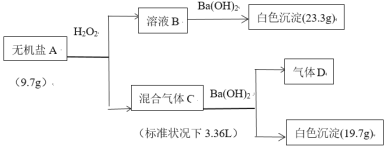

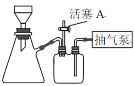
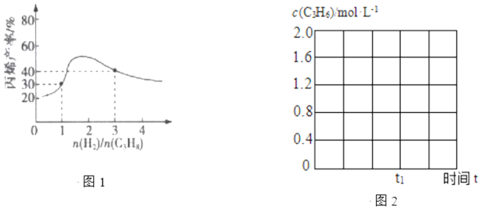
 ×100%)
×100%)