-
1L恒容密闭容器中充入2molNO和1molCl2反应:2NO(g)+Cl2(g) 2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是
| t/min 温度/℃ | 0 | 5 | 8 | 13 |
| T1 | 2 | 1.5 | 1.3 | 1.0 |
| T2 | 2 | 1.15 | 1.0 | 1.0 |
A.T1>T2
B.T1时,反应前5min的平均速率为v(Cl2)=0.5mol·L-1·min-1
C.反应达平衡时,升高温度促进反应向正反应方向进行
D.T2时,向反应后的容器中充入2molNOCl(g),再次平衡时,c(NOCl)>2mol·L-1
-
某科研小组利用如下反应消除NO和CO的污染;2NO(g)+2CO(g) N2(g)+2CO2(g) △H=xkJ/mol。T℃时,在容积为2L的恒容密闭容器中充入2molNO和2molCO,保持温度不变,5min时达到平衡状态,此时c(N2)=0.4mol/L。下列说法中不正确的是 ( )
N2(g)+2CO2(g) △H=xkJ/mol。T℃时,在容积为2L的恒容密闭容器中充入2molNO和2molCO,保持温度不变,5min时达到平衡状态,此时c(N2)=0.4mol/L。下列说法中不正确的是 ( )
A. x<0
B. α(NO)=80%
C. 0~5min内,V(CO)=0.16mol/(L·min)
D. 保持温度不变,若再向上述平衡体系中充入2molNO和2molCO,重新达平衡时,c(N2)=0.8mol/L
-
在一定温度下,向VL密闭容器中充入2molNO2,发生如下反应:2NO2(g) N2O4(g)。达平衡后,NO2的转化率为α1。再向容器中充入2 mol NO2,再次达到平衡,NO2的转化率为α2。再向容器中充入1 mol N2O4,再次达到平衡,NO2的转化率为α3 。则α1与α3的关系正确的是( )
N2O4(g)。达平衡后,NO2的转化率为α1。再向容器中充入2 mol NO2,再次达到平衡,NO2的转化率为α2。再向容器中充入1 mol N2O4,再次达到平衡,NO2的转化率为α3 。则α1与α3的关系正确的是( )
A.α1=α3 B.α1>α3
C.α1<α3 D.无法确定
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.18g氨基(-ND2)中含有的电子数为10NA
B.56gFe与1molCl2充分反应后转移电子的数目为3NA
C.向密闭容器中加入2molNO和1molO2,充分反应后容器中产物分子的数目为2NA
D.向100mL0.1mol/LNH4Cl溶液中通入NH3至溶液为中性,其中NH4+的数目为0.01NA
-
(14分)一定温度下,向2L的密闭容器中充入2molPCl3(g)和1molCl2(g),发生反应:PCl3(g)+Cl2(g) PCl5(g),5min达平衡,容器中的压强为开始时的
PCl5(g),5min达平衡,容器中的压强为开始时的 ,并且放出37.2kJ的热量,请回答下列问题:
,并且放出37.2kJ的热量,请回答下列问题:
(1)前5min内,v(Cl2)= mol·L-1·min,此温度下,平衡常数K= 。
(2)下列哪个图像能正确说明上述反应在进行到t1时刻时,达到平衡状态 。

(3)平衡后,从容器中移走0.4molPCl3,0.2molCl2和0.2molPCl5,则平衡 (填“正向移动”“逆向移动”或“不移动”),c(PCl3) (填“增大”“减小”或“不变”)。
(4)相同条件下,若起始时,向2L的密闭容器中充入1molPCl3(g)和1molPCl5(g),反应达平衡后,理论上吸收 kJ的热量。
(5)PCl5与足量的水能完全反应生成H3PO4和HCl,将反应后的混合液逐滴加入到过量的Na2CO3溶液中,请写出可能发生反应的离子方程式 (已知:H3PO4的电离平衡常数:Ka1=7.52×10-3,Ka2=6.23×10-8,Ka3=2.2×10-13;H2CO3的电离平衡常数:Ka1=4.3×10-7,Ka2=5.61×10-11)
-
[s1] 一定条件下,在一容积固定的密闭容器中充入2molNO和1molO2,发生反应:
 2NO+O2===2NO2、2NO2 N2O4。下列推测中,正确的是 ( )
2NO+O2===2NO2、2NO2 N2O4。下列推测中,正确的是 ( )
A.平衡时体系中含NO、O2、NO2、N2O4
B.平衡后容器中压强为开始时的2/3
C.达到平衡后,压缩容器容积,混合气体颜色变浅
D.达到平衡后,再充入少量O2混合气体颜色不变
[s1]14.
-
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物含量显得尤为重要。
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g) 2NO2(g),下列各项能说明反应达到平衡状态的是 。
2NO2(g),下列各项能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1 molO2同时生成2 molNO2
(2)汽车内燃机工作时会引起N2和O2的反应:N2 + O2 2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ O2(g)
2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ O2(g) 2NO(g)的△H__________0(填“>”或“<”)。
2NO(g)的△H__________0(填“>”或“<”)。

(3)NOx是汽车尾气中的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化如图所示: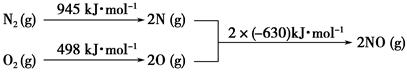
写出该反应的热化学方程式:________________________________。
Ⅱ.碳氧化物研究
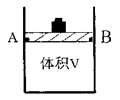
(1)在体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如右图所示,现将3molH2和2molCO放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成甲醇的反应如下:CO(g)+2H2(g) CH3OH(g)。测定不同条件、不同时间段内的CO的转化率,得到如下数据:
CH3OH(g)。测定不同条件、不同时间段内的CO的转化率,得到如下数据:
| CO的转化率 T(℃) | 10min | 20min | 30min | 40min |
| T1 | 20% | 55% | 65% | 65% |
| T2 | 35% | 50% | a1 | a2 |
①根据上表数据,请比较T1_________T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=________,该温度下的化学平衡常数为_______________。
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)________v(逆)(选填“>”、“<”或“=”),判断的理由是 。
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染。常温下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=_________________(用含a和b的代数式表示)。
-
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物含量显得尤为重要。
(1)一定条件下,将2moLNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)⇌2NO2(g),下列各项能说明反应达到平衡状态的是_____________;
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变
d.每消耗1molO2同时生成2molNO2
(2)汽车内燃机工作时会引起N2和O2的反应:N2+O2═2NO,是导致汽车尾气中含有NO的原因之一;在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图所示,根据图象判断反应N2(g)+O2(g)═2NO(g)的△H__________ 0(填“>”或“<”)。

(3)NOx是汽车尾气中的主要污染物之一。汽车发动机工作时会引起N2和O2反应,其能量变化如图所示,写出该反应的热化学方程式_____________________;

-
一定温度下(T2>T1),在3个体积均为2.0L的恒容密闭容器中反应2NO(g)+Cl2(g)= 2ClNO(g) (正反应放热)达到平衡,下列说法正确的是
| 容器 | 温度/ (℃) | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/ mol·L-1 |
| c(NO) | c(Cl2) | C(ClNO).v | C(ClNO) |
| Ⅰ | T1 | 0.20 | 0.10 | 0 | 0.04 |
| Ⅱ | T2 | .020 | 0.10 | 0.20 | cl |
| Ⅲ | T3 | 0 | 0 | 0.20 | C2 |
A. 达到平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1:2
B. 达到平衡时,容器Ⅲ中ClNO的转化率小于80%
C. 达到平衡时,容器Ⅱ中c(ClNO)/C(NO)比容器Ⅰ中的大
D. 若温度为T1,起始时向同体积恒容密闭容器中充入0.20molNO(g).、0.2mo1Cl2(g)和0.20molClNO(g),则该反应向正反应方向进行
-
一定温度下(T2> Tl),在3个体积均为2.0 L的恒容密闭容器中反应 2NO(g)+ Cl2(g) = 2ClNO(g)(正反应放热)达到平衡,下列说法正确的是
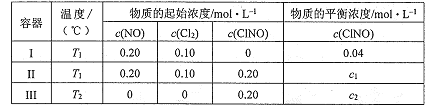
A. 达到平衡时,容器I与容器II中的总压强之比为1:2
B. 达到平衡时,容器III中ClNO的转化率小于80%
C. 达到平衡时,容器II中c(ClNO(/ c(NO)比容器I中的大
D. 若温度为Tl,起始时向同体积恒容密闭容器中充入0.20 mol NO(g)、0.2 mol Cl2(g)和0.20 mol ClNO(g),则该反应向正反应方向进行
2NOCl(g),在温度分别为T1、T2时测得NO的物质的量与时间的关系如表所示,正确的是






