-
下列表示物质分子式的是( )
A.SiO2 B.Na2SO4 C.P(红磷) D.C60 (足球烯)
难度: 简单查看答案及解析
-
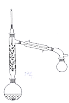
实验室模拟石油的分馏实验中,不需要用到的仪器是( )
A.
 B.
B.C.
 D.
D.
难度: 简单查看答案及解析
-
下列物质在熔融状态(液态)条件下,有较强导电能力的是( )
A.聚乙烯 B.苯酚 C.硫酸 D.醋酸钠
难度: 简单查看答案及解析
-
是优良的水处理剂,一种制备方法是将
、
、
混合共熔,反应为
,下列关于该反应的说法不正确的是( )
A.铁元素被氧化,氮元素被还原
B.
是氧化产物,
是还原产物
C.
在酸性条件下不稳定,会迅速分解并生成氢气
D.
具有强氧化性,因而有杀菌作用
难度: 中等查看答案及解析
-
下列物质的名称正确的是( )
A.
:硫氨 B.
:银氨离子
C.
:硬酯酸甘油酯 D.
:2-甲基-1-丙醇
难度: 简单查看答案及解析
-
下列有关化学用语的表示正确的是( )
A.过氧化钠的电子式:
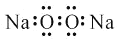 B.乙烯的球棍模型
B.乙烯的球棍模型C.硫离子的结构示意图:
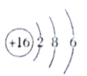 D.甲酸甲酯的结构简式:
D.甲酸甲酯的结构简式:难度: 中等查看答案及解析
-
下列说法正确的是( )
A.C7H16与甲烷必互为同系物
B.
与
互为同分异构体
C.1H、2H、3H互为同位素,实际上是同一种核素
D.12C和14C互为同素异形体,后者可用于考古研究
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.纯碱可作化工原料,也是治疗胃酸过多的一种药剂
B.硝酸是一种重要的化工原料,可用来制造化肥、染料、炸药等
C.NaClO溶液有消毒作用,加入适量醋酸可以增强其消毒作用
D.贮氢合金的发现和应用,开辟了氢气贮存、运输的新途径
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.实验室制备氢氧化铁胶体时,采用的方法是向沸水中滴加硫酸铁溶液
B.工业硝酸呈黄色的原因是混有铁离子
C.制硫酸工业生产中,尾气中含有的二氧化硫可用亚硫酸钠溶液吸收
D.2CaSO4•H2O是生石膏,可用作制作石膏绑带
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.植物进行光合作用时,将光能转化为化学能
B.以原油作为原料,经过裂化工艺可提高轻质油产量和质量
C.工业上,可用淀粉、纤维素为原料生产葡萄糖
D.煤的气化、液化和干馏均发生化学变化
难度: 简单查看答案及解析
-
下列有关实验说法中,正确的是( )
A.氯酸钾、高锰酸钾结块时,可放在研钵中先敲击成小块,再研碎
B.用滴定法进行定量测定时,基准物应该具有性质稳定、相对分子质量较小等特点
C.除去NaCl晶体中的少量KNO3时,主要步骤包括:加热溶解、蒸发、冷却结晶、过滤、洗涤、干燥
D.不慎将苯酚沾到皮肤上时,应立即用酒精洗涤,再用水冲洗
难度: 中等查看答案及解析
-
下列有关物质用途的说法,不正确的是( )
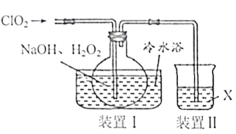
A.ClO2具有强氧化性,可用于自来水的杀菌消毒
B.氮肥包括铵态氮肥、硝态氮肥和尿素
C.电解法冶炼铝时,加入冰晶石可降低氧化铝熔融温度,减少能耗
D.生物炼铜,是指在某些细菌作用下,利用空气中的氧气将不溶性铜矿转化为铜单质
难度: 中等查看答案及解析
-
能正确表示下列变化的离子方程式是( )
A.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶【解析】
B.用铝粉和
溶液反应制取少量H2:
C.四氧化三铁溶于稀硝酸:
D.漂白粉溶液中通入足量SO2:
难度: 中等查看答案及解析
-
下图所示的某聚酰胺树脂是飞机材料中的一种,具有较好的耐热性、耐水性。则下列说法不正确的是( )
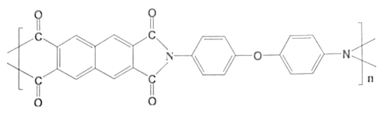
A.该树脂材料可通过缩聚反应合成
B.该树脂能使溴水褪色
C.该树脂中所有碳原子不可能在同一平面上
D.合成该树脂单体可以是
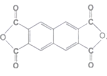 和
和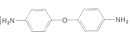
难度: 困难查看答案及解析
-
下列说法正确的是( )
A.核外电子的排布应优先排布在能量最低的电子层
B.对于主族元素而言,若最外层电子数为m,电子层数为n,则
值越大,金属性越强
C.同一周期中,随着核电荷数的增加,阴离子半径逐渐增大
D.第三、四周期中,同族元素原子的核电荷数相差一定为8
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.常温下,pH=7的溶液不一定是纯水
B.常温下,某氨水pH=x,某盐酸pH=14-x,两者等体积混合后,pH>7
C.相同温度下,pH相等的盐酸、CH3COOH溶液中,c(CH3COO-)= c(Cl-)
D.氨水和硫酸反应后的溶液,若溶液呈中性,则c(
)=c(
)
难度: 中等查看答案及解析
-
“三室法”制备烧碱和硫酸示意图如下,下列说法正确的是( )

A.电极A为阳极,发生氧化反应
B.离子交换膜A为阴离子交换膜
C.稀硫酸从c处进,浓
溶液从b处出,浓
溶液从e处进
D.
和
迁移的数量和等于导线上通过电子的数量
难度: 中等查看答案及解析
-
一定温度下,可逆反应:
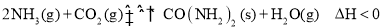 在某密闭容器中达到平衡,下列说法不正确的是
在某密闭容器中达到平衡,下列说法不正确的是A.

B.
,反应达到平衡,升高温度,有利于平衡逆移
C.
,若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大
D.
,在密闭容器中达到平衡,混合气体的平均相对分子质量不变,则反应一定达到平衡
难度: 中等查看答案及解析
-
设
为阿伏加德罗常数的值。下列说法不正确的是( )
A.
与过量浓硝酸反应,收集到
气体(标准状况),则被还原的硝酸的数目是0.06NA
B.常温常压下,
的乙二酸溶液中,总的离子数目大于0.15NA
C.常温常压下,
与足量
反应,共生成
转移电子的数目为0.4NA
D.含
与
共
的溶液中,N(
)+N
)+N(H2CO3)=NA
难度: 中等查看答案及解析
-
化学反应
在四个不同条件下进行。B、D起始为0,反应物A的浓度
随反应时间
变化情况如下表:
实验序号
时间
浓度
温度
0
10
20
30
40
50
60
1
800℃
1.0
0.8
0.67
0.57
0.50
0.50
0.50
2
800℃
0.8
0.67
0.57
0.50
0.50
0.50
3
800℃
0.92
0.75
0.63
0.60
0.60
0.60
4
820℃
1.0
0.40
0.25
0.20
0.20
0.20
0.20
下列说法不正确的是( )
A.实验1,反应在10至
内
B.实验2,A的初始浓度
,还隐含的条件是加入了催化剂
C.实验3的反应速率v3<实验1的反应速率v1
D.比较实验4和实验1,可推测该反应为吸热反应
难度: 中等查看答案及解析
-
NO氧化反应:
分两步进行,其反应过程能量变化示意图如图,下列说法不正确的是( )
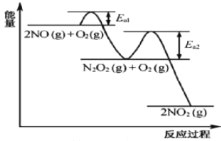
I.
∆H1;II.
∆H2
A.由于
,决定化学反应速率快慢的是反应Ⅱ
B.图示过程中,反应物断键吸收能量小于生成物形成所释放的能量
C.升高温度,2NO(g)+O2(g)
2NO2(g)反应速率一定加快
D.其它条件不变,升高温度,
平衡一定逆向移动
难度: 困难查看答案及解析
-
已知
,25℃时,
的
。该温度下用
溶液滴定
溶液的滴定曲线如图所示。下列说法不正确的是( )
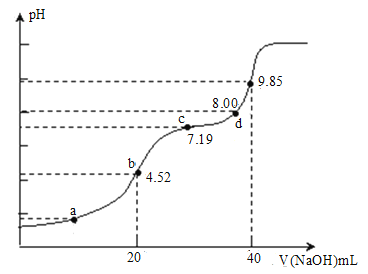
A.若a点溶液c(
)=c(H2SO3),则a点对应的
B.若选择b为反应终点,宜选择甲基橙为指示剂
C.c点对应的溶液2c(Na+)=3c(
)
D.d点对应的溶液c(Na+)>c(
)>c(
)>c(OH-)>c(H+)
难度: 困难查看答案及解析
-
作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。
溶于
溶液能发生
的反应,在低温条件下,可制得
。下列说法不正确的是( )
A.其他条件相同的情况下,
在
溶液中的溶解度大于在水中的溶解度
B.向
溶液中加入淀粉溶液,溶液变蓝色
C.
代替
作为加碘剂,可以减少碘的损失
D.由于还原性
,加入
可以提高加碘盐(添加
)的稳定性
难度: 中等查看答案及解析
-
某固体混合物X,含有NaClO3、KCl、NaOH、ZnSO4、NaAl(OH)4和NaNO2中的几种,进行如下实验:①X溶于水,得到溶液Y;②溶液Y先加入过量稀HNO3酸化,再加入AgNO3溶液,得到白色沉淀W,下列说法不正确的是( )
A.混合物X中可能含有KCl
B.向溶液Y中滴加盐酸,若产生白色沉淀,说明X中一定含有NaAl(OH)4
C.向溶液Y中滴加盐酸,若产生红棕色的气体,说明X中一定含有NaNO2
D.取X溶液进行焰色反应,透过蓝色钴玻璃片没有观察到紫色火焰,说明X中一定含有NaClO3
难度: 困难查看答案及解析
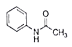 +H2O
+H2O