-
下列常见实验的现象或表述正确的是( )
A. 向某溶液中加入2滴KSCN溶液,溶液不显血红色,再向溶液中加入几滴新制的氯水,溶液变为血红色,该溶液中一定含有Fe2+
B. 为检验红砖中铁的价态,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液变为血红色,说明红砖中只有三氧化二铁
C. 制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁
D. 将(NH4)2Fe(SO4)2·6H2O试样溶于稀硝酸中,滴加KSCN溶液,出现血红色,说明检验前该试样已变质
难度: 困难查看答案及解析
-
根据元素周期律,由下列事实进行归纳推测,推测不合理的是
选项
事实
推测
A
Mg与冷水较难反应,Ca与冷水较易反应
Be(铍)与冷水更难反应
B
Na与Cl形成离子键,Al与Cl形成共价键
Si与Cl形成共价键
C
HCl在1500℃时分解,HI在230℃时分解
HBr的分解温度介于二者之间
D
Si是半导体材料,同族的Ge是半导体材料
ⅣA族元素的单质都是半导体材料
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关C、N、S等非金属元素化合物的说法正确的是( )
A.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
B.SO2具有漂白性可以使酸性高锰酸钾溶液褪色
C.实验室可用NaOH溶液处理NO2和SO2废气
D.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
难度: 中等查看答案及解析
-
化学与生活密切相关。下列说法错误的是
A.煤燃烧时加入适量石灰石,可减少SO2的排放
B.泡沫灭火器可用于一般的起火,也适用于电器起火
C.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
D.铵态氮肥不宜跟碱性物质如草木灰混合使用
难度: 中等查看答案及解析
-
当航天飞机返回地球大气层时,由于与空气的剧烈摩擦,飞机尖端的温度可达1000℃以上,为了防止高温将其烧毁,科学家给航天飞机的相应部位安装了可靠的保护层。制作保护层的材料是
A.塑料 B.玻璃
C.新型陶瓷 D.镁铝合金
难度: 简单查看答案及解析
-
下列说法正确的是
A.浓硫酸使蓝矾晶体变为白色粉末,表现了浓硫酸的吸水性
B.将某气体通入品红溶液,品红溶液褪色,该气体一定是SO2
C.工业上用铝槽车装运浓硫酸是由于铝不与浓硫酸发生反应
D.铵盐中氮元素均为-3价
难度: 中等查看答案及解析
-
环保型燃料——丙烷燃烧时发生反应的化学方程式为C3H8+5O2
3CO2+4H2O。下列说法中不正确的是
A.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料
B.所有的燃烧反应都会释放热量
C.1 mol C3H8和5 mol O2所具有的总能量大于3 mol CO2和4 mol H2O所具有的总能量
D.燃烧时化学能只转化为热能
难度: 中等查看答案及解析
-
下列解释事实的方程式不正确的是
A.实验室配制酸性高锰酸钾溶液不用盐酸:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O
B.用熟石灰处理泄漏的液氯:2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
C.足量铁粉与稀硝酸反应:Fe+4H++NO3-=Fe3++2H2O+NO↑
D.用氨水除去烟气中的SO2:SO2+2NH3·H2O=(NH4)2SO3+H2O
难度: 中等查看答案及解析
-
下列有关能量变化的说法中错误的是( )
A.若反应物的总能量高于生成物的总能量,则该反应是吸热反应
B.1 mol石墨转化为金刚石,要吸收 1.895 kJ的热能,则石墨比金刚石稳定
C.化学变化中的能量变化主要由化学键的变化引起的
D.化学变化必然伴随发生能量变化
难度: 中等查看答案及解析
-
已知反应A+B==C+D的能量变化如图所示,下列说法正确的是( )
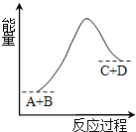
A.该反应为放热反应 B.该反应为吸热反应
C.反应物的总能量高于生成物的总能量 D.该反应只有在加热条件下才能进行
难度: 简单查看答案及解析
-
下列各装置能构成原电池的是
A.
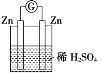 B.
B.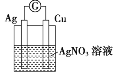
C.
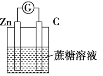 D.
D.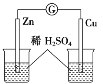
难度: 简单查看答案及解析
-
如图所示,a在金属活动性顺序中排在氢之前,b为碳棒,下列说法中不正确的是

A.a极上发生还原反应,b极上发生氧化反应
B.碳棒上有气体逸出
C.导线上有电流,电子移动方向为a→b
D.反应后a极质量减小
难度: 中等查看答案及解析
-
下列叙述正确的是
①两种原子构成的分子中的化学键都是极性键
②两种不同非金属元素原子间形成的化学键都是极性键
③含有非极性键的化合物一定是共价化合物
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤难失去电子的原子,易形成阴离子
⑥单质分子中不存在化学键,化合物的分子中才存在化学键
⑦离子化合物中一定含有离子键
A.③⑤⑥ B.①⑦ C.②⑦ D.只有①⑤⑦
难度: 中等查看答案及解析
-
下列各组反应(表中物质均为反应物)中,反应刚开始时放出H2的速率最大的是
选项
金属(粉末状)/mol
体积/mL
酸浓度/mol·L-1
酸
反应温度/℃
A
Mg
0.1
10
6
HNO3
60
B
Mg
0.1
10
3
HCl
60
C
Fe
0.1
10
3
HCl
60
D
Mg
0.1
10
3
H2SO4
60
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
以下物质间的每步转化不能通过一步反应实现的是( )
A.C→CO→CO2→Na2CO3
B.S→SO3→H2SO4→Na2SO4
C.Fe→FeCl2→FeCl3→Fe(OH)3
D.N2→NO→NO2→HNO3
难度: 中等查看答案及解析
-
将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即产生电流,称为甲烷燃料电池。下列有关说法中错误的是
A.CH4在负极上反应,O2在正极上反应
B.放电过程中电解质溶液的碱性减弱
C.此电池属于环境友好型电池
D.此电池中化学能100%转化为电能
难度: 中等查看答案及解析
-
根据国外媒体报道,某公司将推出一种全新的银锌电池,这种银锌电池的续航能力要比锂离子电池强,有望取代锂离子电池。其放电过程可表示为Ag2O+Zn=ZnO+2Ag,此电池放电时,有关说法正确的是
A.电能转化为化学能
B.电解质溶液是稀硫酸
C.电子通过外电路从Ag2O极流向Zn极
D.Zn作负极被氧化
难度: 简单查看答案及解析
-
对于反应4A+2B
3C,下列说法中正确的是
A. 某温度时,化学反应速率无论用A. B. C中任何物质表示,其数值都相同
B. 其他条件不变时,降低温度,化学反应速率减小
C. 其他条件不变时,增大压强,化学反应速率一定加快
D. 若增大或减小A的物质的量,化学反应速率一定会发生明显的变化
难度: 中等查看答案及解析
-
在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应:A(s)+3B(g)
2C(g)+D(g) 已达平衡状态的是
A.混合气体的压强 B.混合气体的密度
C.B和C的物质的量浓度相等 D.气体的总物质的量
难度: 简单查看答案及解析
-
将1.92 g铜跟适量的浓硝酸反应,铜全部作用后,共收集到1.12 L标准状况下的气体(假设只有NO2、NO),则反应消耗的硝酸的物质的量可能是
A.0.11 mol B.0.1 mol C.0.09 mol D.0.08 mol
难度: 中等查看答案及解析





