-
在120℃时,1体积甲烷和丁烯的混合物与4体积O2在密闭容器中充分燃烧,只生成水和二氧化碳,反应后恢复到原温度,压强增加为原来的1.1倍,则混合气体中丁烯的体积分数是( )
A. 9 5% B. 50% C. 40% D. 20%
难度: 困难查看答案及解析
-
将a g聚苯乙烯树脂溶于bL苯中,然后通入c mol乙炔气体,所得混合液中碳氢两元素的质量比是( )
A.6︰1 B.12︰1 C.8︰3 D.1︰2
难度: 中等查看答案及解析
-
有关下列说法中,正确的是
A.用标准盐酸滴定未知浓度的NaOH溶液,滴定前酸式滴定管尖嘴有气泡未排出,滴定后气泡消失,会造成测定结果偏低
B.工业废水中的Cu2+、Hg2+等重金属阳离子可以通过加入FeS除去
C.工业上常在铁板表面镀上一层锡(俗称马口铁)来防止铁板表面破损后发生电化学腐蚀
D.等体积的pH均为2的酸HA和HB的溶液分别与足量的铁粉反应,HA放出的H2多,说明HA酸性强
难度: 困难查看答案及解析
-
以下物质:①甲烷 ②苯 ③聚乙烯 ④聚乙炔 ⑤2丁炔 ⑥环己烷 ⑦邻二甲苯 ⑧苯乙烯。既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
A.③④⑤⑧ B.④⑤⑦⑧ C.④⑤⑧ D.③④⑤⑦⑧
难度: 中等查看答案及解析
-
下列各项叙述中,正确的是( )
A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素
C.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同
D.24Cr原子的电子排布式是1s22s22p63s23p63d44s2
难度: 中等查看答案及解析
-
有机物分子中原子(或原子团)之间的相互影响会导致它们化学性质的改变,下列叙述能说明上述观点的是( )
A.等物质的量的乙二醇和乙醇分别与足量金属钠反应,乙二醇产生的氢气多
B.乙烯可发生加成反应,而乙烷不能
C.甲苯能使酸性高锰酸钾溶液褪色,甲基环己烷不能使酸性高锰酸钾溶液褪色
D.乙烯和苯都能和氢气发生加成反应
难度: 中等查看答案及解析
-
下列有关物质的表达式正确的是( )
A.乙炔分子的比例模型:
B.溴乙烷的电子式:
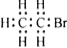
C.2-氯丙烷的结构简式: CH3CHClCH3 D.丙烯的键线式:
难度: 中等查看答案及解析
-
有机物分子
中最多有多少个原子共面( )
A.12 B.16 C.20 D.24
难度: 中等查看答案及解析
-
美国康乃尔大学的威考克斯(C·Wilcox)所合成的一种有机分子就像一尊释迦牟尼佛像,因而称为释迦牟尼分子(分子中所有原子均在同一平面)如图。对于该有机物的叙述正确的是
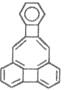
①该有机物属于芳香烃;②该有机物的分子式为C22H12; ③该有机物能发生加成反应;④该有机物的一氯代物的同分异构体有6种
A.①③④ B.①② C.②③ D.①②③④
难度: 困难查看答案及解析
-
下列有关同分异构体数目的叙述错误的是( )
A.丙烷的一氯代物有 2 种,丙烷的二氯代物有 4 种
B.分子式为 C7H8O 且属于芳香族化合物的同分异构体有 5 种
C.联苯
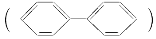 的一氯代物有 3 种,二氯代物有 12 种
的一氯代物有 3 种,二氯代物有 12 种D.
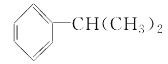 与 Cl2 在光照条件下的取代产物有 3 种
与 Cl2 在光照条件下的取代产物有 3 种难度: 困难查看答案及解析
-
已知分子式为C12H12的物质A的结构简式如图所示,A苯环上的四溴代物的同分异构体的数目有
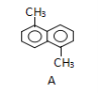
A. 9种 B. 10种 C. 11种 D. 12种
难度: 困难查看答案及解析
-
烷烃
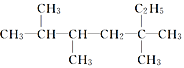 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有A.4种 B.5种 C.6种 D.7种
难度: 简单查看答案及解析
-
符合分子式“C6H6”的多种可能结构如图所示,下列说法正确的是
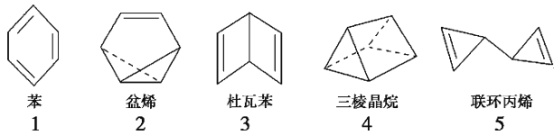
A. 1~5对应的结构中能使溴的四氯化碳溶液褪色的有4个
B. 1~5对应的结构中一氯取代物只有1种的有3个
C. 1~5对应的结构中所有原子均可能处于同一平面的有1个
D. 1~5对应的结构均能与氢气在一定条件下发生加成反应
难度: 困难查看答案及解析
-
下列有关说法错误的是( )
A.三联苯(
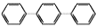 )的一氯代物有 4 种
)的一氯代物有 4 种B.立方烷(
)经硝化可得到六硝基立方烷,其可能的结构有 3 种
C.β-月桂烯(
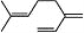 )与溴发生 1:1 加成反应,产物(不考虑顺反异构)有 3 种
)与溴发生 1:1 加成反应,产物(不考虑顺反异构)有 3 种D.
的一溴代物和
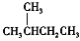 的一溴代物都有 4 种(不考虑立体异构)
的一溴代物都有 4 种(不考虑立体异构)难度: 困难查看答案及解析
-
下列文字表述与反应方程式对应且正确的是( )
A.溴乙烷中滴入 AgNO3 溶液检验其中的溴元素:Br-+Ag+=AgBr↓
B.用醋酸除去水垢:CaCO3+2H+=Ca2++CO2↑+H2O
C.甲苯与浓硝酸和浓硫酸的混合物反应:
3HNO3
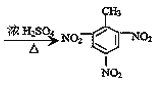 +3H2O
+3H2OD.实验室用液溴和苯制溴苯:

难度: 中等查看答案及解析
-
下列有关实验操作的叙述和与实验得出的相应结论都正确的是( )
实验操作
结论
①
实验室用电石与饱和食盐水在启普发生器中制乙炔常会闻到臭味
乙炔是无色、略有臭味的气体
②
乙醇、浓硫酸混合加热170℃,导出的物质能使酸性高锰酸钾褪色
该反应生成了乙烯
③
在溴乙烷中加入适量的氢氧化钠溶液,加热一段时间,再滴入几滴硝酸银,会有沉淀析出
溴乙烷在碱性条件下能水解出Br-
④
提纯粗苯甲酸用重结晶法,主要步骤为:加热溶解、趁热过滤、冷却结晶、过滤、洗涤
苯甲酸在水中的溶解度受温度的影响很大
⑤
苯不能与酸性高锰酸钾反应,而甲苯却能
苯环使甲基活化
A. ④⑤ B. ②④ C. ①②④ D. ③④⑤
难度: 中等查看答案及解析
-
下列关于有机物说法正确的是( )
A.CH3Cl、
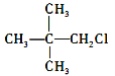 、
、中加入 NaOH 的醇溶液共热,然后加入稀硝酸呈酸性,再滴入 AgNO3 溶液,均有沉淀生成
B.CH3Cl 中加入 NaOH 的水溶液共热,再滴入 AgNO3溶液,可检验该物质中含有的卤素原子
C.
发生消去反应得到两种烯烃
D.
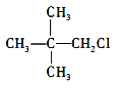 与 NaOH 的水溶液共热,反应后生成的醇能被氧化为醛
与 NaOH 的水溶液共热,反应后生成的醇能被氧化为醛难度: 困难查看答案及解析
-
中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主要过程如下图所示。

已知:几种物质中化学键的键能如下表所示。
化学键
H2O中H—O键
O2中O=O 键
H2中H—H键
H2O2中O—O键
H2O2中O—H键
键能kJ/mol
463
496
436
138
463
若反应过程中分解了2 mol水,则下列说法不正确的是
A. 总反应为2H2O
2H2↑+O2↑
B. 过程I吸收了926 kJ能量
C. 过程II放出了574 kJ能量
D. 过程Ⅲ属于放热反应
难度: 中等查看答案及解析
-
将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应2A(g) + B(g)
xC(g) + 2D(g),经4min后达平衡,测得D的浓度为1.0 mol·L-1,c(A) : c(B)=2 : 3,以C表示的平均速率υ(C)=0.125 mol·L-1·min-1,下列说法不正确的是
A. 反应速率υ(A)=0.25 mol·L-1·min-1
B. 该反应方程式中,x=1
C. 4 min时,B的物质的量为2 mol
D. 该反应的平衡常数K=1/3
难度: 中等查看答案及解析
-
—定条件下,向一带活塞的密闭容器中充入2 molSO2和1molO2,发生反应2SO2(g)+O2(g)
2SO3(g),达到平衡后改变下述条件,平衡时SO3气体的质量百分数不改变的是
A. 保持温度和容器体积不变,充入1mol SO3(g)
B. 保持温度和容器内压强不变,充入1mol SO3(g)
C. 保持温度和容器内压强不变,充入1mol O2(g)
D. 保持温度和容器内压强不变,充入1mol Ar(g)
难度: 困难查看答案及解析
-
下列有关电解质溶液的说法正确的是
A. 向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小
B. 将CH3COONa溶液从20 ℃升温至30 ℃,溶液中c(CH3COO-)/c(CH3COOH)∙c(OH-)增大
C. 向盐酸中加入氨水至中性,溶液中
>1
D. 常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液pH<7
难度: 困难查看答案及解析
-
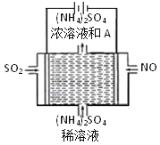
一种熔融碳酸盐燃料电池原理示意如图。有关该电池的说法正确的是( )
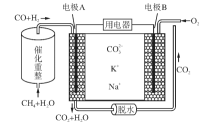
A. 反应CH4+H2O
3H2+CO,每消耗1 molCH4转移12 mol电子
B. 电极B上发生的电极反应:O2+2CO2+4e-=2CO32-
C. 电池工作时,CO32-向电极B移动
D. 电极A上H2参与的电极反应:H2+2OH--2e-=2H2O
难度: 困难查看答案及解析
-
下列描述中正确的是
A. CS2为V形的极性分子
B. ClO3—的空间构型为平面三角形
C. SF6中有6对相同的成键电子对
D. SiF4和SO32—的中心原子均为sp2杂化
难度: 中等查看答案及解析
-
有关晶体的结构如图所示,下列说法中不正确的是( )
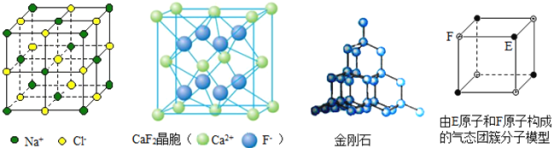
A.在NaCl晶体中,距Na+最近的Cl-有6个
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D.该气态团簇分子的分子式为EF或FE
难度: 中等查看答案及解析
-
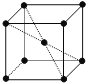
金属钠晶体为体心立方晶胞,实验测得钠的密度为ρ(g·cm-3)。已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性小球且处于体对角线上的三个球相切。则钠原子的半径r(cm)为( )
A.
B.
C.
D.
难度: 困难查看答案及解析
 CH2=CH2+H2O
CH2=CH2+H2O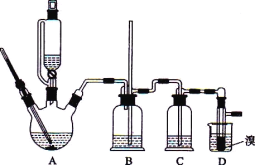
 两种不 同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_________)
两种不 同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_________)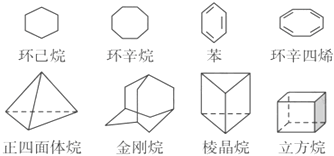
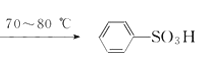 +H2O
+H2O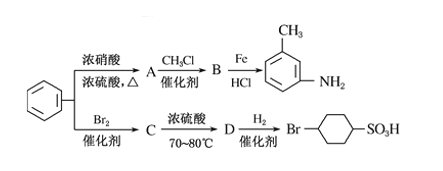
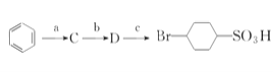 ”的所有反应中属于取代反应的是________(填字母),属于加成反应的是_____(填字母)。
”的所有反应中属于取代反应的是________(填字母),属于加成反应的是_____(填字母)。