-
改革开放四十年来,我国在很多领域取得了举世瞩目的成就,下列工程使用的部分材料如下所示,其中属于有机高分子的是
A.
 港珠澳大桥桥墩——混凝土
港珠澳大桥桥墩——混凝土B.
 “人造太阳”核聚变实验装置——钨合金
“人造太阳”核聚变实验装置——钨合金C.
 高铁轨道与地基之间填隙减震——聚氨酯
高铁轨道与地基之间填隙减震——聚氨酯D.
 “玉兔”月球车太阳能电池帆板——硅
“玉兔”月球车太阳能电池帆板——硅难度: 中等查看答案及解析
-
下列有关化学与生活的说法中正确的是
A.苯甲酸钠和亚硝酸钠是常见的食品防腐剂
B.Na2CO3和Ca(OH)2常用作抗酸药
C.我国目前的加碘盐中添加的是KI
D.柠檬和苹果都是酸性食物
难度: 简单查看答案及解析
-
下列反应中,反应物总能量低于生成物总能量的是
A.金属铝与稀盐酸反应 B.甲烷在空气中燃烧
C.盐酸与氢氧化钠溶液反应 D.氯化铵与Ba(OH)2·8H2O固体反应
难度: 简单查看答案及解析
-
下列化学用语不正确的是
A.羟基的电子式:
B.丙酸乙酯的分子式:C5H10O2
C.葡萄糖的实验式:C6H12O6 D.乙炔分子的球棍模型:
难度: 简单查看答案及解析
-
下列物质不能与银氨溶液反应生成银镜的是
A.葡萄糖 B.蔗糖 C.甲酸甲酯 D.乙醛
难度: 简单查看答案及解析
-
下列各组物质中,不能用溴水鉴别的是
A.苯和乙醇 B.乙烯和甲醛 C.甲苯和苯乙烯 D.乙烷和乙炔
难度: 中等查看答案及解析
-
下列分子式表示的物质一定是纯净物的是
A.C5H10 B.C7H8O
C.CH4O D.C2H4Cl2
难度: 中等查看答案及解析
-
下列各物质中含有的少量杂质,不能用“加入NaOH溶液,分液”的方法除去的是
A.溴苯中的溴 B.苯中的苯酚
C.硝基苯中的硝酸 D.乙酸乙酯中的乙酸
难度: 中等查看答案及解析
-
核磁共振氢谱有2组峰,且峰面积比为3:2的化合物是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列关于营养物质的说法中不正确的是
A.油脂制肥皂的原理是油脂发生碱性水解
B.碘酒可用于杀菌消毒是因为它能使蛋白质变性
C.鸡蛋清溶液中加入醋酸铅溶液,会因为盐析而沉淀
D.淀粉为人体提供能量,是因为淀粉水解生成葡萄糖,葡萄糖氧化释放能量
难度: 中等查看答案及解析
-
下列烷烃中,与
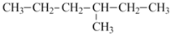 互为同分异构体的是
互为同分异构体的是A.2,3-二甲基丁烷 B.2,2,3-三甲基丁烷
C.2-甲基丁烷 D.2,2,3,3-四甲基丁烷
难度: 简单查看答案及解析
-
下列热化学方程式中,能表示可燃物的燃烧热的是
A.CO(g) +1/2O2 (g) = CO2 (g) ΔH =-283.0 kJ/mol
B.C(s) + 1/2O2 (g) = CO(g) ΔH =-110.5 kJ/mol
C.H2(g)+1/2O2(g) = H2O(g) ΔH =-241.8 kJ/mol
D.2C8H18(l)+25O2(g) = 16CO2(g)+18H2O(l) ΔH =-11036 kJ/mol
难度: 中等查看答案及解析
-
下列说法正确的是
A.3-戊醇和2-甲基-2-丁醇互为同系物
B.顺-2-丁烯和反-2-丁烯的加氢产物不同
C.CH2=C(CH3)2的名称是2-甲基-2-丙烯
D.沸点:1-丁醇>戊烷>2-甲基丁烷
难度: 中等查看答案及解析
-
下列装置或操作不能达到实验目的的是
A.
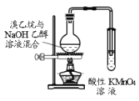 检验溴乙烷发生消去反应的产物
检验溴乙烷发生消去反应的产物B.
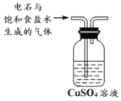 除去乙炔中的硫化氢
除去乙炔中的硫化氢C.
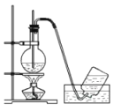 实验室制取乙烯
实验室制取乙烯D.
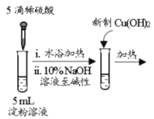 检验淀粉水解产物
检验淀粉水解产物难度: 中等查看答案及解析
-
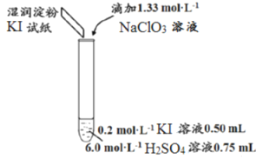
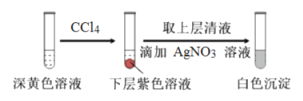
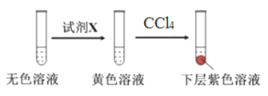
某学习小组按如下实验过程(固定、加热及盛接仪器略)证明了海带中存在碘元素:

下列说法不正确的是
A.步骤①需要将干海带放入坩埚中灼烧
B.步骤②反应的离子方程式为:2I-+2H++H2O2=I2+2H2O
C.步骤③操作后,观察到试管中溶液变为蓝色,可以说明海带中含有碘元素
D.若步骤③加入的试剂是CCl4,振荡、静置后,液体分层,上层紫色,下层无色
难度: 中等查看答案及解析
-
下列说法正确的是
A.酚醛树脂的结构简式为

B.高聚物
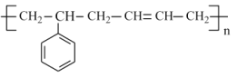 由3种单体加聚得到
由3种单体加聚得到C.n
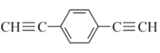 →
→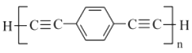 +(n-1)H2是加聚反应
+(n-1)H2是加聚反应D.1mol
 在碱性条件下完全水解,消耗n mol NaOH
在碱性条件下完全水解,消耗n mol NaOH难度: 中等查看答案及解析
-
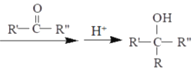
酸与醇发生酯化反应的过程如下,下列说法正确的是
R—O—H+R'—COOH

R'—COOR+H2O
A.①的反应类型是取代反应
B.②的反应类型是消去反应
C.若用R18OH作反应物,产物可得H218O
D.酯化过程中,用稀硫酸做催化剂
难度: 中等查看答案及解析
-
反应N2(g)+O2(g)=2NO(g)的能量变化如图所示:

已知:断开1mol N2(g)中化学键需吸收946kJ能量,断开1mol O2(g)中化学键需吸收498kJ能量。下列说法正确的是
A.断开1mol NO(g)中化学键需要吸收632kJ能量
B.NO(g)=
N2(g)+
O2(g) ∆H=+90kJ/mol
C.N2(g)+O2(g)=2NO(g) ∆H=-180kJ/mol
D.形成1mol NO(g)中化学键时释放90kJ能量
难度: 中等查看答案及解析
-
下列“烧杯中的物质”和“向烧杯中分别加入的试剂”不能完成“实验目的”的是
①
②
实验目的
烧杯中的物质
向烧杯中分别加入的试剂
A
醋酸的酸性强于苯酚
①醋酸 ②苯酚溶液
碳酸氢钠溶液
B
羟基对苯环的活性有影响
①苯 ②苯酚溶液
饱和溴水
C
甲基对苯环的活性有影响
①苯 ②甲苯
酸性高锰酸钾溶液
D
乙醇羟基中的氢原子不如水分子中的氢原子活泼
①水 ②乙醇
金属钠
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列说法不正确的是
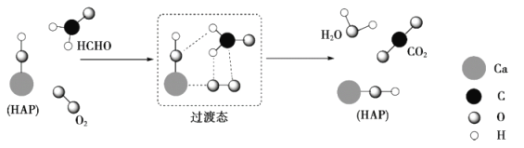
A.HAP能提高HCHO与O2的反应速率
B.根据图示信息,CO2分子中的氧原子全部来自O2
C.HCHO在反应过程中,有C-H键发生断裂
D.该反应可表示为: HCHO+O2
CO2+H2O
难度: 中等查看答案及解析
-
有机物A的结构简式如图所示,下列有关该物质的说法不正确的是
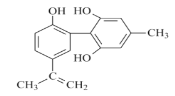
A.A分子中的所有碳原子可能共平面
B.1mol A与碳酸钠溶液反应,最少消耗1.5mol Na2CO3
C.向A中滴入酸性KMnO4溶液,紫色褪去,不能证明A的结构中存存碳碳双键
D.1mol A分别与浓溴水和H2反应,最多消耗的Br2和H2的物质的量分别为4mol、7mol
难度: 中等查看答案及解析
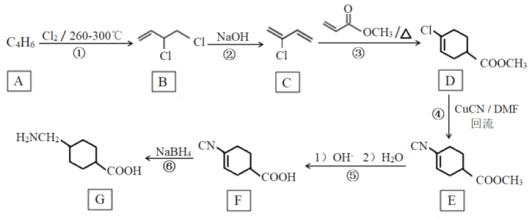

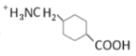
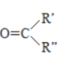
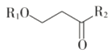
 (R、R'、R〃代表烃基或氢)
(R、R'、R〃代表烃基或氢)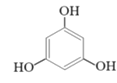 +2CH3OH
+2CH3OH +2H2O
+2H2O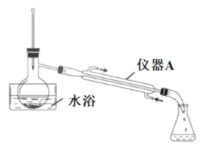
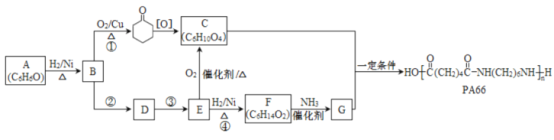

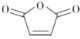 是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。
是一种重要的化工原料,可用于合成可降解的高聚物PES树脂以及具有抗肿瘤活性的化合物K。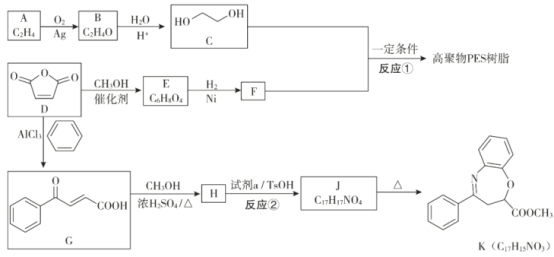
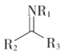 +H2O
+H2O