-
有下列仪器:①烧杯;②蒸发皿;③圆底烧瓶;④试管;⑤坩埚;⑥锥形瓶。
其中可以用酒精灯直接加热的仪器是
A.①②④⑤⑥ B.②④⑤ C.①③⑥ D.④⑥
难度: 简单查看答案及解析
-
下列实验装置一般不用于分离物质的是

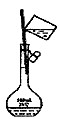

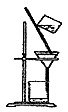
A B C D
难度: 简单查看答案及解析
-
下列说法中正确的是
A.Ag+ + Cl- = AgCl↓ 的反应属于化合反应
B.按照分散剂粒子的直径大小可将分散系分为溶液、胶体和浊液
C.可以利用丁达尔效应区分胶体和溶液
D.晶体硅是制造光导纤维的原料
难度: 中等查看答案及解析
-
下列混合物分离(或除杂)的方法正确的是
物质 杂质 药品 操作
A 溴水 NaCl 酒精 萃取
B 乙醇 醋酸 NaOH 过滤
C Na2CO3 NaHCO3 H2O 溶解、过滤
D Fe Al NaOH溶液 过滤
难度: 中等查看答案及解析
-
若NA表示阿伏加德罗常数,下列说法中错误的是
A.0.1mol/L稀硫酸中含有硫酸根离子个数为0.1NA
B.32g O2与O3混合气体中含有原子数为2NA
C.1molMg与足量N2反应生成Mg3N2失去的电子数为2NA
D.1mol H2和O2的混合气体在标准状况下的体积约为22.4L
难度: 中等查看答案及解析
-
配制100mL 1mol·L-1 NaOH溶液,若实验仪器有:①100mL量筒;②托盘天平;③玻璃棒;
④50mL容量瓶;⑤胶头滴管;⑥50mL烧杯;⑦100mL容量瓶,实验时选用仪器的先后顺序是
A.②⑦③④⑥ B.⑥②⑦③④ C.②⑥③⑦⑤ D.②⑦③⑥⑤
难度: 中等查看答案及解析
-
下列有关合金的说法中正确的是
A.青铜、硬铝和不锈钢都属于合金
B.铝合金是用量最大、用途最广的合金
C.铝合金是一种纯净物,它比纯铝的硬度大
D.Na-K合金的熔点介于Na和K熔点之间
难度: 简单查看答案及解析
-
下列物质分类的正确组合是
混合物 纯净物 单质 电解质
A 盐酸 NaOH 石墨 K2SO4溶液
B 空气 Fe(OH)3胶体 铁 Na2CO3
C CuSO4·5H2O CaCl2 水银 铜
D 氯水 KNO3晶体 O3 NaCl
难度: 中等查看答案及解析
-
已知标准状况下:①6.72L CH4 ②3.01×1023HCl ③23.1g CCl4 ④2.3g Na,下列对四种物质的
关系由小到大表示正确的是
A.体积 ④<①<②<③ B.密度 ①<④<③<②
C.原子数 ④<③<②<① D.质量 ④<①<③<②
难度: 中等查看答案及解析
-
下列离子方程式的书写正确的是
A.SiO2与NaOH溶液反应:SiO2+2Na++2OH-=Na2SiO3+ H2O
B.浓烧碱溶液中加入铝片:2Al + 2OH-+2 H2O=2AlO2-+3H2↑
C.铁和稀硝酸反应:Fe + 2H+ =Fe2+ + H 2↑
D.Cl2通入水中:Cl2 + H2O = 2H++Cl-+ClO-
难度: 中等查看答案及解析
-
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于区域3的是
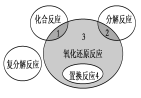
A.4Fe(OH)2+O2+2H2O=4Fe(OH)3
B.2KMnO4
K2MnO4+MnO2+O2↑
C.4NH3+5O2
4NO+6H2O
D.Fe+CuSO4=FeSO4+Cu
难度: 中等查看答案及解析
-
某溶液中含有Na+ 、CO32-、 HCO3-、 SO32-、 Cl-,在加入Na2O2后浓度不发生变化的是
A.Na+ 、CO32- B.Cl- C.CO32-、Cl- D.HCO3-、SO32-
难度: 中等查看答案及解析
-
一种盐X与氢氧化钠溶液共热,可放出气体Y,Y经过一系列氧化后再溶于水可得Z溶液,Y和Z溶液反应又生成X,则X可能是
A.NH4NO3 B.NH4Cl C.NH4HCO3 D.(NH4)2CO3
难度: 中等查看答案及解析
-
下列溶液中能用来区别SO2和CO2气体的是
①澄清的石灰水 ②氢硫酸 ③氯水 ④酸性高锰酸钾溶液 ⑤氯化钡溶液 ⑥品红溶液
A.①⑤ B.③④⑤ C.②⑥ D.②③④⑥
难度: 中等查看答案及解析
-
只用一种试剂即可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是
A. BaCl2 B. H2SO4 C. NaOH D. AgNO3
难度: 中等查看答案及解析
-
相同条件下,质量相同的NH3和CH4,下列说法正确的是
A.密度比为16:17 B.氢原子比为3:4
C.物质的量比为1:1 D.体积比为16:17
难度: 中等查看答案及解析
-
丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇碘化钾→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色
A.①②④⑤ B.②③④⑤ C.①④⑤ D.①②③④⑤
难度: 中等查看答案及解析
-
下列各组离子中,在碱性溶液中能共存,且加入硫酸过程中会产生气体和沉淀的是
A. K+ 、Na+、AlO2-、CO32- B.Na+、Cl-、SiO32-、K+
C. Na+、NO3-、AlO2-、K+ D.Na+、Cl-、HCO3-、Ba2+
难度: 中等查看答案及解析
-
下列叙述中正确的是
A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应均能生成气体
C.C、S分别在氧气中燃烧均可生成两种相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
难度: 中等查看答案及解析
-
某无色溶液中可能含有I-、K+ 、Cu2+、SO32-(还原性:SO32->I-),向该溶液中加入少量
溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-。
A.①③ B.①②③ C.②③④ D.①②
难度: 中等查看答案及解析
-
将一小块金属钠投入下列物质的水溶液中,既能生成气体,又能生成白沉淀的是
A.NH4Cl B.BaCl2 C.FeCl3 D.MgSO4
难度: 中等查看答案及解析
-
下列各物质中,不能满足“
”转化关系的一组是
X Y Z
A Si SiO2 Na2SiO3
B Fe FeCl3 FeCl2
C HCl Cl2 HClO
D H2SO4 SO2 SO3
难度: 中等查看答案及解析
-
科学的假设与猜想是科学探究的先导和价值所在。在下列假设或猜想引导下的探究肯定
没有意义的是
A.探究SO2和Na2O2可能化合生成Na2SO4
B.探究NO和N2O3可能化合生成NO2
C.探究NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3
D.探究红色酚酞试液通入Cl2褪色,原因是溶液酸碱性改变或被漂白
难度: 中等查看答案及解析
-
下列图像与对应的实验内容不相符的是


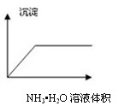
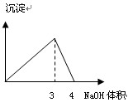
A B C D
A.在澄清石灰水中通入CO2气体至过量
B.在NaAlO2溶液中逐滴加入HCl溶液至过量
C.在AlCl3溶液中逐滴加入氨水至过量
D.在AlCl3溶液中逐滴加入NaOH溶液至过量
难度: 中等查看答案及解析
-
某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数为5.1%,300mL该溶液中氯离子的物质的量为
A.0.37mol B.0.63mol C.0.74mol D.1.5mol
难度: 中等查看答案及解析