-
(1)黄铁矿(FeS2)是制造硫酸的矿物原料,反应历程为FeS2→SO2→SO3→H2SO4,请写出
SO2制备SO3反应的化学方程式,并用双线桥标出电子转移的方向和数目 ;
(2)下列酸在与黄铁矿(FeS2)发生反应时,其中S或N元素的化合价不会发生变化的是 ;
a.稀硫酸 b.稀硝酸 c.浓硫酸 d.浓硝酸
(3)从矿物学资料查得,自然界存在反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,
该反应的氧化剂为 ,反应中转移的电子数为 NA;
(4)将(2)中反应的产物溶于水后过滤(Cu2S不溶于水和稀酸),再将滤液滴入用硫酸酸化的高锰酸钾溶液中发现溶液褪色,已知反应后锰元素呈+2价,请写出反应的化学方程式 。
高一化学填空题中等难度题查看答案及解析
-
工业上用黄铁矿(FeS2)为原料制备硫酸的流程如下:
黄铁矿(FeS2)
SO2
气体B
硫酸
关于工业制硫酸的说法不正确的是
A.煅烧时FeS2发生氧化反应 B.A可以是空气
C.步骤②产物中有SO3 D.步骤③发生了氧化还原反应
高一化学单选题简单题查看答案及解析
-
工业上用黄铁矿(FeS2)为原料制备硫酸的流程如下:

回答下列问题:
(1)在接触室中发生的反应是2SO2+O2
2SO3,该反应属于__________(填字母)
a.氧化还原反应 b.离子反应
c.化合反应 d.可逆反应
(2)Fe2O3废渣的用途有________________________(答出一条即可)。
(3)写出沸腾炉中发生反应的化学方程式:________
(4)取硫酸产品加入蔗糖中,有“黑面包”现象发生,该过程体现出浓硫酸的性质是_____。
高一化学工业流程中等难度题查看答案及解析
-
以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4∙xH2O)的工艺流程如下:
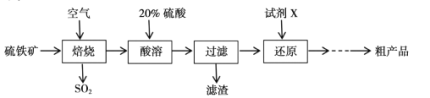
(1)已知焙烧后得到的固体主要成分为Fe2O3。写出焙烧过程主要反应的化学方程式____。
(2)写出酸溶过程主要反应的离子方程式____。
(3)试剂X是(写化学式)____。
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4∙xH2O)的操作是____
(5)利用如图装置测定FeSO4∙xH2O中结晶水含量:
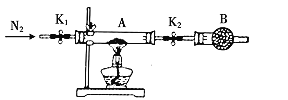
实验前通入N2,的主要目的是____,装置B中盛放的试剂是____。
高一化学工业流程中等难度题查看答案及解析
-
以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4·7H2O)的工艺流程如下:
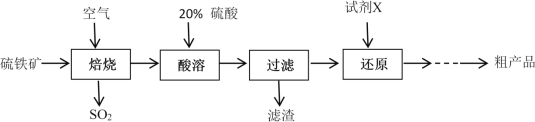
回答下列问题:
(1)焙烧后得到的固体主要成分为Fe2O3。写出焙烧过程主要反应的化学方程式____________________
(2)试剂X是(写化学式)__________________
(3)设计实验检验还原得到的溶液是否达标:_________________________________________
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4·7H2O)的操作是_______________________
(5)可以用标准浓度的酸性KMnO4溶液来测定产品中FeSO4的纯度,反应中KMnO4被还原成Mn2+。反应的离子方程式为 __________________________________
(6)某种工业品中含有FeSO4和Fe2(SO4)3。通过元素分析得知其中铁元素和硫元素的物质的量之比n(Fe)︰n(S) =1︰1.2 ,此工业品中FeSO4的物质的量分数为___________________________
高一化学填空题中等难度题查看答案及解析
-
二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义.
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:4FeS2 + 11O2
8SO2 + 2Fe2O3,该反应中被氧化的元素是_________(填元素符号)。当该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为_________L.
(2)实验室中用如图1所示的装置测定SO2催化氧化为SO3,的转化率。(已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响.)
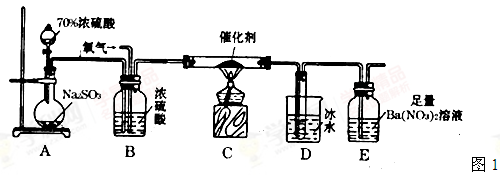
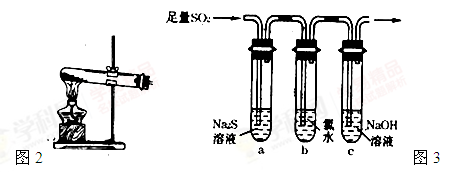
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是____________.
②实验过程中,需要通入氧气.试写出一个用图2所示装置制取氧气的化学方程式____________.
③当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是____________.
④实验结束后,若装置D增加的质量为m g,装置E中产生白色沉淀的质量为n g,则此条件下二氧化硫的转化率是____________(用含字母的代数式表示,不用化简)。
(3)某学习小组设计用如图3装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为____________.
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成
三份,分别进行如下实验:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,产生白色沉淀
上述方案中合理的是_______________(填“I”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为__________________.
高一化学实验题极难题查看答案及解析
-
硫酸亚铁铵(NH4)2Fe(SO4)2•6H2O又称莫尔盐,是浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:(已知:FeS2与H2SO4不反应)
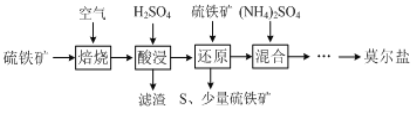
(1)莫尔盐属于____________。
A、酸式盐 B、碱式盐 C、复盐 D、硫酸盐
(2)硫铁矿焙烧的主反应是:4FeS2+11O2
2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有__________,若150kg硫铁矿(FeS2质量分数为80%)完全反应转移电子数为________________________
(3)加H2SO4酸浸,发生反应的离子方程式为________________________________。
(4)“还原”时,Fe3+可通过反应Ⅰ、Ⅱ被FeS2还原。
反应Ⅰ的离子方程式为:FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42—+16H+
反应Ⅱ的离子方程式为:_________________________________。
(5)为证明所得莫尔盐晶体中含有Fe2+和NH4+,实验方法是取其少量溶液于一支试管中,_______________证明含有Fe2+和NH4+。
高一化学工业流程中等难度题查看答案及解析
-
铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2
6SO2+Fe3O4,该反应中氧化产物为________,若有3mol FeS2参加反应,转移电子的物质的量为_______.
(2)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为_________.
(3)将一定量的Fe2O3溶于160mL 5mol•L﹣1盐酸中,再加入一定量铁粉,铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为______.
高一化学填空题中等难度题查看答案及解析
-
在硫酸的工业生产中,我国主要采用以黄铁矿(FeS2)为原料生产SO2,该反应的化学方程式为_________________,该反应在_______________(填设备名称)中进行.
高一化学填空题中等难度题查看答案及解析
-
硫铁矿【主要成分是二硫化亚铁(FeS2)】是一种重要的化工原料,常用来制备铁、硫酸和氯化铁,其工业流程示意图如图.(资料:Fe+2FeCl3=3FeCl2)
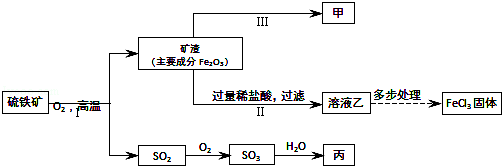
(1)Ⅱ中反应的化学方程式是 .
Ⅲ中反应的化学方程式是 .
(2)结合上述流程,硫铁矿中硫元素的化合价 ,如图出现的含硫元素的物质中,属于氧化物的有 (填化学式).
(3)若向溶液乙和丙的稀溶液中分别加入足量的甲,观察到的现象不同点是
高一化学填空题困难题查看答案及解析