-
化学与社会生活密切相关,下列说法正确的是( )
A.体积分数为95%的酒精通常作为医用酒精
B.石油裂解、煤的气化、海水的提镁都包含化学变化
C.绿色化学的核心是应用化学原理对环境污染进行治理
D.利用高纯度二氧化硅制造的太阳能电池板可将光能直接转化为电能
难度: 简单查看答案及解析
-
某烯烃与氢气加成后得到2,2-二甲基戊烷,烯烃的名称是( )
A.2,2-二甲基-3-戊烯 B.2,2-二甲基-4-戊烯
C.4,4-二甲基-2-戊烯 D.2,2-二甲基-2-戊烯
难度: 简单查看答案及解析
-
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
难度: 简单查看答案及解析
-
已知:H2(g)+1/2O2(g)=H2O(l) △H=-285.83kJ/mol
CO(g)+1/2O2(g)=CO2(g) △H=-282.91kJ/mol
若氢气与一氧化碳的混合气体完全燃烧可生成5.4克水(l),并放出114.04 kJ的热量,则混合气中一氧化碳的物质的量为( )
A.0.22 mol B.0.15 mol
C.0.1 mol D.0.05 mol
难度: 简单查看答案及解析
-
有机物的分离和提纯是有机化学研究的重要内容,分离和提纯下列物质所用的方法不正确的是
A.酒精和水—分液 B.淀粉中混有氯化钠—用半透膜进行渗析
C.汽油和柴油—分馏 D.三氯甲烷和水—分液
难度: 简单查看答案及解析
-
将a g聚苯乙烯树脂溶于bL苯中,然后通入c mol乙炔气体,所得混合液中碳氢两元素的质量比是( )
A.6︰1 B.12︰1 C.8︰3 D.1︰2
难度: 中等查看答案及解析
-
在2HCHO+NaOH(浓)→HCOONa+CH3OH中,甲醛( )
A. 仅被氧化 B. 仅被还原
C. 既未被氧化,又未被还原 D. 既被氧化,又被还原
难度: 中等查看答案及解析
-
利用电解法可将Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是( )
A.电解时以纯铜作阳极
B.电解时阳极发生还原反应
C.纯铜连接电源负极,电极反应是Cu-2e- =Cu2+
D.电解后,电解槽底部会形成含少量Ag、Au等金属阳极泥
难度: 中等查看答案及解析
-
用分液漏斗可以分离的一组液体混合物是( )
A.溴和CCl4 B.苯和溴苯 C.硝基苯和水 D.汽油和苯
难度: 中等查看答案及解析
-
能证明苯酚具有弱酸性的方法是( )
①苯酚溶液加热变澄清
②苯酚浊液中加NaOH后,溶液变澄清,生成苯酚钠和水.
③苯酚可与FeCl3反应
④在苯酚溶液中加入浓溴水产生白色沉淀
⑤苯酚能使石蕊溶液变红色
⑥苯酚能与Na2CO3溶液反应生成NaHCO3
A.⑤⑥ B.①②⑤ C.③④⑥ D.③④⑤
难度: 中等查看答案及解析
-
下列有关有机物分离提纯的方法正确的是( )
A.溴乙烷中混有溴单质,用NaOH溶液和水溶液,反复洗涤,再分液
B.肥皂中混有甘油,加入NaCl粉末,盐析
C.乙酸乙酯中混有乙酸,加入饱和Na2CO3溶液,充分反应后,再蒸馏
D.乙醛中混有乙烯,可通过溴水,即可除去乙烯
难度: 简单查看答案及解析
-
反应C(s)+H2O(g)⇌CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.将容器的体积扩大一倍 B.将容器的体积缩小一半
C.保持体积不变,充入N2使体系压强增大 D.保持压强不变,充入N2使容器体积变大
难度: 简单查看答案及解析
-
下列有关说法中正确的是( )
A.Ksp(AB2)<Ksp(CD),说明AB2的溶解度小于CD的溶解度
B.在ZnS的沉淀溶解平衡体系中加入蒸馏水,ZnS的Ksp改变
C.已知Ksp(AgCl)>Ksp(AgI),则反应AgCl(s)+I-(aq)═AgI(s)+Cl-(aq)能够发生
D.在CaCO3的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动
难度: 中等查看答案及解析
-
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
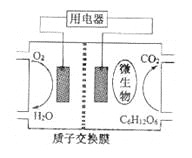
A. 该电池能够在高温下工作 B. 电池的负极反应为:
C. 放电过程中,
从正极区向负极区迁移 D. 在电池反应中,每消耗1mol氧气,理论上能生成标准状况下
气体
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.增大压强,活化分子数增多,化学反应速率一定增大
B.使用催化剂,降低反应的活化能,增大了活化分子百分数,化学反应速率一定增大
C.加入反应物,使活化分子百分数增加,化学反应速率增大
D.升高温度,活化分子百分数不一定增大,化学反应速率一定增大
难度: 中等查看答案及解析
-
反应4A(g)+5B(g)
4C(g)+6D(g),在5 L的密闭容器中进行,半分钟后,C的物质的量增加了0.30 mol。下列叙述正确的是( )
A. A的平均反应速率是0.010 mol•L﹣1•s﹣1
B. 容器中含D物质的量至少为0.45 mol
C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加了0.30 mol
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A. 凡能发生银镜反应的有机物一定是醛
B. 酸和醇发生的反应一定是酯化反应
C. 乙醇易溶于水是因为分子间形成了一种叫氢键的化学键
D. 在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯
难度: 简单查看答案及解析
-
有机物的结构简式可以用“键线式”表示,其中线表示键,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。已知利用某些有机物之间的转化可贮存太阳能,如降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应为
 (反应吸热),下列叙述中错误的是( )
(反应吸热),下列叙述中错误的是( )A. NBD和Q互为同分异构体
B. Q可使溴水褪色
C. Q的一氯代物只有3种
D. NBD的同分异构体可以是芳香烃
难度: 中等查看答案及解析
-
既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是( )
A. 通入足量溴的四氯化碳溶液中 B. 与足量的液溴反应
C. 通入酸性高锰酸钾溶液 D. 一定条件下与H2反应
难度: 简单查看答案及解析
-
下列叙述不正确的是
A.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.甲烷、乙醇、乙酸、乙酸乙酯都能发生取代反应
D.乙烯和苯都能使溴水褪色,且褪色的原因相同
难度: 简单查看答案及解析
-
某烯烃与氢气加成后得到2,2-二甲基丁烷,则该烯烃的名称是( )
A. 3,3-二甲基-1-丁烯 B. 2,2-二甲基-2-丁烯
C. 2,2-二甲基-1-丁烯 D. 2,2-二甲基-3-丁烯
难度: 简单查看答案及解析
-
下列物质属于芳香烃,但不是苯的同系物的是( )
①
②
③
④
⑤
⑥
A. ③ ④ B. ② ⑤ C. ① ② ⑤ ⑥ D. ② ③ ④ ⑤ ⑥
难度: 简单查看答案及解析
-
某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。下列说法中正确的是( )
①该化合物仅含碳、氢两种元素 ②该化合物中碳、氢原子个数比为1∶4
③无法确定该化合物是否含有氧元素 ④该化合物中一定含有氧元素
A. ①② B. ②④ C. ③④ D. ②③
难度: 中等查看答案及解析
-
下列关于苯酚的叙述中,错误的是( )
A.苯酚在水中的溶解度随温度的升高而增大
B.苯酚易溶于乙醇等有机溶剂
C.苯酚没有毒,其稀溶液可用作防腐剂和消毒剂
D.苯酚水溶液呈弱酸性,能与碱反应
难度: 简单查看答案及解析
-
化合物丙可由如图反应得到,则丙的结构不可能是
C4H10O
C4H8
C4H8Br2
A.CH3CBr2CH2CH3 B.(CH3)2CBrCH2Br
C.CH3CH2CHBrCH2Br D.CH3(CHBr)2CH3
难度: 中等查看答案及解析