-
已知:H2(g)+1/2O2(g)=H2O(l) △H =-285.83kJ/mol
CO(g)+1/2O2(g)=CO2(g) △H =-282.9kJ/mol
若氢气与一氧化碳的混合气体完全燃烧可生成5.4克水(l),并放出114.3kJ的热量,则混合气中一氧化碳的物质的量为( )
A.0.22 mol
B.0.15 mol
C.0.1 mol
D.0.05 mol
高二化学选择题中等难度题查看答案及解析
-
已知:H2(g)+1/2O2(g)=H2O(l) △H=-285.83kJ/mol
CO(g)+1/2O2(g)=CO2(g) △H=-282.91kJ/mol
若氢气与一氧化碳的混合气体完全燃烧可生成5.4克水(l),并放出114.04 kJ的热量,则混合气中一氧化碳的物质的量为( )
A.0.22 mol B.0.15 mol
C.0.1 mol D.0.05 mol
高二化学单选题简单题查看答案及解析
-
关于下列各图的叙述错误的是 ( )



A. 已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);ΔH= - 483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B. 常温下0.2 mol·L-1 HA溶液和0.1mol·L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(A-)> c(Na+)>c(H+)>c(OH-)
C. 常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐减小,且HX的还原性逐渐减弱
D. 图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
的变化情况
高二化学单选题中等难度题查看答案及解析
-
已知:CO(g)+H2O(g)
CO2(g)+H2(g) △H= -42kJ·mol-1
(1)在一定温度下,向一定体积的密闭容器中通入1molCO、2molH2O(g),反应达平衡时,测得放出的热量为28kJ,求CO的转化率为________;
(2)该温度下,向该密闭容器中通入
molCO2、
molH2,欲使反应达平衡时CO的转化率与(1)相同,则还需满足的条件是________;
(3)该温度下,向该密闭容器中通入2molCO、3molH2O(g),反应达平衡时时,求H2O(g)的转化率;
(4)该温度下,向该密闭容器中通入1.5molCO、3molH2O(g),反应达平衡时,放出的热量为________kJ。
高二化学填空题简单题查看答案及解析
-
已知:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-42kJ•mol-1
(1)在一定温度下,向一定体积的密闭容器中通入1molCO、2molH2O(g),反应达平衡时,测得放出的热量为28kJ,求CO的转化率为______;
(2)该温度下,向该密闭容器中通入molCO2、
molH2,欲使反应达平衡时CO的转化率与(1)相同,则还需满足的条件是______;
(3)该温度下,向该密闭容器中通入2molCO、3molH2O(g),反应达平衡时时,求H2O(g)的转化率______;
(4)该温度下,向该密闭容器中通入1.5molCO、3molH2O(g),反应达平衡时,放出的热量为______kJ.高二化学解答题中等难度题查看答案及解析
-
已知反应:COS(g)+H2(g)
H2S(g)+CO(g) ΔH1=+7 kJ/mol
COS(g)+H2O(g)
H2S (g)+CO2(g) ΔH2=-35 kJ/mol
则热化学方程式:CO(g)+H2O (g)
H2 (g)+CO2 (g) ΔH3,则ΔH3为
A.-42kJ/mol B.-28kJ/mol C.+42kJ/mol D.+28kJ/mol
高二化学单选题中等难度题查看答案及解析
-
已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g)⇌COS(g)+H2O(g)△H=﹣Q kJ•mol﹣1 (Q>0)。在温度为T1时,将0.10molCO2与0.40mol H2S充入2.5L 的空钢瓶中,经过4min反应达到平衡,平衡时H2O(g)的物质的量分数为 2%,则下列说法不正确的是( )
A.0~4 min内用H2S表示该反应的速率为0.001 mol•L﹣1•min﹣1
B.CO2的平衡转化率α=2.5%
C.上述条件下反应达到平衡时放出的热量为0.01Q kJ
D.其他条件不变,若该反应在温度为T2 条件下进行,达到平衡所需时间小于4 min,则 T1<T2
高二化学单选题中等难度题查看答案及解析
-
已知:CO2(g)+3H2(g)
CH3OH(g)+ H2O(g) ΔH=-49.0 kJ﹒mol-1。一定条件下,向体积为1 L的密闭容器中充入1 molCO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中,正确的是
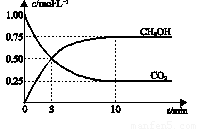
A.10min后,升高温度能使
增大
B.3 min时,CO2的消耗速率等于用CH3OH生成速率,且二者浓度相同
C.欲提高H2的平衡转化率只能加压减小反应容器的体积
D.从反应开始到平衡,H2的平均反应速率v(H2)=0.075 mol﹒L-1﹒min-1
高二化学选择题困难题查看答案及解析
-
已知:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=﹣49.0kJ•mol﹣1.一定条件下,向体积为1L的密闭容器中充入1molCO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示.下列叙述中正确的是
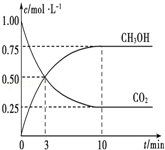
A.欲增大平衡状态时
的比值,可采用升高温度的方法
B.达到平衡状态时,CO2的平衡转化率为75%
C.欲提高H2的平衡转化率只能加压减小反应容器的体积
D.从反应开始到平衡,H2的平均反应速率v(H2)=0.075 mol•L﹣1•min﹣1
高二化学选择题困难题查看答案及解析
-
氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:
H2(g)+1/2O2(g)=H2O(l); △H=-285.8 kJ / mol
CO(g)+1/2O2(g)=CO2(g); △H=-283.0 kJ / mol
C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(l); △H=-5518 kJ / mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l); △H=-890.3 kJ / mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是
A. H2(g) B. CO(g) C. C8H18(l) D.CH4(g)
高二化学选择题中等难度题查看答案及解析