-
下列民间制作属于化学变化的是( )
A.佛山剪纸 B.潮州木雕 C.信宜竹编 D.客家米酒
难度: 简单查看答案及解析
-
2019年12月以来,新冠疫情席卷全球。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是( )
A.家庭消毒时,消毒液越浓越好 B.吸烟、喝酒可以预防“新型冠状病毒”
C.应经常保持室内清洁卫生和通风 D.必须每天吃药,补充人体所需化学物质
难度: 简单查看答案及解析
-
除去下列物质中所含的杂质,所用的试剂和方法正确的是
选项
物质
杂质
试剂和方法
A
CO2
水蒸气
通过碱石灰
B
KOH溶液
Ca(OH)2
加入过量K2CO3溶液,过滤
C
CaO
CaCO3
高温煅烧
D
CuO
Cu
加入适量稀硫酸,过滤
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
下列物质的性质与用途对应关系错误的是
A.金刚石硬度大,可制造钻头 B.氮气的化学性质不活泼,常用作保护气
C.铜有良好的导电性,可制作导线 D.氢氧化钠具有碱性,常用于改良酸性土壤
难度: 简单查看答案及解析
-
2020年复工不足一月,国内就已经发生了12起火灾爆炸事故,安全生产、警钟长鸣,为做好复工及春季防火工作,下列安全标识不应在化学品仓库出现的是( )
A.
 B.
B. C.
C. D.
D.
难度: 简单查看答案及解析
-
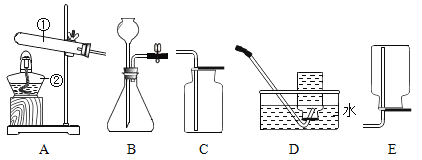
下列操作不正确的是( )
A.
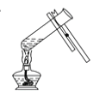 加热液体 B.
加热液体 B. 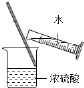 稀释浓硫酸
稀释浓硫酸C.
 取固体粉末 D.
取固体粉末 D. 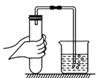 检查气密性
检查气密性难度: 中等查看答案及解析
-
某同学测得生活中常见物质的pH如下表,其中能使紫色石蕊试液变红的物质是
物质
牙膏
肥皂水
橘汁
草木灰水
食盐水
pH
8.2
9.2
3.5
10.6
7.0
A.食盐水 B.牙膏
C.草木灰 D.橘汁
难度: 简单查看答案及解析
-
下列物质中,属于混合物的是( )
A.氧化铜 B.氯化氢气体 C.洁净的空气 D.冰水混合物
难度: 简单查看答案及解析
-
近期,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。过氧乙酸CH3COOOH可以起到消毒作用,其分子结构如图所示。有关过氧乙酸的下列叙述不正确的是( )
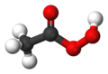
A.每个过氧乙酸分子由9个原子构成
B.其相对分子质量为76
C.C、H、O三种元素的质量比为2:4:3
D.完全燃烧生成CO2和H2O
难度: 简单查看答案及解析
-
用红磷燃烧测定空气中氧气含量的实验装置如图所示,实验过程中,下列做法不能达到实验目的的是( )
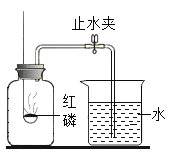
A.使用过量的红磷进行实验
B.冷却后再打开止水夹,使水倒流入集气瓶
C.把红磷改为铁丝再进行实验
D.可以直接用放大镜聚焦太阳光点燃红磷,进行实验
难度: 简单查看答案及解析
-
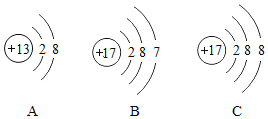
芯片是中美经贸摩擦的焦点之一、制造芯片的高纯硅可以用下述方法制取(反应条件略):下列有关说法错误的是( )
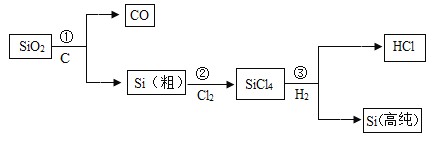
A.反应①、③均为置换反应
B.SiCl4中Si的化合价为—4
C.反应①中表现了碳的还原性
D.硅原子的核电荷数为14
难度: 中等查看答案及解析
-
可用推拉注射器活塞的方法检查如图中装置的气密性.当缓慢拉活塞时,如果装置气密性良好,可观察到
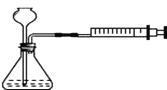
A.长颈漏斗下端口产生气泡
B.瓶中液面明显上升
C.长颈漏斗内有液面上升
D.注射器内有液体
难度: 中等查看答案及解析
-
在点燃条件下,甲与一定量的乙反应生成丙和丁的微观示意图如图。下列说法正确的是( )
0
A.该反应前后,硫元素的化合价不变
B.该反应的化学方程式为:H2S+O2
S+H2O
C.若在该反应中继续通入足量的乙,则乙与丙可进一步反应
D.该反应不属于置换反应
难度: 中等查看答案及解析
-
下列图像能正确反映实验操作的是
A.
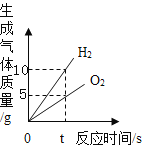 电解水
电解水B.
向一定量稀硫酸中不断加入氢氧化钡溶液
C.
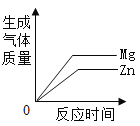 向两份等质量、相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉
向两份等质量、相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉D.
用氯酸钾和二氧化锰混合加热制取氧气
难度: 困难查看答案及解析