-
化学与生产、生活、科技、环境等密切相关。下列说法不正确的是
A.“华为麒麟980”手机中芯片的主要成分是硅单质
B.高铁“复兴号”车厢连接关键部位使用的增强聚四氟乙烯板属于高分子材料
C.港珠澳大桥设计使用寿命120年,水下钢柱镶铝块防腐的方法为牺牲阳极的阴极保护法
D.纳米铁粉可以高效地去除被污染水体中的
、
、
、
等重金属离子,其本质是纳米铁粉对重金属离子的物理吸附
难度: 简单查看答案及解析
-
设
表示阿伏伽德罗常数的值,下列说法正确的是
A.标准状况下,2.24L三氯甲烷中含碳氯共价键的数目为0.3
B.
溶液与
溶液中的
数目相同
C.1mol硝基
与46g二氧化氮
中所含的电子数均为23
D.在一定条件下,
和
,充分反应,生成
的分子数为0.2
难度: 中等查看答案及解析
-
正四面体烷的球棍模型如图所示。下列关于该化合物的说法正确的是
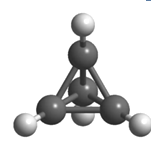
A.碳碳键的键角为
B.与丁二烯互为同分异构体
C.二氯代物有2种 D.正四面体烷生成1mol丁烷至少需要3mol
难度: 中等查看答案及解析
-
用下列试剂和试管中的物质不能完成相应实验目的的是
实验目的
试剂
试管中的物质
A
鉴别碳酸钠和碳酸氢钠固体
稀盐酸
①碳酸钠②碳酸氢钠
B
比较
、
、
的还原性
氯水
①
溶液②
溶液
C
证明苯分子中没有碳碳双键
的
溶液
①苯②己烯
D
探究接触面积对反应速率的影响
VmL、
的盐酸
①ag大理石块②ag大理石粉
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
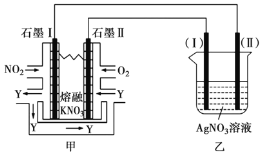
我国科学家成功研制出铝-石墨烯(
)可充电电池,电解质为阳离子(
)与阴离子(
)组成的离子液体,该电池放电过程如右图所示。下列说法错误的是
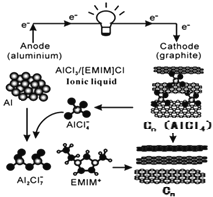
A.放电时负极的反应为:
B.放电时石墨烯为正极,发生还原反应
C.充电时石墨烯与电源的正极相连
D.充电时的总反应为:
难度: 中等查看答案及解析
-
X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的两种或三种所组成的化合物,其中A、C、E为有机物。已知A的相对分子质量为28,B分子中含有18个电子,D分子中含有10个电子,五种化合物间的转化关系如下图所示。下列说法正确的是
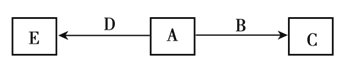
A.W是所在周期中原子半径最大的元素
B.Y的最高价氧化物的水化物为弱酸
C.X、Y、Z组成的分子中只含有极性键
D.X、Y组成的化合物的沸点一定比X、Z组成的化合物的沸点低
难度: 中等查看答案及解析
-
已知
。
时,
和
的饱和溶液中,金属阳离子的物质的量浓度的负对数
与溶液pH的变化关系如图所示。下列说法正确的是
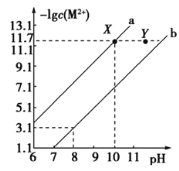
A.向等浓度的
和
的混合溶液中滴加
溶液,
先沉淀
B.当
和
沉淀共存时,溶液中:
C.Y点对应的
分散系是不稳定的体系
D.通过直接控制pH的方法可除去
溶液中含有的量
难度: 中等查看答案及解析
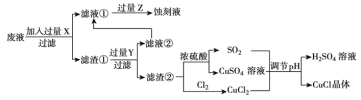
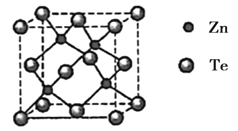
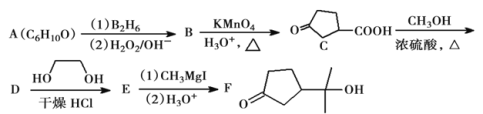
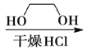
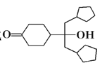 路线(其他试剂任选)。__________
路线(其他试剂任选)。__________