-
碘量法测定废水中硫化物的实验装置如图所示。
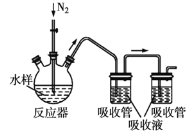
Ⅰ.取样、吹气、固硫
按右图连接好装置,检查气密性。取足量的醋酸锌吸收液于两支吸收管中,取100mL水样于反应器中,通入氮气一段时间后,向反应器中加入10mL盐酸, 加热,反应后继续通入氮气。
加热,反应后继续通入氮气。
已知:废水中的硫化物在酸性条件下易转化为剧毒的硫化氢,醋酸锌可用于完全吸收硫化氢生成硫化锌沉淀。回答下列问题:
(1)图中反应器的名称是________,反应后继续通入氮气的目的是________,反应器加热温度不能高于 的原因是________。
的原因是________。
Ⅱ.滴定、分析
关闭氮气后,往两支吸收管中各加入 的碘标准溶液50mL(过量),静置。加入淀粉指示液,用
的碘标准溶液50mL(过量),静置。加入淀粉指示液,用 的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定,共消耗
的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定,共消耗 ,溶液
,溶液 。
。
(2)加入碘标准溶液时吸收管中发生反应的化学方程式为________。
(3)滴定终点的现象为________。
(4)废水中硫的含量为________ 。若只使用一支吸收管,可能致测定结果偏________(填“高”或“低”。)
。若只使用一支吸收管,可能致测定结果偏________(填“高”或“低”。)
-
硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:
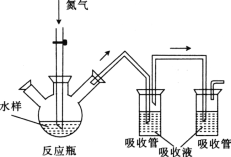
Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。
(已知: )
)
回答下列问题:
(1)反应瓶中前后通入氮气的目的分别是________________、_________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是____,若只使用一个吸收管,会导致测定结果偏____(填“高”或“低”)。
(4)实验室常用FeS固体与酸常温下反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是_______________(填序号)。
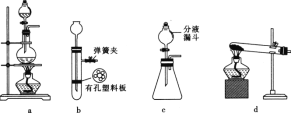
(5)上图a中盛装液体药品的玻璃仪器名称为________。
(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:_______________。
-
硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:
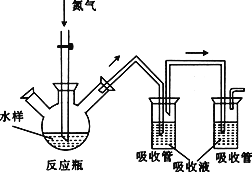
Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。(已知: )
)
回答下列问题:
(1)水浴加热的温度不能高于85℃,原因是_____________________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是_____________________________,若只使用一个吸收管,会导致测定结果偏______________________(填“高”或“低”)。
(4)该200mL水样经吹气、固硫后,滴定操作时共消耗160mLNa2S2O3溶液,则废水中硫的含量为________mg·L-1。
(5)实验室常用FeS固体与酸反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是________(填序号)。
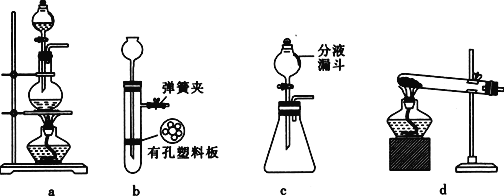
(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:____。
-
硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:
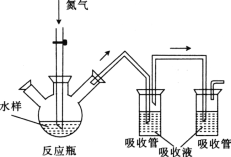
Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。
(已知: )
)
回答下列问题:
(1)反应瓶中前后通入氮气的目的分别是________________、_________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是____,若只使用一个吸收管,会导致测定结果偏____(填“高”或“低”)。
(4)实验室常用FeS固体与酸常温下反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是_______________(填序号)。
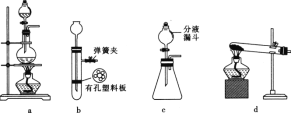
(5)上图a中盛装液体药品的玻璃仪器名称为________。
(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:_______________。
-
某学习小组在实验室中利用如图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
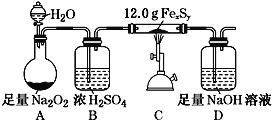
实验步骤:
步骤Ⅰ如图连接装置,检查装置气密性,装入试剂;
步骤Ⅱ旋开分液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤Ⅲ足够长时间后,D中产生气泡速率变快时,停止加热,继续向烧瓶中滴水一段时间
步骤Ⅳ实验结束后,将D中所得溶液加水配制成250mL溶液;
……
请回答:
(1)步骤Ⅲ中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为___。
(2)在C、D装置之间不需要防倒吸装置的理由是___。
(3)步骤Ⅳ中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___。
(4)取25.00mL步骤Ⅳ中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则FexSy的化学式为___。
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案是否合理:__(填“是”或“否”),原因为__。
(6)反应后D装置所得溶液中除含有Na2SO4外,还可能含有Na2SO3。现用滴定法测定溶液中Na2SO3的含量。可供选择的试剂:0.1000mol·L-1 KMnO4酸性溶液;0.1000mol·L-1 H2O2溶液;0.1000mol·L-1KI淀粉溶液;0.1000mol·L-1BaCl2溶液;0.1000mol·L-1HCl溶液。
①所选试剂应装在___(填“酸式”或“碱式”)滴定管中。
②所利用的反应原理为___(用离子方程式表示)。
-
某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。

实验步骤:
步骤I如图连接装置,检查装置气密性,装入药品;
步骤II旋开滴液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤III当硬质玻璃管中固体质量不再改变时,停止加热,继续向烧瓶中滴水一段时间
步骤IV实验结束后,将D中所得溶液加水配制成250mL溶液;
……
请回答:
(1)步骤III中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为___________________。
(2)在C、D装置之间不需要防倒吸装置的理由是_______________________________________。
(3)步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有_____________________。
(4)取25.00mL步骤IV 中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则FexSy的化学式为________________。
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案____(填“是”或“否”)合理,原因为_____________________。
(6)反应后D装置所得溶液中除含有Na2SO4外,还可能含有Na2SO3。现用滴定法测定溶液中Na2SO3的含量。可供选择的试剂:①0.1000mol/LKMnO4酸性溶液;②0.1000mol/LH2O2溶液;③0.1000mol/LKI淀粉溶液;④0.1000 mol/LBaCl2溶液;⑤0.1000mol/LHCl溶液。
①所选试剂应装在_____(填“酸式”或“碱式”) 滴定管中。
②所利用的反应原理为___________________________________(用离子方程式表示)。
-
水中的溶解氧是水生生物生存不可缺少的条件。某课外小组设计如图所示的实验装置 夹持装置略
夹持装置略 ,采用碘量法测定学校周边河水中的溶解氧的含量。
,采用碘量法测定学校周边河水中的溶解氧的含量。
实验步骤及测定原理如下:
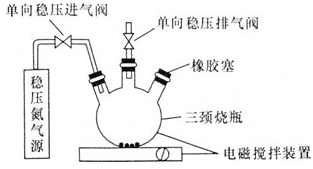
Ⅰ.取样、氧的固定
 用溶解氧瓶采集水样,记录大气压及水体温度。
用溶解氧瓶采集水样,记录大气压及水体温度。
 向烧瓶中加入200mL水样。
向烧瓶中加入200mL水样。
 向烧瓶中依次迅速加入
向烧瓶中依次迅速加入 无氧溶液
无氧溶液 过量
过量 和2mL碱性KI无氧溶液
和2mL碱性KI无氧溶液 过量
过量 ,开启搅拌器,反应生成
,开启搅拌器,反应生成 ,实现氧的固定。
,实现氧的固定。
Ⅱ 酸化、滴定
酸化、滴定
 搅拌,并向烧瓶中加入2mL硫酸无氧溶液至
搅拌,并向烧瓶中加入2mL硫酸无氧溶液至 被
被 还原为
还原为 ,溶液为中性或弱酸性。
,溶液为中性或弱酸性。
 在暗处静置5min后,取一定量溶液,用
在暗处静置5min后,取一定量溶液,用 标准溶液滴定生成的
标准溶液滴定生成的 ,记录数据。
,记录数据。

 处理数据
处理数据 忽略氧气从水样中的逸出量和加入试剂后水样体积的变化
忽略氧气从水样中的逸出量和加入试剂后水样体积的变化 。
。
回答下列问题:
 配制以上无氧溶液时,除去所用溶剂水中的氧气的简单操作为________。
配制以上无氧溶液时,除去所用溶剂水中的氧气的简单操作为________。
 取水样时应尽量避免扰动水体表面,这样操作的主要目的是________。
取水样时应尽量避免扰动水体表面,这样操作的主要目的是________。
 “步骤c”中“搅拌”的作用是________。
“步骤c”中“搅拌”的作用是________。
 “氧的固定”中发生主要反应的化学方程式为________。
“氧的固定”中发生主要反应的化学方程式为________。
 “步骤f”为________。
“步骤f”为________。
 “步骤e”中,用amol/LNa2S2O3标准溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为________;若200mL水样经处理后,共消耗
“步骤e”中,用amol/LNa2S2O3标准溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为________;若200mL水样经处理后,共消耗 标准溶液的体积为bmL,则水样中溶解氧的含量为________
标准溶液的体积为bmL,则水样中溶解氧的含量为________ 用含字母的式子表示)mg/L。
用含字母的式子表示)mg/L。
 “步骤d”中加入硫酸溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的原因
“步骤d”中加入硫酸溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的原因 用离子方程式表示,至少写出2个
用离子方程式表示,至少写出2个 :________。
:________。
-
利用下左图所示实验装置可以测定常温常压下气体的摩尔体积。
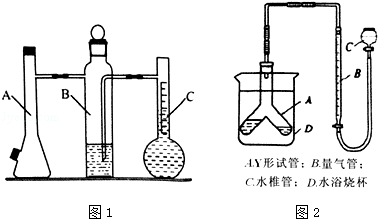
甲同学利用如图1装置,根据下列步骤完成实验:①装配好装置,作气密性检查.②用砂纸擦去镁带表面的氧化物,然后取0.108g的镁带.③取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口.④用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平.⑤用注射器吸取10mL3mol•L﹣1硫酸溶液,用针头扎进A瓶加料口橡皮塞,将硫酸注入A瓶,注入后迅速拔出针头.⑥当镁带完全反应后,读取C瓶中液体的体积,记录数据.⑦用注射器从A瓶加料口处抽出8.0mL气体,使B瓶中导管内外液面持平.⑧读出C瓶中液体体积是115.0mL.完成下列填空:
(1)常温常压下的压强为 ,温度为 .
(2)在常温常压下气体摩尔体积理论值约为24.5L/mol,甲同学测出此条件下lmol气体的体积为 ,计算此次实验的相对误差为 %(保留2位有效数字).引起该误差的可能原因是 .
a.镁带中含铝;b.没有除去镁带表面的氧化物;c.反应放热;d.所用硫酸的量不足
(3)丙同学提出可用如图2装置完成该实验.该装置气密性的检查方法是: .
(4)与原方案装置相比,丙同学使用的装置实验精度更高.请说明理由(回答两条) , .
-
某同学利用如图所示实验装置测定常温常压下的气体摩尔体积。
根据下列步骤完成实验:
①装配好装置,检查气密性
②用砂纸擦去镁带表面的氧化物,然后取0.0480g的镁带加入仪器a中,分液漏斗内加入足量1mol/L硫酸溶液
③量气装置中加入适量水,记录量气管读数(读数为0.10mL)
④通过分液漏斗向仪器a中加入适量硫酸溶液,使镁带与硫酸充分反应
⑤当镁带完全反应后,再次记录量气管读数(读数为49.60mL)。
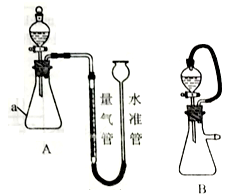
完成下列填空:
(1)仪器a的名称_______,通过分液漏斗向仪器a中加入硫酸溶液的操作是_______。
(2)在记录量气管读数时,应注意将_______,再________,视线与量气管内凹液面相切,水平读数。
(3)该同学测出此条件下气体摩尔体积为__________,测定结果比理论值偏大,可能的原因是(填字母代号)__________。
a.镁带中氧化膜未除尽 b.镁带含有杂质铝
c.③记录量气管读数时俯视读数 d.镁带完全反应后有残留的未溶固体
(4)与原方案装置相比,有同学设想用装置B代替装置A,实验精确度更高。请说明理由____________________。
-
(14分)工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:实验原理是
A.连接全部仪器,使其成为如图装置,并检查装置的气密性。
B.称取研细的辉铜矿样品1.000g。
C. 将称量好的样品小心地放入硬质玻璃管中。
D.以每分钟1L的速率鼓入空气。
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2=SO2 +2Cu。
F.移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。
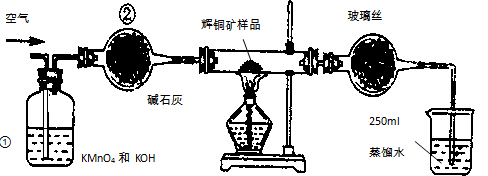
试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是_________。
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
| | | |
(4)本方案设计中有一个明显的缺陷影响了测定结果(不属于操作失误),你认为是__________(写一种即可)。
(5)已知在常温下FeS 的 Ksp= 6.25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系: c2 (H+) ·c(S2-) = 1.0×10-22 。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为 lmol/L,应调节溶液的c(H十)为__________________。
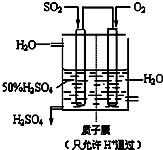
(6)某人设想以下图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式______.

加热,反应后继续通入氮气。
的原因是________。
的碘标准溶液50mL(过量),静置。加入淀粉指示液,用
的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定,共消耗
,溶液
。
。若只使用一支吸收管,可能致测定结果偏________(填“高”或“低”。)












