-
下列说法正确的是( )
A.硅胶可作袋装食品的干燥剂
B.漂白粉在空气中很稳定
C.生石灰能与水反应,可用来干燥氯气
D.碘是人体必需微量元素,所以要多吃富含高碘酸的食物
难度: 简单查看答案及解析
-
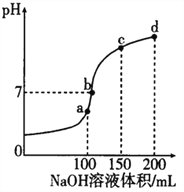
下列说法不正确的是
A.常温下,pH<7的溶液一定是酸溶液
B.常温下,浓度均为0.1mol·L-1的盐酸和醋酸溶液,盐酸的导电能力强
C.中和相同体积、相同浓度的氨水和NaOH溶液,所需HCl的物质的量相同
D.向NaOH溶液中滴加醋酸至c(CH3COO‾)=c(Na+),则溶液呈中性
难度: 中等查看答案及解析
-
2019年12月27日20时45分,长征五号遥三运载火箭(被称为“胖五”)在中国文昌航天发射场点火升空,“胖五”浑身是高科技。下列有关其说法正确的是( )
A.液氢、煤油、液氧推进剂利用了燃料电池原理
B.“胖五”某些外表部位覆盖玻璃纤维织物,玻璃纤维是有机高分子材料
C.储氢箱、储氧箱表面裹有10~20mm发泡塑料,其作用是保温
D.“胖五”外壳主要材料是铝合金,利用了该材料耐腐蚀、密度大等特点
难度: 简单查看答案及解析
-
一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐的装置示意图如图1所示; 研究人员发现的一种“水”电池,其总反应为:5MnO2 +2Ag+2NaCl=Na2Mn5Ol0+2AgCl,用该“水”电池为电源电解NaCl溶液的实验装置如图2所示,电解过程中X电极上有无色气体逸出。下列说法正确的是( )
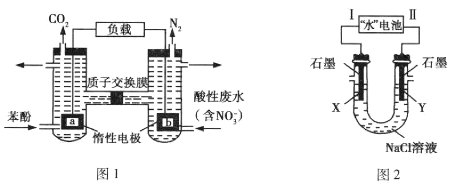
A.图1装置中若右池产生0.672 L气体(标准状况下),则电路中通过电子0.15 mol
B.图1装置中左池消耗的苯酚与右池消耗的
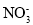 的物质的量之比为28:5
的物质的量之比为28:5C.图2装置的电路中每通过1 mol e-,U形管中消耗0.5 mol H2O
D.图2装置中“水”电池内每生成1 mol Na2Mn5O10,X电极上生成1 mol气体
难度: 中等查看答案及解析
-
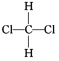
1-甲基环丙烯(
 )是合成的植物生长调节剂,可用来防止乙烯敏感型果蔬的早熟,下列有关其说法正确的是
)是合成的植物生长调节剂,可用来防止乙烯敏感型果蔬的早熟,下列有关其说法正确的是A.与丁烯互为同分异构体
B.所有碳原子均处于同一平面
C.生成1molC4H10至少需要1molH2
D.与高锰酸钾溶液合用,增长果蔬的保鲜时间
难度: 中等查看答案及解析
-
海水结冰形成海冰,海冰中部分盐分被包裹在冰晶中,形成如下图所示的含“盐泡”(设1个盐泡中含1个NaCl单元)的海冰。测得某海冰内层中NaCl的浓度为10-4mol·L-1,已知该层海冰的密度为0.9g·cm-3。下列说法错误的是( )
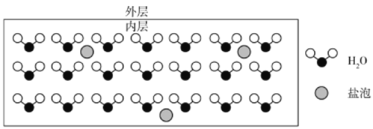
A.“盐泡”内的钠、氯以离子的形式存在
B.海冰密度越大,则海冰中的“盐泡”越少
C.海冰中形成的氢键比例比海水中的大
D.该海冰中“盐泡”与H2O的个数比约为1:(5105)
难度: 简单查看答案及解析
-
某同学采用废铁屑(主要成分为Fe2O3、Fe,少量碳) 制取碳酸亚铁(FeCO3) ,设计了如下流程:
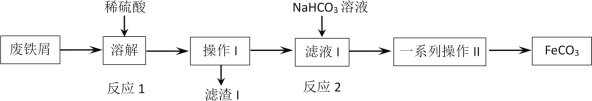
根据以上流程图,下列说法不正确的是( )
A.工业废铁屑往往附着有油脂,可通过热饱和碳酸钠溶液洗涤除去
B.反应2的离子方程式:Fe2++HCO3- = FeCO3↓+H+
C.操作I为过滤,洗涤操作,一系列操作II为过滤,洗涤,干燥
D.为避免硫酸溶解时Fe2+被空气氧化,废铁屑应适当过量
难度: 中等查看答案及解析
-
某固体X可能含有FeO、Fe2O3、MnO2、K2SO3、Na2CO3、NaClO、K2SO4中的一种或几种物质,进行如下实验以确定其组成:
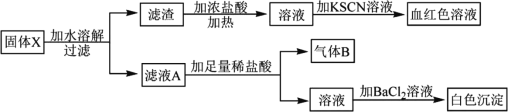
下列有关说法正确的是
A.若固体X中不含K2SO4,则一定含NaClO
B.固体X中一定含有Fe2O3
C.滤液A中一定含有Na+
D.气体B一定是纯净物
难度: 中等查看答案及解析
 和
和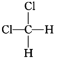 ⑦
⑦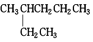 和
和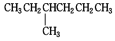 ⑧氯气和氯水 ⑨红磷和白磷
⑧氯气和氯水 ⑨红磷和白磷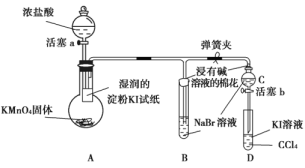

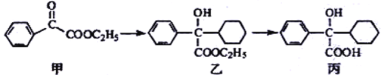
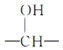 不能最终被氧化为—COOH;
不能最终被氧化为—COOH;