-
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_____、_______;杂化轨道分别是________、_________;a分子的立体结构是____________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体;
(3)X的氧化物与Y的氢化物中,分子极性较小的是(填分子式)________;
(4)Y与Z比较,电负性较大的是____________;
(5)W的元素符号是________,其+2价离子的核外电子排布式是________。
高二化学推断题中等难度题查看答案及解析
-
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,a的分子式是_____,b的结构式是_______;中心原子的杂化轨道类型分别是________、_________;a分子的立体结构是____________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体;
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)________;
(4)Y与Z比较,电负性较大的是____________;
(5)W的元素符号是________,其+2价离子的核外电子排布式是________
高二化学填空题简单题查看答案及解析
-
(10分) 四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4︰1,其d轨道中的电子数与最外层电子数之比为5︰1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是________、________;杂化轨道分别是________、________;a分子的立体结构是________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________晶体、________晶体。
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)________。
(4)Y与Z比较,电负性较大的________,其中W+2价离子的核外电子排布式是________。
高二化学填空题简单题查看答案及解析
-
(10分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,
①它们的分子式分别是________、________;
②杂化轨道分别是________、________;
③a分子的立体结构是________;
(2)X的氧化物与Y的氧化物中,分子极性较小的是________;(填分子式)
(3)Y与Z比较,电负性较大的是________;(填元素名称)
(4)W的元素符号是________,其+2价离子的核外电子排布式是________。
高二化学填空题简单题查看答案及解析
-
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4∶1,其d轨道中的电子数与最外层电子数之比为5∶1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是________、________;杂化轨道分别是________、________;a分子的立体结构是________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________晶体、________晶体。
(3)Y与Z比较,电负性较大的是________,W2+离子的核外电子排布式是________。
高二化学推断题简单题查看答案及解析
-
A、B、C、D四种原子序数为前20号元素,核电荷数依次增加,它们离子的电子层数相同,且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。回答以下问题:
(1)写出元素符号:B______C______
(2)试画出离子结构示意图:B______,A的简单氢化物的结构式______
(3)写出B元素的最高价氧化物对应水化物的化学式______
高二化学有机推断题中等难度题查看答案及解析
-
已知:G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大。G的简单阴离子最外层有2个电子,Q原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同;T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于分子晶体;在元素周期表中Z元素位于第11列。
回答下列问题:
(1)Z的核外外围电子排布式是____________________________________________。
(2)X以及与X左右相邻的两种元素,其第一电离能由小到大的顺序为____________(填元素符号)。
(3)QR2分子中,Q原子采取________杂化,写出与QR2互为等电子体的一种分子的化学式:____________。
(4)分子式为G 2R、G 2Y的两种物质中一种更稳定,原因是_____________;T的氯化物的熔点比Q的氯化物的熔点高,原因是___________________。
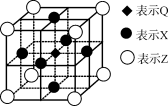
(5)据报道,由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如下图所示。晶体中距每个X原子周围距离最近的Q原子有______个。
高二化学填空题极难题查看答案及解析
-
已知Q、R、X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中Q原子外层电子数是内层电子数的两倍;化合物R2Z的晶体为离子晶体,Z原子核外的M层中有两对成对电子;X元素最外层电子数与最内层电子数相同;Y单质的晶体类型在同周期的单质中没有相同的;W元素所在族有三列,只有两个未成对的电子。请根据以上信息,回答下列问题:(答题时,Q、R、X、Y、Z、W用所对应的元素符号表示)
(1)W的外围电子(价电子)排布式是 。
(2)Q、R、X、Y的第一电离能由小到大的顺序为_ 。(用元素符号表示)
(3)QZ2分子的空间构型为 形。
(4)R的氯化物的熔点比Y的氯化物的熔点_ _(填高或低),理由是_ _ 。
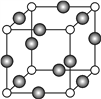
(5)据报道,只含Q、X、W三种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构如图,试写出该晶体的化学式_ 。晶体中每个X原子周围距离最近的W原子有__ _个。

高二化学填空题简单题查看答案及解析
-
有V、W、X、Y、Z五种元素,它们是核电荷数依次增大的前四周期元素;X、Z是金属元素;V和X元素原子的最外层电子都只有一个;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;Z是一种常见金属元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。由此可知:
(1)X在元素周期表中的位置是________,Z的元素符号是________
(2)V-W和V—Y属于极性共价键,其中极性较强的键是______(V、W、Y用元素符号表示)。
(3)w与X形成原子个数之比为1:1的化合物的电子式为________
(4)工业上冶炼Z单质的化学方程式为________
高二化学填空题简单题查看答案及解析
-
X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
(1)U2+的外围电子排布式为________.
(2)X、Y、Z 可以形成化学式为XYZ的分子.该分子中各原子均达到稀有气体稳定结构,则该分子中Y采取的杂化轨道类型为__________.
(3)比较Y和W的第一电离能,较大的是__________(填元素符号).
(4)X与Z形成的最简单化合物Q的分子构型为__________;
(5)U+与Z3﹣形成的晶胞结构如图所示,阴、阳离子间的核间距为acm.与同一个Z3﹣相连的U+有________个,该晶体的密度为__________ g·cm﹣3.(设NA表示阿伏加德罗常数)
高二化学填空题困难题查看答案及解析