-
有V、W、X、Y、Z五种元素,它们是核电荷数依次增大的前四周期元素;X、Z是金属元素;V和X元素原子的最外层电子都只有一个;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;Z是一种常见金属元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。由此可知:
(1)X在元素周期表中的位置是________,Z的元素符号是________
(2)V-W和V—Y属于极性共价键,其中极性较强的键是______(V、W、Y用元素符号表示)。
(3)w与X形成原子个数之比为1:1的化合物的电子式为________
(4)工业上冶炼Z单质的化学方程式为________
高二化学填空题简单题查看答案及解析
-
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族.
(1)D在周期表中的位置______;B的原子结构示意图______;
(2)E元素形成最高价氧化物对应的水化物的化学式为______;
(3)元素C、D、E形成的原子半径大小关系是______(用元素符号表示).
(4)C、D可形成化合物D2C2,D2C2含有的化学键是______;
(5)A、C两种元素形成的原子个数之比为1:1的化合物电子式______,
(6)B的氢化物与B的最高价氧化物的水化物反应的离子方程式_____。
高二化学综合题中等难度题查看答案及解析
-
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第________周期第________族。
(2)E元素形成的氧化物对应的水化物的化学式为____________________。
(3)元素C、D、E形成的简单离子半径大小关系是 ______>______>_____(用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:____________________。C、D还可形成化合物D2C2,D2C2中含有的化学键是________________________。
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)E元素形成的氧化物对应的水化物的化学式为_______________________________。
(2)元素C、D、E形成的简单离子半径大小关系是____________(用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程:_________________。C、D还可形成化合物D2C2,D2C2中含有的化学键类型是_______________________________________________。
(4)由A、B、C三种元素形成的离子化合物的化学式为__________________,它与强碱溶液共热,发生反应的离子方程式是______________________。
(5)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为________________________(化学式用具体的元素符号表示)。
高二化学填空题中等难度题查看答案及解析
-
元素性质呈现周期性变化的根本原因是( )
A.元素原子电子层数增大
B.元素原子最外层电子数呈现周期性变化
C.元素的化合价呈现周期性变化
D.核电荷数依次增大
高二化学单选题简单题查看答案及解析
-
m、n、p、q、w五种元素,其核电荷数依次增大。m元素基态原子核外只有三个能级,且各能级电子数相等,p、q元素位于同一族,且两者核电荷数之和为24,w元素原子核外有4个电子层,最外层只有1个电子,其余各层均排满电子。下列说法错误的是( )
A.m、n、p元素第一电离能依次增大
B.基态n元素原子的轨道表示式为:
C.w元素原子的价电子排布式为4s1
D.w单质分别与p、q单质反应,产物中w的化合价不同
高二化学多选题简单题查看答案及解析
-
(选做题)(8分)有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且均小于20,其中X、Z是金属元素,V和Z元素原子的最外层都只有一个电子,W和Y元素原子的最外层电子数相等,且W元素原子L层电子数是K层电子数的3倍,X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可推知(填元素符号):
V是__________ W是__________ X是__________ Y是__________
高二化学填空题简单题查看答案及解析
-
(10分)Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,Q、W、Z是非金属元素。五种元素核电荷数之和为55,对应原子最外层电子数之和为21。W、Z最外层电子数相同,但Z的核电荷数是W的2倍。
(1)Q在周期表中位于第________________________________________周期________________________________________族。
(2)X、Y各自的最高价氧化物对应的水化物可以发生反应生成盐和水,请写出该反应的离子方程式:________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
(3)X单质能在W单质中燃烧可生成化合物R,R的电子式___________________________________________________________________________,该物质所含有的化学键的类型为________________________________________________________________________________________________________________________________________________。
(4)Z的氢化物与W的氢化物发生反应生成Z单质和水,写出其化学方程式________________________________________________________________________________________________________________________________。
高二化学填空题中等难度题查看答案及解析
-
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,Q、W、Z是非金属元素。五种元素核电荷数之和为54,对应原子最外层电子数之和为20。W、Z最外层电子数相同,但Z的核电荷数是W的2倍。
(1)X、Y各自的最高价氧化物对应的水化物可以发生反应生成盐和水,该反应的离子方程式为______________________________________________________。
(2)X与W可形成X2W和X2W2两种化合物,X2W2的电子式为_____________。
(3)Q与W可形成化合物QW2,这种化合物固态时属于________晶体。
(4)Y的硝酸盐水溶液显________性,用离子方程式解释原因___________________。
(5)Z的氢化物与W的氢化物发生反应生成Z的单质和水,其化学方程式为_____________________。
(6)W、X、Y、Z四种元素原子半径由大到小的顺序是:________(用元素符号表示)。
(7)0.5 mol Q的单质与足量的W单质完全反应,放出196.75 kJ的热量。写出该反应的热化学方程式:____________________________________________。
高二化学综合题中等难度题查看答案及解析
-
已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素.其中A、B、C、D核电荷数之和为36,A、C原子的最外层电子数之和等于B原子 的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是_________。
a.B、C、D的原子半径由大到小的顺序为:D >C >B
b.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F都位于周期表的3区
(2)B单质有两种同素异形体.其中在水中溶解度较大的是_______(填化学式)。
(3)EA2和A2B熔点较高的是 _______(填化学式),原因是_________。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是____。下列分子或离子中与DB3结构相似的是____________。
a. NH3 b. SO32- c.NO3- d.PCl3
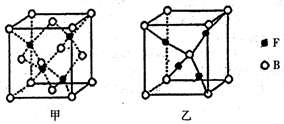
(5)已知B、F能形成两种化合物,其晶胞如下图所示.则高温时甲易转化为乙的原因为 ___________。若乙晶体密度为pg/cm3,则乙晶胞的晶胞边长a =________nm(用含P和NA的式子表示)
高二化学推断题困难题查看答案及解析