-
下列盐可由金属和盐酸反应直接制得的是( )
A. CuCl2 B. AlCl3 C. FeCl3 D. AgCl
难度: 中等查看答案及解析
-
现有X、Y、Z三种金属,已知:①X+YSO4=XSO4+Y ② Y+ 2ZNO3= Y(NO3)2+2Z ③ Y+ H2SO4不反应,则下列符合要求的X、Y、Z分别是( )
A. Mg、Zn、Ag B. Mg、Fe、Ag
C. Zn、Fe、Ag D. Fe、Cu、Ag
难度: 困难查看答案及解析
-
验证镁、铜的金属活动性顺序,下列试剂不能选用的是
A. MgSO4溶液 B. KCl溶液 C. 稀盐酸 D. ZnCl2溶液
难度: 中等查看答案及解析
-
某兴趣小组在研究Zn-Cu合金、Zn-Fe合金、Fe-Al合金、Fe-Cu合金时,发现其中一种合金6.5g与足量稀盐酸充分反应产生了0.5g气体,该合金可能是
A.Zn-Cu合金 B.Zn-Fe 合金 C.Fe-Al合金 D.Fe-Cu合金
难度: 困难查看答案及解析
-
合金具有许多优良的性能,下列材料不属于合金的是( )
A.生铁 B.玻璃钢 C.焊锡 D.18K 金
难度: 简单查看答案及解析
-
下列金属不能与CuSO4溶液反应的是( )
A.Ag B.Fe C.Zn D.Al
难度: 简单查看答案及解析
-
在已平衡的天平两边分别放一个等质量的烧杯,烧杯中装有等质量、等质量分数的足量稀盐酸,在左边烧杯中加入5.6g金属铁,在右边烧杯中加入5.5g镁和铜的混合物,充分反应后天平仍然保持平衡,则右边烧杯中加入的混合物中镁和铜的质量比为( )
A.36:19 B.12:43 C.24:31 D.13:42
难度: 困难查看答案及解析
-
通常状况下,颜色呈紫红色的金属是
A.铁 B.银 C.铜 D.铝
难度: 简单查看答案及解析
-
(2018雅安)下列关于金属的说法中,错误的是( )
A.铜有良好的导电性,常用于制作导线
B.所有的金属都能与稀盐酸反应
C.铁制品在干燥的空气中不易生锈
D.不能用铁桶盛放硫酸铜溶液
难度: 简单查看答案及解析
-
(2017长沙改编)下列关于金属材料的说法不正确的是( )
A.常温下,铝能与空气中的氧气反应,在其表面生成致密的氧化铝薄膜
B.铁片在海水中不易生锈
C.硬铝(铝合金)的硬度大于纯铝
D.金属资源的回收利用既保护了环境,又节约了金属资源
难度: 简单查看答案及解析
-
下列有关说法正确的是( )
A.光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡
B.将打磨好的铜丝在酒精灯上加热,铜丝表面由黑色变红色
C.将铜片放入硝酸银溶液,溶液由无色变为蓝色
D.将铁钉加入到稀硫酸中,溶液由无色变为黄色
难度: 中等查看答案及解析
-
(2018兰州)利用下列试剂之间的反应现象,能验证Fe、Cu、Ag三种金属活动性强弱顺序的是( )
A.Fe、Cu、AgNO3溶液
B.Fe、CuSO4溶液、Ag
C.FeSO4溶液、CuSO4溶液、Ag
D.Fe、CuSO4溶液、AgNO3溶液
难度: 中等查看答案及解析
-
如图是探究铁和铜金属活动性实验,关于此实验说法错误的是( )

A.铁丝需要砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性强弱:Fe>Cu
D.化学反应方程式为:Fe+CuSO4=Cu+FeSO4
难度: 中等查看答案及解析
-
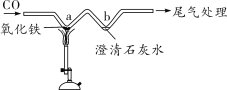
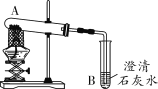
(2018杭州)如图为氢气还原氧化铜的实验装置图,下列有关分析正确的是( )
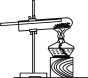
A.装置中试管口需略向下倾斜,主要是为了利于通入氢气
B.在给试管内药品加热前,需先通氢气排尽试管内的空气
C.待药品完全反应后,需同时撤去酒精灯和通氢气的导管
D.该实验装置也可直接用于一氧化碳还原氧化铜的实验
难度: 简单查看答案及解析
-
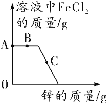
将等质量的铁粉和锌粉分别与等质量且溶质质量分数相等的稀盐酸充分反应,产生氢气的质量与时间的关系如图所示。下列说法正确的是( )
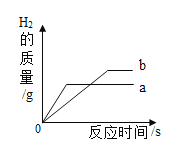
A.a表示铁与稀盐酸反应
B.a表示的反应,金属一定有剩余
C.b表示的反应,稀盐酸一定有剩余
D.若有一种金属剩余,则剩余的金属一定是铁
难度: 中等查看答案及解析
-
在一定量的硝酸银和硝酸铜溶液中加入锌粉,充分反应后过滤,得到滤液和滤渣,下列分析正确的是( )
A.如果滤液显蓝色,则滤渣一定没有Cu
B.如果滤渣只含一种金属,滤液中的溶质可能含有三种
C.在滤渣中加入稀盐酸有气泡产生,滤液中的溶质可能含有两种
D.在滤渣中加入稀盐酸没有气泡产生,则滤渣一定含有Ag和Cu
难度: 困难查看答案及解析
-
(2018贵港)把8.9 g Mg、Zn合金放入一定量的稀盐酸中,恰好完全反应,产生0.4 g H2,在上述反应后的溶液中滴入足量的NaOH溶液,充分反应后生成NaCl的质量为( )
A.23.4 g B.29.25 g C.30.5 g D.26.25 g
难度: 困难查看答案及解析
-
下列金属活动性最强的是( )
A.锌 B.铜 C.钾 D.金
难度: 简单查看答案及解析
-
根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是
A.用铁制容器盛盐酸 B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液 D.用铜制容器盛硝酸银溶液
难度: 中等查看答案及解析
-
(2018菏泽)现有X、Y、Z三种金属,将它们分别放入稀H2SO4中,只有X无氢气放出,将Y投入Z的盐溶液中,Y的表面没有发生变化,则X、Y和Z的金属活动性顺序正确的是( )
A.X>Y>Z B.Z>Y>X
C.X>Z>Y D.Y>Z>X
难度: 简单查看答案及解析
-
有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快,甲、丁无现象;再将甲投入丁的盐溶液中,甲的表面有丁析出,则这四种金属的活动性由强到弱的序为( )
A.甲>乙>丙>丁 B.丙>乙>甲>丁 C.丙>乙>丁>甲 D.丁>甲>乙>丙
难度: 中等查看答案及解析
-
(2017广安)下列现象和事实,可用金属活动性作出合理解释的是( )
①相同几何外形的金属镁、铝分别与相同浓度的稀盐酸反应,镁反应更剧烈,说明镁比铝的金属活动性强
②用硫酸铜、石灰水配制农药波尔多液时,不能用铁制容器盛放
③尽管金属的种类很多,但在自然界中,仅有少数金属(银、铂、金)以单质形式存在
④金属铝比金属锌更耐腐蚀,说明锌比铝的金属活动性强
A.①②③ B.①②
C.③④ D.①②③④
难度: 中等查看答案及解析
-
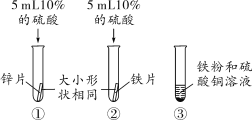
探究锌、铜、镁的金属活动性时,下列现象、分析或结论正确的是
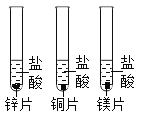
A.盐酸的浓度可以不同 B.铜片表面有气泡
C.镁片的试管表面发烫 D.活动性Cu>Zn>Mg
难度: 中等查看答案及解析
-
向氧化铜和铁粉的混合物中加入一定量稀硫酸,充分反应后过滤,向滤渣中再滴入稀硫 酸,有气泡产生,则下列判断正确的是
A.滤渣中可能含 Cu B.滤渣中只含 Fe
C.滤液中不含 CuSO4 D.滤液中不一定含 FeSO4
难度: 中等查看答案及解析
-
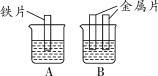
(2018衢州)小柯为比较Mg、Fe、Cu三种金属的活动性顺序,进行了如图甲所示的实验。实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤。滤液中含有的金属离子可能的组成有( )
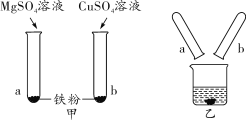
①Mg2+ ②Mg2+和Fe2+ ③Fe2+和Cu2+④Mg2+、Fe2+和Cu2+
A.①② B.①③ C.②④ D.③④
难度: 困难查看答案及解析
-
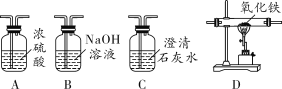
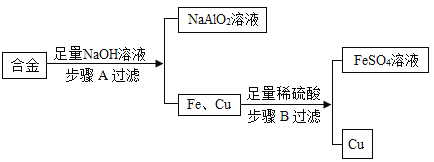
化学小组为探究铝、铜、银三种金属的活动性顺序,设计了如图所示实验方案。
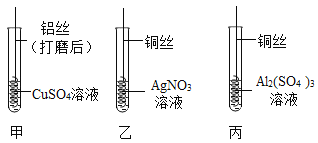
下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
D.实验甲中的CuSO4改为CuCl2不能完成本实验探究
难度: 中等查看答案及解析
-
(2017通辽)向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,下列说法正确的是( )
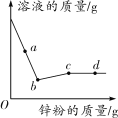
A.a点所得固体为银和铁
B.b点所得溶液中的溶质为硝酸银、硝酸亚铁和硝酸锌
C.c点所得溶液中的溶质为硝酸亚铁和硝酸锌
D.d点所得固体为银、铁和锌
难度: 困难查看答案及解析
-
(2018昆明)向AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn、Fe和Cu的混合粉末,充分反应后,过滤,洗涤,得到滤渣和滤液。下列说法正确的有( )
①滤渣中一定有Ag,滤液中可能有Fe(NO3)2、Cu(NO3)2、AgNO3
②当滤液为蓝色时,滤渣中一定有Cu、Ag,一定没有Zn、Fe
③向滤渣中加入盐酸,有气泡产生,则滤渣中一定有Fe、Cu、Ag,可能有Zn
④向滤液中加入KCl溶液,无明显现象,则滤液中一定有Zn(NO3)2,可能有Fe(NO3)2、Cu(NO3)2,滤渣中可能有Zn、Fe、Cu
A.1种 B.2种 C.3种 D.4种
难度: 困难查看答案及解析