-
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池.以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同.
A.①②
B.②③
C.②④
D.③④难度: 中等查看答案及解析
-
如表所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是( )
不纯物质 除杂试剂 分离方法 A 苯(甲苯) KMnO4(酸化),NaOH溶液 分液 B NH4Cl溶液(FeCl3) NaOH溶液 过滤 C 乙酸乙酯(乙酸) KOH溶液,水 分液 D 苯(苯酚) 浓Br2水 过滤
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
英国化学家波义耳1661年提出化学元素的概念,标志着近代化学的诞生.波义耳指出:我指的元素应当是某些不由任何其他物质所构成的原始和简单的物质或完全纯净的物质,是具有一定确定的、实在的、觉察到的实物,它们应该是用一般化学方法不能再分解为更简单的某些实物.从现代化学的观点看,波义耳定义的元素实际为( )
A.原子和分子
B.纯净物
C.单质
D.化合物难度: 中等查看答案及解析
-
下列化学用语的表示中,不正确的是( )
A.氢负离子(H-)结构示意图
B.氯化铵的电子式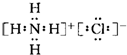
C.甲酸乙酯的结构简式:C2H5OOCH
D.N2的电子式难度: 中等查看答案及解析
-
五颜六色的颜色变化增添了化学的魅力,对下列有关反应的颜色叙述正确的是( )
①新制氯水久置后→浅黄绿色消失;②淀粉溶液遇单质碘→蓝色;③溴化银见光分解→银白色;④热的氧化铜遇乙醇→红色;⑤鸡蛋白遇浓硝酸→黄色;⑥苯酚在空气中氧化→粉红色.
A.①②③④⑤
B.②③④⑤⑥
C.①②④⑤⑥
D.①④⑤⑥难度: 中等查看答案及解析
-
下列各组物质,只用水不能加以区分的是( )
A.溴蒸气、二氧化氮两种气体
B.己烯、甲苯、四氯化碳三种液体
C.溴苯、苯、乙醛三种液体
D.氯化钠、无水硫酸铜、氢氧化钾三种固体难度: 中等查看答案及解析
-
已知乙烯分子的所有原子在一个平面上.乙酸在一定条件下能生成一种重要的有机试剂M.核磁共振光谱发现M分子中的氢原子没有差别,红外光谱发现M分子里存在羰基,且M分子中所有原子在一个平面上.M极易与水反应重新变为乙酸,则M分子的结构简式可能是( )
A.(CH3CO)2O
B.CH2=CO
C.CH3CHO
D.HCHO难度: 中等查看答案及解析
-
美丽的“水立方”(Water Cube)是北京奥运会游泳馆,采用膜材料ETFE(四氟乙烯和乙烯的共聚物),为场馆带来更多的自然光.下列说法正确的是( )
A.ETFE的结构中,存在-CF2-CF2-CH2-CH2-连接方式
B.四氟乙烯与乙烯发生缩聚反应得到ETFE
C.以乙烯为原料经过加成反应、氧化反应可制得乙二醇
D.ETFE材料是热固型(体型结构)的塑料难度: 中等查看答案及解析
-
下列有关同分异构体数目的叙述不正确的是( )
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种
B.与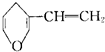 互为同分异构体的芳香族化合物有5种
互为同分异构体的芳香族化合物有5种
C.含有5个碳原子的某饱和链烃,其一氯取代物可能只有3种
D.菲的结构简式为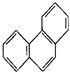 ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物 难度: 中等查看答案及解析
-
下列有关实验的操作过程,正确的是( )
A.钠与水的反应:用镊子从试剂瓶中取出金属钠,用小刀切下绿豆粒大小的一粒钠小心放入装满水的烧杯中
B.配制100mL的质量分数10%的H2O2溶液:取一支规格为100mL的量筒,先取质量分数为30%的双氧水溶液33.3mL,然后于加水至100mL刻度线
C.检验某浅绿色溶液中含有Fe2+离子:取该溶液少许,向其中加入KSCN溶液,不变红色;再向其中滴加氯水,溶液变为红色
D.取出分液漏斗中所需的上层液体:当下层液体从分液漏斗下端管口流出后,及时关闭活塞,然后更换一个接收容器,打开活塞将分液漏斗中的液体放出难度: 中等查看答案及解析
-
水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-═Fe3O4+S4O62-+2H2O,下列说法中,正确的是( )
A.x=2
B.参加反应的Fe2+全部作还原剂
C.每生成1molFe3O4,反应转移的电子总数为4mol
D.1molFe2+被氧化时,被Fe2+还原的O2的物质的量为mol
难度: 中等查看答案及解析
-
苯氯乙酮(
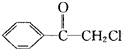 )是一种具有荷花香味的有机物,苯氯乙酮可能发生的化学反应类型有( )
)是一种具有荷花香味的有机物,苯氯乙酮可能发生的化学反应类型有( )
①加成反应 ②取代反应 ③消去反应 ④水解反应 ⑤银镜反应.
A.①②③
B.②③④
C.②③⑤
D.①②④难度: 中等查看答案及解析
-
由溴乙烷制取乙二醇.依次发生的反应类型是( )
A.取代、加成、水解
B.消去、加成、取代
C.水解、消去、加成
D.消去、水解、取代难度: 中等查看答案及解析
-
某种高分子化合物的结构简式如图所示:合成它的单位可能有:①对苯二甲酸,②对苯二甲酸甲酯,③丙烯醇,④丙烯,⑤乙烯.
其中正确的一组是( )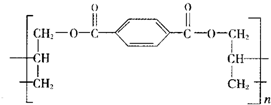
A.①②
B.④⑤
C.①③
D.②④难度: 中等查看答案及解析
-
有机物A、B只可能为烃或烃的含氧衍生物,等物质的量的A和B完全燃烧时,消耗氧气的量相等,则A和B的分子量相差不可能为(n为正整数)( )
A.8n
B.14n
C.18n
D.44n难度: 中等查看答案及解析
-
把一定量的Na2O2的NaHCO3的混合粉末分为两等份,将其中一份加入100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为2.24L(标准状况下);再将此气体通入另一份混合物中,充分反应后,得到O2 2.016L(标准状况下),则原混合粉末中Na2O2和NaHCO3的物质的量之比及稀盐酸的物质的量浓度是( )
A B C D Na2O2和NaHCO3的物质的量之比 8:1 9:2 8:1 2:9 原稀盐酸的物质的量的浓度 1.4 1.4 1.8 1.3
A.A
B.B
C.C
D.D难度: 中等查看答案及解析