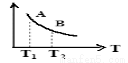-
下列说法中正确的是
A.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
B.升高温度能降低反应活化能,所以反应速率加快
C.中和热测定实验中需要用到的玻璃仪器有烧杯、温度计和环形玻璃棒搅拌棒三种
D.等量的CH4在氧气中燃烧放出的热量与形成燃料电池放出的热量一样多
难度: 简单查看答案及解析
-
下列关于电化学的实验事实正确的是
出现环境
实验事实
A.
以稀H2SO4为电解质的Cu-Zn原电池
Cu为正极,正极上发生还原反应
B.
用惰性电极电解CuCl2溶液
在阳极有红色固体物质析出
C.
弱酸性环境下钢铁腐蚀
负极处产生H2,正极处吸收O2
D.
将钢闸门与外加电源负极相连
牺牲阳极的阴极保护法,可防止钢闸门腐蚀
难度: 中等查看答案及解析
-
下列依据热化学方程式得出的结论正确的是
A.已知C(石墨, s)=C(金刚石, s); ΔH>0,则金刚石比石墨稳定
B.2H2(g)+O2(g)=2H2O(g);ΔH=-483.6kJ/mol,则氢气的燃烧热为241.8kJ•mol-1
C.500℃、30MPa下,N2(g)+3H2(g)
2NH3(g)ΔH=-38.6kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量19.3kJ
D.H2(g)+F2(g)=2HF(g) ΔH = -270kJ•mol-1,则相同条件下,2molHF气体的能量小于1mol氢气和1mol氟气的能量之和
难度: 中等查看答案及解析
-
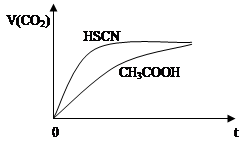
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
难度: 中等查看答案及解析
-
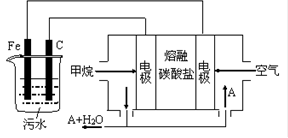
微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,
电极反应式为:Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-,
总反应式为:Ag2O+Zn===ZnO+2Ag 根据上述反应式,判断下列叙述中正确的是
A.在使用过程中,电池负极区溶液的pH增大
B.在使用过程中,电子由Ag2O经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn极发生还原反应,Ag2O极发生氧化反应
难度: 中等查看答案及解析
-
下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是
A
B
C
D
强电解质
Fe
NaCl
CaCO3
HNO3
弱电解质
CH3COOH
NH3
H3PO4
Fe(OH)3
非电解质
C12H22O11(蔗糖)
BaSO4
C2H5OH
H2O
难度: 简单查看答案及解析
-
某温度下,密闭容器中,发生如下可逆反应:2E(g)
F(g)+xG(g);
ΔH<0。若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5a mol/L;若E的起始浓度改为2a mol/L,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
A.若x=l,容器体积保持不变,新平衡下E的体积分数为50%
B.升高温度时,正反应速率加快、逆反应速率减慢
C.若x=2,容器体积保持不变,新平衡下F的平衡浓度为0.5a mol·L-1
D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol
难度: 困难查看答案及解析
-
如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是

A.K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B.K1闭合,石墨棒周围溶液pH逐渐降低
C.K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
D.K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体
难度: 中等查看答案及解析
-
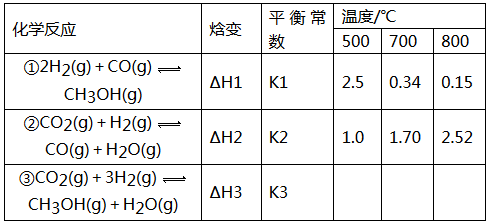
700℃时,H2(g)+CO2(g)
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示.其中甲经2min达平衡时,v(H2O)为0.025mol/(L•min),下列判断不正确的是
起始浓度
甲
乙
丙
c(H2)/mlo/L
0.10
0.20
0.20
c(CO2)/mlo/L
0.10
0.10
0.20
A.平衡时,乙中CO2的转化率大于50%
B.当反应平衡时,丙中c(CO2)是甲中的2倍
C.温度升至800℃,上述反应平衡常数为25/16 ,则正反应为吸热反应
D.其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/LCO2,到达平衡时c(CO)与乙不同
难度: 困难查看答案及解析
-
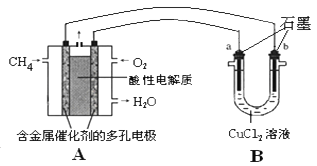
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH–4e- + H2O = CH3COOH + 4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O
D.正极上发生的反应为:O2 + 4e- + 2H2O = 4OH-
难度: 中等查看答案及解析
-
在1.0L密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g)
Y(g)+Z(g)△H<0容器内气体总压强p随反应时间t的变化关系如下图所示.以下分析正确的是
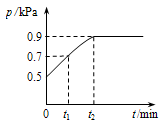
A.从反应开始到t1时的平均反应速率v(X)=0.2/t1mol/(L•min)
B.该温度下此反应的平衡常数K=0.32mol/L
C.欲提高平衡体系中Y的含量,可升高体系温度或减少Z的量
D.其他条件不变,再充入0.1 mol 气体X,平衡正向移动,X的转化率增大
难度: 困难查看答案及解析
-
现有室温下的四种溶液,其pH如下表所示,下列有关叙述不正确的是
①
②
③
④
pH
11
11
3
3
溶液
氨水
NaOH溶液
醋酸
盐酸
A.③④中分别加入适量醋酸钠晶体,两溶液pH均增大
B.②③两溶液等体积混合,所得溶液中:c(OH-)>c(H+)
C.分别加水稀释10倍,溶液的pH:①>②>④>③
D.V1L④和V2L①溶液混合后,若pH=7,则V1<V2
难度: 中等查看答案及解析
-
用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲,电解过程中的实验数据如图乙。横坐标表示转移电子的物质的量,纵坐标表示产生气体的总体积(标准状况)。则下列说法不正确的是

A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的反应方程式为:4OH--4e- = 2H2O+O2↑
C.从开始到Q点时收集到的混合气体的平均摩尔质量为12 g/ mol
D.从开始到P点收集到的气体是O2
难度: 困难查看答案及解析
-
某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。据图判断错误的是
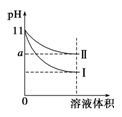
A.a的数值一定大于9
B.Ⅱ为氨水稀释时溶液的pH变化曲线
C.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
D.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水)
难度: 困难查看答案及解析
-
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
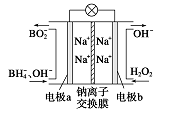
A.电池放电时Na+从a极区移向b极区
B.每消耗3 mol H2O2,转移的电子为3 mol
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
D.该电池的负极反应为
难度: 中等查看答案及解析
-
下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是

A.①是其它条件一定时,反应速率随温度变化的图象,正反应△H<0
B.②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C.③是在有无催化剂存在下建立的平衡过程图象,曲线a是使用催化剂的曲线
D.④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2
难度: 困难查看答案及解析
-
某密闭容器中充入等物质的量的A和B,一定温度下发生反应[A(g)+xB(g)
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
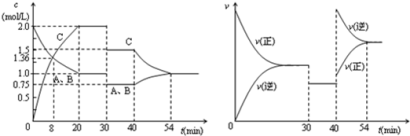
A.30min~40min间该反应使用了催化剂
B.30min时降低温度,40min时升高温度
C.反应方程式中的x=1,正反应为放热反应
D.8min前A的平均反应速率为0.08mol/(L•min)
难度: 困难查看答案及解析
-
用惰性电极电解煤浆液的方法制H2的反应为C(s)+2H2O(l)=CO2(g)+2H2(g)。现将一定量的1mol/LH2SO4溶液和适量煤粉充分混合,制成含碳量为0.02g/mL~0.12g/mL的煤浆液,置于如图所示装置中进行电解(两电极均为惰性电极)。下列说法错误的是
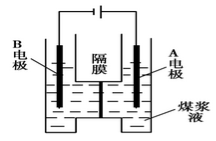
A.A极是阳极,B极为阴极
B.A极的电极反应式为C+2H2O-4e-=CO2↑+4H+
C.B极的电极反应式为2H++2e-=H2↑
D.电解一段时间后,煤浆液的pH增大
难度: 中等查看答案及解析