-
下列现象不能用氢键解释的是
A.冰的密度比水小,浮于水面 B.氨气易液化
C.乙醇极易溶于水 D.碘易溶于苯(C6H6)
难度: 简单查看答案及解析
-
下列各组物质的晶体中,化学键种类相同,晶体类型也相同的是
A.MgO和BaO2 B.SO2和SiO2 C.KOH和NH4Cl D.CCl4和KCl
难度: 简单查看答案及解析
-
下列分子的中心原子的杂化类型与其他不同的是
A.SiCl4 B.H2S C.PCl5 D.NH3
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.前四周期中,原子最外层为1个电子的元素有5种
B.Fe2+的价电子排布为3d6
C.2p轨道上有1个未成对电子的原子与3p轨道上有1个未成对电子的原子化学性质相似
D.AB3型分子的中心原子A采取sp3杂化
难度: 简单查看答案及解析
-
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3; ③1s22s22p3; ④1s22s22p5。则下列有关比较中正确的是
A.第一电离能:①>② B.原子半径:④>③
C.电负性: ②>③ D.氢化物稳定性:①>②
难度: 简单查看答案及解析
-
下列粒子(或化学键)的数目之比不是1∶1的是
A.氘原子中的质子和中子
B.Na2O2固体中的阴离子和阳离子
C.CO2分子中的σ键和π键
D.常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH-
难度: 简单查看答案及解析
-
下列关于粒子结构的描述正确的是
A.NF3和BF3是中心原子杂化类型相同的极性分子
B.CH2Cl2和C2H4是空间构型不同的非极性分子
C.在SiO2晶体中,Si原子与Si—O键数目比为1︰2
D.CF4和CO2是含极性键的非极性分子
难度: 中等查看答案及解析
-
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是
A.该物质的分子式为SN B.该物质的晶体中微粒间作用力有2种
C.该物质具有很高的熔、沸点 D.该物质与化合物S2N2互为同素异形体
难度: 中等查看答案及解析
-
下列说法正确的是
A.沸点:H2O>H2S>H2Se>H2Te B.稳定性:SiH4>PH3>H2S >HCl
C.熔点:SiC >KCl> I2>CO2 D.沸点:CH4 >SiH4>GeH4>SnH4
难度: 简单查看答案及解析
-
X、Y、Z是短周期的三种主族元素,在周期表中的相对位置如图所示,下列说法正确的是
X
Y
Z
A.原子半径:X<Y<Z
B.X、Y、Z三种元素的最高价氧化物对应水化物中最多有一种强酸
C.X的气态氢化物的稳定性比Y的气态氢化物强
D.常温下X、Y、Z的单质不可能均与盐酸反应
难度: 中等查看答案及解析
-
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm ,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,
下列说法正确的是( )
X
Y
W
A.元素Z处于周期表的阴影位置
B.X与W形成的化合物熔点很高,为离子化合物
C.X、W的最高价氧化物对应水化物的酸性: X>W
D.Y、W的最高价氧化物的晶体类型相同
难度: 中等查看答案及解析
-
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
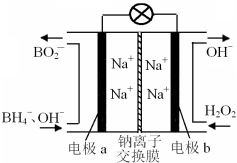
A.电池放电时Na+从b极区移向a极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.该电池的负极反应为:BH4-+ 8OH-+8e-→BO2-+ 6H2O
D.每消耗3 mol H2O2,转移的电子为3 mol
难度: 中等查看答案及解析
-
下列说法不正确的是
A.氯化钠晶体中,每个Cl-周围最近且距离相等的Cl-共有12个
B.分子晶体中有范德华力,也有共价键
C.干冰晶体中,每个CO2分子周围最近且距离相等的CO2分子共有12个
D.晶体熔点:晶体硅<SiC
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
B.滴入酚酞试液显红色的溶液中:K+、Fe3+、ClO-、SO42-
C.c(H+)/c(OH-)=1×1012的溶液中:NH4-、Cl-、NO3-、Al3+
D.由水电离出的c(H+)=1×10-12mol/L的溶液中:Na+、K+、Cl-、HCO3-
难度: 中等查看答案及解析
-
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A.加入KSCN溶液一定不变红色 B.溶液中一定含Cu2+
C.溶液中一定含Fe2+ D.剩余固体中一定含铜
难度: 简单查看答案及解析
-
常温下,向20.00 mL 0.100 mol·L-1CH3COONa溶液中逐滴加入0.100 mol·L-1盐酸,溶液的pH与所加入盐酸体积的关系如图所示(不考虑挥发)。下列说法正确的是
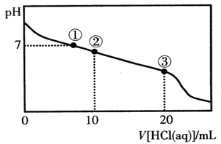
A.点①所示溶液中:c(Na+)=c(Cl-)>c(H+)=c(OH-)
B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C.点③所示溶液中:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-)
D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COO-)+c(CH3COOH)
难度: 困难查看答案及解析