-
X元素最高价氧化物对应的水化物为H3XO4,则它对应的气态氢化物为( )
A. HX B. H2X C. XH4 D. XH3
难度: 中等查看答案及解析
-
对元素周期表和元素周期律的发现有突出贡献的科学家是( )
A. 拉瓦锡 B. 门捷列夫 C. 阿伏加德罗 D. 道尔顿
难度: 简单查看答案及解析
-
下列关于元素周期表的叙述,正确的是( )
A. 周期表是按各元素的相对原子质量递增的顺序从左到右排列的
B. 每一周期的元素都是从碱金属开始,以稀有气体结束
C. 最外层电子数为2的元素都位于第ⅡA族
D. 在已经发现的元素中,金属元素种类比非金属元素多
难度: 中等查看答案及解析
-
如图带漏斗U型管中装有足量的煤油和水的混合物,静置后投入一小块碱金属.可观察到金属在煤油和水的界面a附近上下往复运动,下列说法不正确的是( )
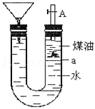
A. 此碱金属可能是钾或钠
B. 反应一段时间煤油会燃烧
C. 碱金属上下运动是由于与水反应产生了氢气
D. 若是金属锂则不能观察到上述现象
难度: 困难查看答案及解析
-
下列关于F、Cl、Br、I性质的比较,不正确的是( )
A. 单质的颜色随核电荷数的增加而加深
B. 单质的熔、沸点随核电荷数的增加而升高
C. 单质的氧化性减弱
D. 它们的氢化物的稳定性随核电荷数的增加而增强
难度: 中等查看答案及解析
-
在下列分子结构中,所有原子的最外层电子不能满足8电子稳定结构的是( )
A.H2O B.PCl3 C.N2 D.CO2
难度: 中等查看答案及解析
-
下列互为同位素的是( )
A. H2D2 B. 14N14C C. 16O17O D. 金刚石石墨
难度: 简单查看答案及解析
-
下列微粒半径大小比较正确的是( )
A. Na+<Mg2+<Al3+<O2﹣
B. S2﹣>Cl﹣>Na+>Al3+
C. Na<Mg<Al<S
D. Ca<Rb<K<Na
难度: 中等查看答案及解析
-
下列反应能说明卤素的活泼性顺序的是( )
①2HClO4+Br2(g)═2HBrO4+Cl2
②2NaBr+Cl2═NaCl+Br2
③2KI+Cl2═2KCl+I2④2KI+Br2═2KBr+I2.
A. ①②③ B. ①②④ C. ②③④ D. ①②③④
难度: 中等查看答案及解析
-
已知1~18号元素的离子aW3+、bX+、cY2﹣、dZ﹣都具有相同的电子层结构,下列关系正确的是( )
A. 质子数:c>d
B. 离子的还原性:Y2﹣>Z﹣
C. 氢化物的稳定性:H2Y>HZ
D. 原子半径:X<W
难度: 中等查看答案及解析
-
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
B
C
D
A.简单离子的半径大小关系:B>C>E
B.D元素的气态氢化物比C元素的气态氢化物稳定
C.由A、B、C三种元素组成的离子化合物中,阴、阳离子个数比为1:1
D.A、D、E均可形成两种常见氧化物
难度: 中等查看答案及解析
-
下列有关离子键和离子化合物的说法正确的是( )
A.凡含离子键的化合物,一定含金属元素
B.在化合物MgCl2中,两个氯离子之间也存在离子键
C.离子化合物中不可能有共价键
D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键
难度: 中等查看答案及解析
-
下列有关元素性质比较正确的是( )
A. 碱性:NaOH<Mg(OH)2<Al(OH)3
B. 氢化物稳定性:HF>HCl>PH3
C. 原子半径:S>F>O
D. 酸性:HClO>HNO3>H2CO3
难度: 中等查看答案及解析
-
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.原子核内有10个中子的氧原子:
O
B.氧的原子结构示意图:
C.NaCl的电子式:
D.质量数为37的氯原子:
Cl
难度: 简单查看答案及解析
-
下列表示电子式的形成过程正确的是( )
A.
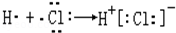
B.
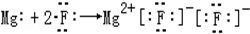
C.

D.
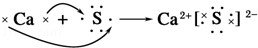
难度: 中等查看答案及解析
-
下列物质中,既有离子键又有共价键的是( )
A.CaCl2 B.KOH C.H2O D.HF
难度: 中等查看答案及解析
-
下列有关化学键的叙述,正确是的( )
A.共价化合物中可以含有离子键
B.单质分子中均不存在化学键
C.含活泼金属元素的化合物可能是共价化合物
D.含有共价键的化合物一定是共价化合物
难度: 中等查看答案及解析
-
下列电子式书写正确的是( )
A.氯化钠
B.氨气
C.NH4Cl的电子式
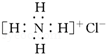
D.硫化钠
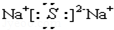
难度: 中等查看答案及解析
-
在下列各组化合物中,化学键类型相同的是( )
A.HCl和MgCl2 B.H2O和CO2 C.CO2和NaCl D.F2和NaF
难度: 简单查看答案及解析
-
实现下列变化,需克服相同类型作用力的是( )
A.石墨和氯化钠分别受热熔化
B.冰的融化和水的分解
C.NaCl和HCl溶于水
D.干冰和碘的升华
难度: 中等查看答案及解析
-
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A.NH4Cl→NH3↑+HCl↑
B.NH3+CO2+H2O→NH4HCO3
C.2NaOH+Cl2→NaCl+NaClO+H2O
D.2Na2O2+2CO2→2Na2CO3+O2
难度: 中等查看答案及解析
-
新能源的开发利用是人类社会可持续发展的重要课题.下列属于新能源的是( )
A.氢气 B.煤炭 C.天然气 D.石油
难度: 简单查看答案及解析
-
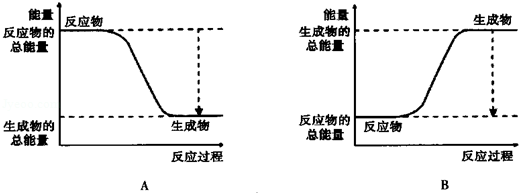
下列反应符合如图所示的反应是( )
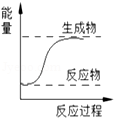
A.金属钠与水的反应
B.氢气燃烧
C.浓硫酸的稀释
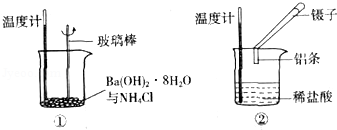
D.Ba(OH)2•8H2O和NH4Cl (固体)混合
难度: 中等查看答案及解析
-
下列说法正确的是( )
①需要加热才能发生的反应一定是吸热反应
②放热的反应在常温下一定很容易发生
③反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
④放热反应加热到一定温度引发后,停止加热反应也能继续进行.
A.①②③④ B.只有①② C.只有③④ D.②③④
难度: 中等查看答案及解析
-
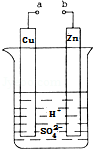
如图为水果电池的示意图,下列说法正确的是( )
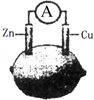
A.锌片作负极,质量逐渐减少
B.电子由铜片沿导线流向锌片
C.铜电极逐渐溶解
D.该装置能将电能转化为化学能
难度: 中等查看答案及解析