-
2018年环境日我国主题是“美丽中国,我是行动者”,共建天蓝、地绿、水清的美丽中国。下列建议不可行的是
A. 垃圾分类回收 B. 禁止使用化肥、农药,以防止水体污染
C. 城市道路定时洒水,以减少PM2.5的含量 D. 出行尽量选择步行或骑“共享单车”
难度: 简单查看答案及解析
-
下列人体所缺元素与引起的健康问题关系正确的是
A. 缺铁会引起贫血 B. 缺碘会引起龋齿
C. 缺锌会导致甲状腺疾病 D. 缺钙会导致侏儒症
难度: 简单查看答案及解析
-
粗盐提纯的实验操作中正确的是
A.
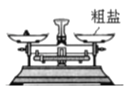 称量粗盐 B.
称量粗盐 B.  量取9.5mL水
量取9.5mL水C.
 过滤 D.
过滤 D. 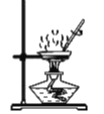 蒸发
蒸发难度: 简单查看答案及解析
-
下列化学用正确的是
A. 4 个氢原子:2H2 B. l 个锌离子:Zn2
C. 碳酸钠:NaCO3 D. 3 个氮气分子:3N2
难度: 简单查看答案及解析
-
亮氨酸(C6H13NO2)是人体必需的氨基酸之一,下列有关亮氨酸的说法错误的是
A. 由4种元素组成 B. 碳元素的质量分数最大 C. 含有氧分子 D. 碳、氧元素的质量比为9︰4
难度: 简单查看答案及解析
-
诗句“遥知不是雪,为有暗香来”中“暗香来”的主要原因是
A. 分子间有间隔 B. 分子在不断运动 C. 分子分解成原子 D. 分子的质量很大
难度: 简单查看答案及解析
-
下列家庭小实验不.能.成功的是( )
A. 用食盐水除去热水瓶中的水垢(主要成分是碳酸钙)
B. 用冷碟压在蜡烛火焰上,证明蜡烛中含有碳元素
C. 用加热的方法鉴别真黄金和假黄金(铜锌合金)
D. 将铁钉分别半浸没于纯水和白醋中,比较生锈的快慢
难度: 中等查看答案及解析
-
物质的性质决定其用途,下列说法不正确的是
A. 甲烷作燃料,是因为甲烷具有可燃性 B. 铜作导线,是因为铜具有良好的导电性
C. 洗洁精洗涤油污,是因为洗洁精能溶解油污 D. 活性炭除冰箱异味,是因为活性炭具有吸附性
难度: 简单查看答案及解析
-
“铜绿”受热时发生如下反应:Cu2(OH)2CO3
2X+CO2↑+H2O。下列有关说法正确的是( )
A. X的化学式为Cu2O
B. 反应前后元素的种类发生改变
C. 反应后固体质量减少,不遵守质量守恒定律
D. 反应后固体中铜元素的质量分数增大
难度: 简单查看答案及解析
-
在如图气密性良好的装置中充满了二氧化碳气体,往2支试管中分别缓缓注入5mL紫色石蕊试液和5mL澄清石灰水。下列有关叙述不正确的是

A. 左边试管内液体变红色
B. 右边试管内石灰水有浑浊现象产生
C. 充分反应后,U型管中的液面左边高于右边
D. 相同体积的水和石灰水,石灰水吸收的二氧化碳较多
难度: 简单查看答案及解析