-
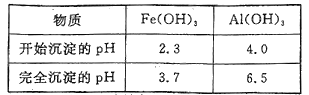
某化工厂制备净水剂硫酸铁铵晶体[NH4Fe(SO4)2·6H2O]的一种方案如下:
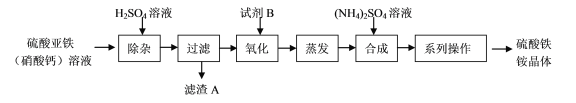
下列说法不正确的是
A. 滤渣A的主要成分是CaSO4
B. 相同条件下,NH4Fe(SO4)2·6H2O净水能力比FeCl3强
C. “合成”反应要控制温,温度过高,产率会降低
D. “系列操作”包括蒸发浓缩、降温结晶、过滤、干燥等
难度: 中等查看答案及解析
-
NA代表阿伏加德罗常数的值。下列有关说法正确的是
A. 1L0.1mol·L-1 NaHSO3溶液中含S原子的粒子个数为0.1NA
B. 标准状况下,6.72LNO2通入足量水中充分反应,转移电子数为0.6NA
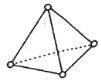
C. 28gN4(如图所示)含N一N键数目为2NA
D. 1L0.5mol·L-1pH=7的CH3 COONH4溶液中NH4+数目为0.5NA
难度: 中等查看答案及解析
-
某抗结肠炎药物的有效成分(R)的结构简式如下。下列说法不正确的是

A. R能发生加成、取代反应
B. R分子中所有C和N原子一定共平面
C. R的苯环上官能团位置异构体有10种
D. R的分子式为C7H7O3N
难度: 中等查看答案及解析
-
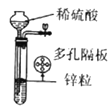
文献报道,H2能还原FeCl2。某学习小组设计实验探究“文献”的真实性,下列装置错误的是
A.
 B.
B. 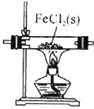
C.
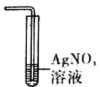 D.
D. 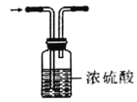
难度: 中等查看答案及解析
-
某实验小组模拟光合作用,采用电解CO2和H2O的方法制备CH3CH2OH和O2装置如图所示。下列说法不正确的是
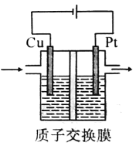
A. 铂极为阳极,发生氧化反应
B. 电解过程中,H+由交换膜左侧向右侧迁移
C. 阴极的电极反应式为2CO2+12H++12e-====CH3CH2OH+3H2O
D. 电路上转移2mol电子时铂极产生11.2LO2(标准状况)
难度: 中等查看答案及解析
-
短周期元素a、b、c、d的原子序数依次增大。a、b能组成常温下呈液态的两种常见化合物。b和d位于同主族。已知:a2b和c2d3混合发生剧烈反应生成白色沉淀和无色气体。下列说法正确的是
A. 气态氢化物稳定性:d>b B. 原子半径:d>c>b>a
C. a2db3化合物能促进水电离 D. 工业上电解熔融c2b3冶炼c单质
难度: 中等查看答案及解析
-
常温下,二甲胺[(CH3)2NH·H2O]是一元弱碱,其电离常数Kb=1.6×10-4。10 mL c mol·L-1二甲胺溶液中滴加0.1mo1·L-1盐酸,混合溶液的温度与盐酸体积的关系如图所示。下列说法不正确的

A. 二甲胺溶液的浓度为0.2mol·L-1
B. 在Y和Z点之间某点溶液pH=7
C. Y点存在:c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-)
D. 常温下,(CH3)2NH2Cl水解常数Kh≈5.0×10-11
难度: 困难查看答案及解析



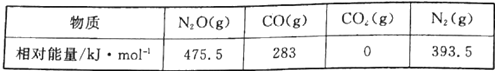
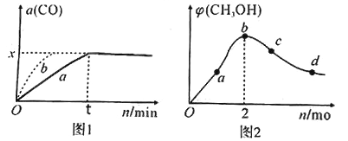
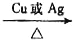 CH3CHO+H2↑。CH3CH2OH的沸点高于CH3CHO的主要原因是________;从原子轨道重叠方式分类,H2分子中σ键类型是____________。
CH3CHO+H2↑。CH3CH2OH的沸点高于CH3CHO的主要原因是________;从原子轨道重叠方式分类,H2分子中σ键类型是____________。
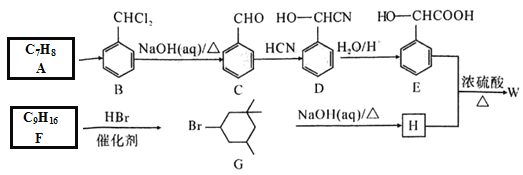
 ,设计合成路线(其他试剂自选):______________。
,设计合成路线(其他试剂自选):______________。