-
联合国将2019年定为“国际化学元素周期表年”,这是为了纪念
A.门捷列夫 B.居里夫人 C.拉瓦锡 D.卢瑟福
难度: 简单查看答案及解析
-
人类从自然界获取物质的下列变化中,属于化学变化的是
A.冶铁炼钢 B.工业制氧 C.海水晒盐 D.沙里淘金
难度: 简单查看答案及解析
-
《天工开物》中记载“每金七厘造方寸金一千片”,体现了黄金具有良好的
A.磁性 B.延展性 C.导热性 D.导电性
难度: 简单查看答案及解析
-
生活中常见的下列物质,属于溶液的是
A.牛奶 B.白酒 C.泥浆 D.蒸馏水
难度: 简单查看答案及解析
-
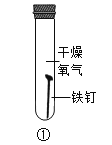
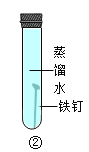
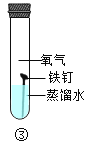
下列实验操作中,正确的
A.
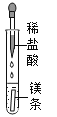 B.
B.C.
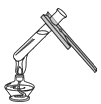 D.
D.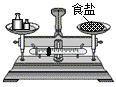
难度: 简单查看答案及解析
-
下列物质中,属于合金的是
A.赤铁矿 B.水银 C.四氧化三铁 D.不锈钢
难度: 中等查看答案及解析
-
下列溶液中,导电性最弱的是
A.蔗糖溶液 B.氯化钠溶液 C.硫酸溶液 D.氢氧化钠溶液
难度: 中等查看答案及解析
-
以下化学用语正确的是
A.两个氯原子:Cl2 B.三个亚铁离子 :3Fe2+
C.8个硫原子构成的一个硫分子:8S D.+6价硫元素形成的氧化物:SO6
难度: 中等查看答案及解析
-
配制化妆品时,为使油脂均匀悬浮在水中,需要添加
A.催化剂 B.吸附剂 C.消毒剂 D.乳化剂
难度: 简单查看答案及解析
-
“粗盐提纯实验”中不需要使用的仪器是
A.酒精灯 B.蒸发皿 C.玻璃棒 D.集气瓶
难度: 中等查看答案及解析
-
在给定条件下,下列转化不能实现的是
A.Al
Al2O3 B.H2O
H2
C.KMnO4
O2 D.Fe
Fe2O3
难度: 中等查看答案及解析
-
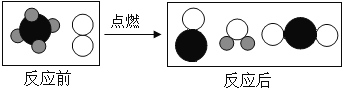
将下列各组气体的混合气点燃,可能发生爆炸的是
A.H2、CO B.CO、CO2 C.H2、O2 D.N2、O2
难度: 中等查看答案及解析
-
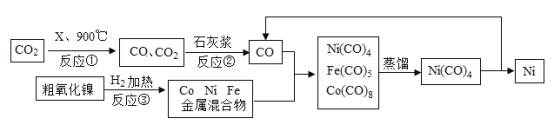
师昌绪院士是我国高温合金研究的莫基人,曾荣获国家最高科学技术奖,为我国的金属和材料学作出了巨大贡献。以下对某种高温合金(含铁、铬、镍、钻、碳元素)。理解错误的是
A.至少含四种金属元素 B.硬度一定比纯铁小
C.可用于造某些设备的高温部件 D.与足量稀盐酸反应后有固体物质剩余
难度: 中等查看答案及解析
-
下列关于工业炼铁的叙述中错误的是
A.使用的设备是高炉 B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是:2Fe2O3+3C===4Fe+3CO2↑ D.主要产物为生铁
难度: 中等查看答案及解析
-
下图是A、B两物质的溶解度曲线,下列信息中,正确的是
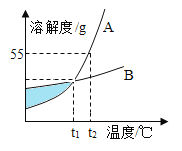
A.t1℃时,A、B两物质溶解度相同
B.t2℃时,A物质的饱和溶液中溶质的质量分数为55%
C.除去固体A中的少量杂质B可采取蒸发结晶法
D.图中阴影部分表明A、B两溶液都是饱和溶液
难度: 中等查看答案及解析
-
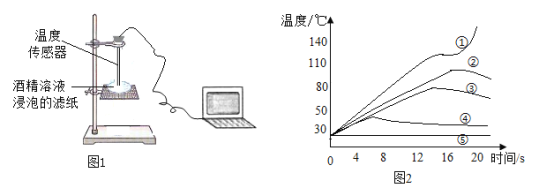
在下图1所示密闭装置内燃烧红磷测定空气中氧气含量,用传感器记录集气瓶中压强随时间变化的情况,得图2所示数据。下列说法正确的是
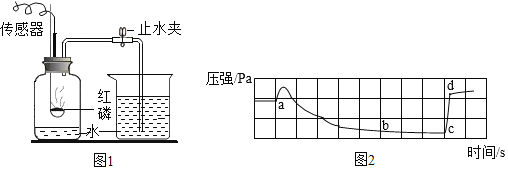
A.a点处压强增大主要是因为少量空气进入 B.a→b段压强减小的原因只能是氧气被消耗
C.c点时打开了弹簧夹,导致气压增大 D.d点集气瓶中的温度一定等于室温
难度: 中等查看答案及解析
-
为了回收硫酸铜废液中的铜,称取m克铁粉与一定体积的硫酸铜废液混合,充分反应后过滤、洗涤、干燥,得到的固体一部分能被磁铁吸引;再将该固体与足量的稀硫酸混合,充分反应后,过滤、洗涤、干燥,得到不能被磁铁吸引的固体m克。则整个过程中参加反应的CuSO4与H2SO4的质量之比为
A.80:63 B.80:49 C.80:7 D.16:7
难度: 困难查看答案及解析