-
化学与社会、科学、技术等密切相关,下列说法正确的
A. 瓷器属硅酸盐产品,china一词又指“瓷器”,这反映了在世界人眼中,中国作为“瓷器故乡“的形象
B. “青蒿一握,以水二升渍;绞取汁”,屠呦呦对青蒿素的提取属于化学变化
C. “一带一路”是“丝绸之路经济带”和“21世紀海上丝绸之路”的简称。丝绸的主要成分是天然纤维素,属于高分子化合物
D. 制作“嫦娥”太空飞行器使用的碳纤维复合材料是一种新型有机高分子材料
难度: 中等查看答案及解析
-
金刚烷具有类似樟脑气味的无色晶体,其衍生物在医药方面有着重要的用途。以化合物X为起始原料没生一系列反应制得金刚烷(Z)的过程如图所示,下列说法不正确的是
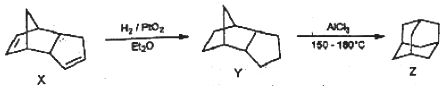
A. X的分子式为C10H12
B. X生成Y的反应为还原反应
C. Y和Z互为同分异构体
D. Z和环已烷属于同系物
难度: 中等查看答案及解析
-
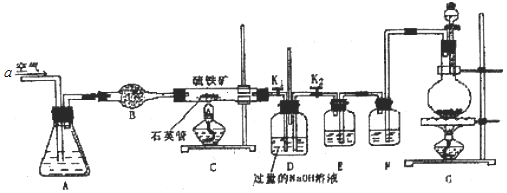
用下列实验装置进行相应的实验,能达到实验目的是
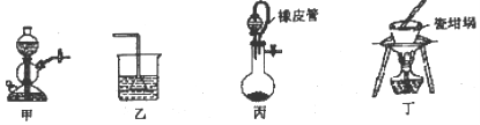
A. 实验室用甲装置制取氯气
B. 盛有水的乙装置,吸收NH3气体
C. 用丙装置对生成的气体体积进行测量可以减少误差
D. 用丁装置灼烧FeSO4•7H2O晶体得到固体FeSO4
难度: 中等查看答案及解析
-
NA是阿伏加德罗常数的值。下列说法一定正确的是
A. 在一密闭容器中充入2mol SO2和1mol O2,充分反应后分子总数为2NA
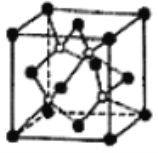
B. 常温常压下,124g P4(正四面体结构)中所含P﹣P键数目为4NA
C. 标准状况下,11.2L氯气和一氧化碳组成的混合气体所含原子数为NA
D. 常温常压下,92g C2H6O中所含乙醇分子数为2NA
难度: 中等查看答案及解析
-
氟利昂是饱和碳氢化合物的卤族衍生物的总称,其破坏臭氧层的化学反应机理如下(以二氯二氟甲烷为例,二氯二氟甲烷可由四氯化碳与氟化氢在催化剂存在下、控制回流冷凝温度为﹣5℃时得到):
①CF2Cl2
CF2Cl+Cl
②Cl+O3→ClO+O2
③ClO+ClO→ClOOCl(过氧化氯)
④ClOOCl
2Cl+O2
下列说法中不正确的是
A. 紫外线使CF2Cl2分解产生的是臭氧生成氧气的催化剂
B. 反应③中的氯子与反应④中生成的氯原子化学性质相同
C. ClOOCl分子中各原子最外层均达到8电子稳定結构
D. 气态氢化物的稳定性:HF>H2O>HCl
难度: 中等查看答案及解析
-
用以葡萄糖为燃料的生物燃料电池甲与盛有足量硫酸铜溶液的装置乙相连,起始电路接入状况如图以电流强度0.1A,通电10min后,将电池的正、负极互换接入,移动滑动变阻器:以电强度0.2A,继续通电10min,结束实验。下列有关说法正确的是
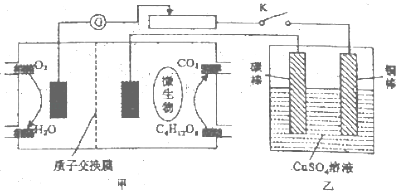
A. 葡萄糖在装置甲的正极参加反应,氧气在负板参加反应
B. 在该电池反应中,每消耗1mol氧气理论上能生成标准状况下二氧化碳11.2L
C. 电池工作20min时,乙装置电极析出固体和电极上产生气体的质量比为2:1
D. 电池工作15分钟时,乙装置中铜棒的质量与起始通电前相等
难度: 中等查看答案及解析
-
在体积均为0.5L、pH均等于1的盐酸、醋酸溶液中,分别投入1.4g铁粉,则下图所示曲线比较符合客观事实的是( )
A.
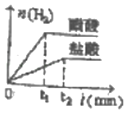 B.
B. 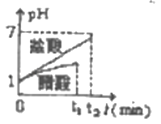
C.
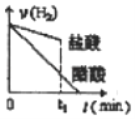 D.
D. 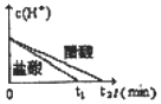
难度: 中等查看答案及解析
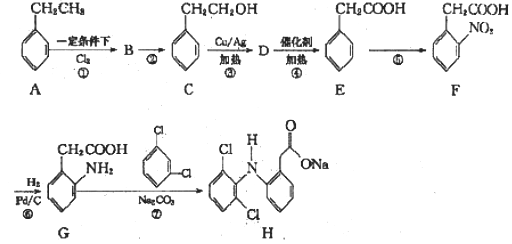
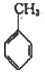 为原料制备
为原料制备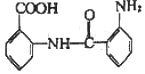 的合成路线(无机试剂任选)。___________________
的合成路线(无机试剂任选)。___________________