-
2018年10月21日,港珠澳大桥正式开通,该桥的建成创下多项世界之最,其中仅大桥主梁使用的钢材42万吨。下列材料中不属于铁合金的是
A. 生铁 B. 铁锈 C. 不锈钢 D. 铁锰合金
难度: 简单查看答案及解析
-
下列含 N 的物质中,属于电解质的是
A. N2 B. NO C. NH3 D. HNO3
难度: 简单查看答案及解析
-
生活中的下列物质,属于硅酸盐产品的是
A. 陶瓷 B. 水晶 C. 玛瑙 D. 沙子
难度: 简单查看答案及解析
-
下列物质不能用作干燥剂的是
A. 硅胶 B. 浓硫酸 C. Fe2O3 D. 固体 NaOH
难度: 简单查看答案及解析
-
下列物质在氯气中燃烧,不产生烟的是
A. 钠 B. 铜 C. 铁 D. 氢气
难度: 简单查看答案及解析
-
下列有关实验室制取氨气的操作中错误的是
A. 检查气密性
B. 装入药品

C. 制取气体

D. 收集气体
难度: 简单查看答案及解析
-
下列物质的俗名与化学式一致的是
A. 铁红——Fe2O3 B. 水玻璃——Na2SiO3
C. 纯碱——NaOH D. 明矾——KAl(SO4)2
难度: 简单查看答案及解析
-
氨水中不存在的粒子是
A. NH3 B. N3- C. NH4+ D. OH-
难度: 简单查看答案及解析
-
做焰色试验时,用于清洗铂丝的是
A. 盐酸 B. 硫酸 C. 硝酸 D. 碳酸
难度: 简单查看答案及解析
-
我国古代文献中有许多化学知识的记载,如《淮南万毕术》中提到“曾青得铁则化为铜”,其反应的化学方程式是 Fe+CuSO4=FeSO4+Cu,该反应不属于
A. 复分解反应 B. 置换反应 C. 离子反应 D. 氧化还原反应
难度: 简单查看答案及解析
-
还原铁粉与水蒸气反应的装置如图所示,下列有关该实验的说法正确的是

A. 反应生成FeO
B. 湿棉花的主要作用是冷却试管,防止炸裂
C. 肥皂液的主要作用是检验生成的H2
D. 铁粉与水蒸气反应后,可立即用磁铁将剩余铁粉分离出来
难度: 简单查看答案及解析
-
在无色溶液中大量共存的一组离子是
A. Cu2+、SO42-、K+、Cl- B. Ag+、Cl-、OH-、Na+
C. NO3-、Cl-、Na+、Ca2+ D. NO3-、OH-、Mg2+、Na+
难度: 简单查看答案及解析
-
下列试剂的保存或盛装方法中,错误的是
A. 钠保存在煤油中
B. 铁罐贮存浓硝酸
C. 新制的氯水保存在棕色玻璃瓶中
D. NaOH 溶液盛装在带玻璃塞的玻璃瓶中
难度: 简单查看答案及解析
-
物质X既能与稀盐酸反应,也能与氢氧化钠溶液反应,则X不可能是
A. Al2O3 B. NH4Cl C. NaHCO3 D. Al(OH)3
难度: 简单查看答案及解析
-
实验室用如图所示装置制取Fe(OH)2,下列说法正确的是
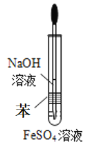
A. FeSO4溶液为黄色
B. 苯的作用是隔离氧气
C. 可将苯换成酒精进行实验
D. 沉淀的颜色变化是白色→灰绿色→红褐色
难度: 简单查看答案及解析
-
下列有关反应的离子方程式,书写正确的是
A. 硫酸滴在铜片上:Cu+2H+=Cu2++H2↑
B. 小苏打与稀盐酸的反应:CO32-+2H+=CO2↑+H2O
C. 向氢氧化钡溶液中滴加稀硫酸:H++OH-=H2O
D. 向AlCl3溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+
难度: 简单查看答案及解析
-
除去下列物质中混有的少量杂质(括号内为杂质),所用试剂或方法错误的是
物质(杂质)
除杂试剂或方法
A
CO2(SO2)
NaOH溶液
B
汽油(H2O)
分液
C
FeCl3溶液(FeCl2)
Cl2
D
Na2CO3固体(NaHCO3)
加热
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 30 g NO中所含原子数为2NA
B. 11.2 L Cl2中所含分子数为0.5NA
C. 1 mol•L-1 Na2CO3溶液中的Na+数为2NA
D. 56 g Fe与足量氯气反应,转移的电子数为2NA
难度: 简单查看答案及解析
-
将NaOH溶液逐滴滴入Y的溶液中,生成沉淀的物质的量与NaOH溶液体积的关系如图所示,则Y是

A. AgNO3 B. NaAlO2
C. AlCl3 D. Fe2(SO4)3
难度: 简单查看答案及解析
-
向 a g Al2O3、Fe2O3的混合物中加入100mL 0.05mol/L的盐酸中,固体全部溶解,再向其中加入NaOH溶液使Fe3+、Al3+恰好全部转化成沉淀,用去NaOH溶液100mL,则此NaOH溶液的浓度为
A. 0.2mol/L B. 0.1mol/L C. 0.05mol/L D. 无法计算
难度: 中等查看答案及解析