还原铁粉与水蒸气反应的装置如图所示,下列有关该实验的说法正确的是

A. 反应生成FeO
B. 湿棉花的主要作用是冷却试管,防止炸裂
C. 肥皂液的主要作用是检验生成的H2
D. 铁粉与水蒸气反应后,可立即用磁铁将剩余铁粉分离出来
高一化学单选题简单题
还原铁粉与水蒸气反应的装置如图所示,下列有关该实验的说法正确的是

A. 反应生成FeO
B. 湿棉花的主要作用是冷却试管,防止炸裂
C. 肥皂液的主要作用是检验生成的H2
D. 铁粉与水蒸气反应后,可立即用磁铁将剩余铁粉分离出来
高一化学单选题简单题
还原铁粉与水蒸气反应的装置如图所示,下列有关该实验的说法正确的是

A. 反应生成FeO
B. 湿棉花的主要作用是冷却试管,防止炸裂
C. 肥皂液的主要作用是检验生成的H2
D. 铁粉与水蒸气反应后,可立即用磁铁将剩余铁粉分离出来
高一化学单选题简单题查看答案及解析
铁粉和水蒸气反应的装置如右图所示,有关该反应的说法正确的是

A.该反应属于复分解反应
B.网罩的作用是集中火焰,提高温度
C.湿棉花的作用是给试管降温,防止炸裂
D.反应中水既不是氧化剂,也不是还原剂
高一化学选择题中等难度题查看答案及解析
铁粉与水蒸气反应的装置如图所示,有关该反应的说法正确的是( )
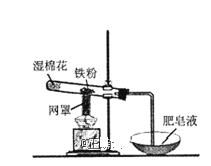
A.该反应属于复分解反应
B.网罩的作用是集中火焰,提高温度
C.湿棉花的作用是给试管降温,防止炸裂
D.铁与水蒸气在高温下的反应产物为Fe2O3和H2
高一化学单选题中等难度题查看答案及解析
已知在温度低于570°C时,还原铁粉与水蒸气反应的产物是FeO;高于570°C时,生成Fe3O4。老师用如图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。
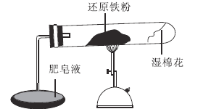
甲同学为探究实验后试管内固体的成分,进行了下列实验:

试回答下列问题:
(1)湿棉花的作用是_______________________________________________________ 。
(2)写出高于570°C时,Fe与水蒸气反应的化学方程式:______________________________________。
(3)乙同学认为加入KSCN溶液没有出现血红色原因可能是固体中没有Fe3O4,也有可能是因为______(填物质名称)过量造成的。该物质过量时,溶液中还会发生反应,导致加入KSCN溶液时没有出现血红色,该反应的离子方程式是___________________________________________________。
(4)丙同学利用上述实验①加盐酸后的溶液制取白色的Fe(OH)2沉淀,向滤液中加入足量NaOH溶液后,观察到的实验现象为_____________________________________________________________。
高一化学实验题中等难度题查看答案及解析
已知在温度低于570 0C 时,还原铁粉与水蒸气反应的产物是FeO,高于570 0C时,生成Fe3O4。老师用上图所示实验装置,完成了还原铁粉与水蒸气反应的演示实验。
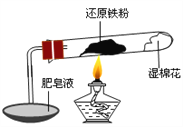
甲同学为探究实验后试管内的固体含有哪些物质,进行了下列实验:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末放入试管中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| ② | 向试管中滴加几滴KSCN溶液,振荡 | 溶液没有出现血红色 |
根据上述实验,下列说法不正确的是( )
A. 试管内的固体一定含有铁粉
B. 试管内的固体一定不含有Fe3O4
C. 不能确定试管内的固体一定含有FeO
D. 可通过将试管内固体彻底还原,分析其质量减小的方法来确定是否含有Fe3O4
高一化学单选题中等难度题查看答案及解析
下列有关铁及其化合物的说法中正确的是( )
A. 赤铁矿的主要成分是FeO
B. 铁与水蒸气在高温下反应的产物为Fe2O3和H2
C. 除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤
D. Fe3+与KSCN反应产生红色沉淀
高一化学单选题中等难度题查看答案及解析
下列有关铁及其化合物的说法中正确的是
A. 赤铁矿的主要成分是FeO
B. 除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤
C. 铁与水蒸气在高温下反应的产物为Fe2O3和H2
D. Fe3+与KSCN反应产生红色沉淀
高一化学单选题中等难度题查看答案及解析
下列有关铁及其化合物的说法中正确的是( )
A.赤铁矿的主要成分是FeO
B.铁与水蒸气在高温下反应的产物为Fe2O3和H2
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤
D.Fe3+与KSCN反应产生红色沉淀
高一化学单选题简单题查看答案及解析
高一化学选择题中等难度题查看答案及解析
铁不能与冷、热水反应,但能与水蒸气反应。资料显示,在不同温度下,铁粉与水蒸气反应的产物不同,温度低于570 ℃时,生成FeO,高于570 ℃时,生成Fe3O4。某学生用如图所示实验装置,完成还原铁粉与水蒸气反应的实验。
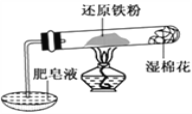
(1)实验中使用肥皂液的作用是____________。
(2)甲同学为探究实验后试管内的固体含有哪些物质,进行 了下列实验:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热 | 黑色粉末逐渐溶解,溶液呈绿色;有少量气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据上述实验,能确定固体中存在的物质有:______________________________;不能确定是否存在Fe3O4的原因是:___________________________________________。
(3)乙同学设计下列实验方案以确定实验后试管内的固体是否存在Fe3O4。
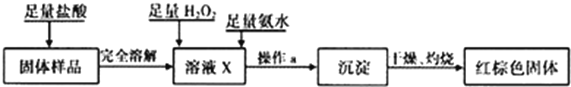
①溶液X中发生氧化还原反应的离子方程式为___________;
②操作a为_______,检验沉淀是否已经洗涤干净的操作是___________________。
(4)丙同学将试管内固体看做铁的氧化物(FexO),取出6.08 g溶于足量盐酸中,向所得溶液中通入448 mLCl2(标准状况),恰好将Fe2+完全氧化。则x=__________。
高一化学实验题中等难度题查看答案及解析